Цель урока: уметь определять кислоты, определять свойства кислот, уметь писать уравнение реакции. СОЦИАЛИЗАЦИЯ ЦЕЛИ: 1. Знания функциональные: обеспечение устойчивого понятия о свойствах кислот 2. Знания междисциплинарные: проявление индивидуального мыслительного потенциала 3. Знания, необходимые для изучения данной дисциплины: как научиться мыслить с помощью элементарной мыслительной операции «сравнение».
Просмотр содержимого документа
«химические свойства кислот »
Задание №1
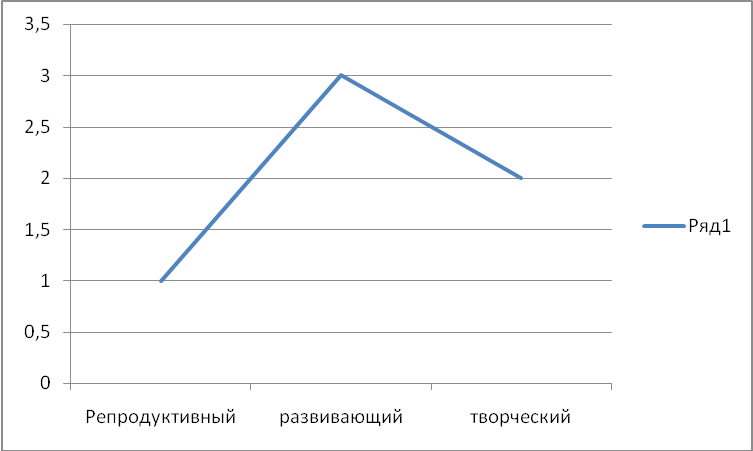
Протокол учебных заданий
№
Типология учебных заданий
Количество учебных заданий
1 2 3 4 5
1
Репродуктивный
1
2
Развивающийся
1
1
1
3
Творческий
1
1
План урока №1
Тема урока: Химические свойства кислот
Класс: 8
Преподаватель: Тахметова Адия Сайрановна
Дидактическая степень/категория: 1 квалификационная категория
Учебное заведение: КГУ Николаевская средняя школа, село Николаевка, Есильский район, Северо-Казахстанская область.
Базовый учебник: Химия, Н.Н Нурахметов 8 класс, Алматы «Мектеп»
1. Базовая компетенция: умение учиться
1.1 Составляющая компетенция: Как научиться мыслить/элементарные мыслительные операции
1.1.1 Метод, приём, операция, средство/цикл: приём «Сравнение»
Цель урока: уметь определять кислоты, определять свойства кислот, уметь писать уравнение реакции.
СОЦИАЛИЗАЦИЯ ЦЕЛИ:
1. Знания функциональные: обеспечение устойчивого понятия о свойствах кислот
2. Знания междисциплинарные: проявление индивидуального мыслительного потенциала
3. Знания, необходимые для изучения данной дисциплины: как научиться мыслить с помощью элементарной мыслительной операции «сравнение».
№
Учебное задание
Таксономия учебных задач по Блуму
( уровень)
Время в мин
Общее время: 45 мин
Организационная форма/форма оценивания
1
Укажите, как классифицируют кислоты, по каким признакам?
1 уровень
2 мин
Индивидуальная/самопроверка по ключу учителя
2
К каким кислотам относится H3 PO4 , HJ, H2 SiO3
К каким кислотам относится лимонная, уксусная, молочная?
1 уровень
2 мин
Индивидуальная/самопроверка по ключу учителя
3
Какие способы получения кислот ты знаешь? Напиши уравнения соответствующих реакции
2 уровень
4 мин
Индивидуальная/самопроверка по ключу учителя
4.
Напиши уравнение реакции получения угольной , азотной, хлороводородной кислот
3 уровень
10 мин
Парная/проверка учителя
5.
Используя ряд активности металов, закончитеуравнения тех реакции, которые осуществимы:
Mg+HCL→ AL+H2 SO4 → Fe+H2 SO4 → Cu+HCL→
4 уровень
4 мин
Работа в паре/самопроверка по ключу учителя
6
Какие из приведенных ниже веществ вступают в реакцию нейтрализации:H3 PO4 , KOH, H2 SO4 , NaOH, HCL
4 уровень
5 мин
Работа в паре/самопроверка по ключу учителя
7
При сильном нагревании ортофосфорная кислота, теряя воду, превращается в метафосфорную кислоту НРО3 . Напишите уравнение реакции.
5 уровень
10 мин
Индивидуальная/оценка учителя
8
Установите формулу вещества массовые доли которого составляют:
Н-24%, S-39,1%, O-58,5%
6 уровень
8 мин
Индивидуальная/оценка учителя
Поставь себе оценку! Если ты выполнил верно задания с 1 по 4 поставь себе «3», с 1 по 7, то «4», с 1 по 8 оценку «5».
СПАСИБО ЗА РАБОТУ!
Номер задания/максимальное количество баллов
уровень
1/1 балл
Знание
2/1 балл
Знание
3/ 2 балла
Понимание
4/ 3 балла
Применение
5/4 баллов
Анализ
6/4 баллов
Анализ
7/5 баллов
Синтез
8/6 баллов
Оценка
Итого всего баллов: 26 баллов
Результат урока
Порядковый номер
1
2
3
4
5
6
7
8
9
10
Задания выполненные
7
4
7
7
7
4
7
7
7
7
Оценка за урок
4
3
4
4
4
3
4
4
4
4
План урока №2
Тема урока: Уравнения химических реакции
Класс: 8
Преподаватель: Тахметова Адия Сайрановна
Дидактическая степень/категория: 1 квалификационная категория
Учебное заведение: КГУ Николаевская средняя школа, село Николаевка, Есильский район, Северо-Казахстанская область.
Базовый учебник: химия, Н.Н. Нурахметов Алматы: Атамұра 2011 год.
1. Базовая компетенция: умение учиться
1.1 Составляющая компетенция: Как научиться мыслить/элементарные мыслительные операции
1.1.1 Метод, приём, операция, средство/цикл: « Ромашка Блума»;
Цель урока: Изучить и отработать алгоритм написания уравнения химической реакции.
СОЦИАЛИЗАЦИЯ ЦЕЛИ:
1. Знания функциональные: условие составления химического уравнения.
2. Знания междисциплинарные: проявление индивидуального мыслительного потенциала
3. Знания, необходимые для изучения данной дисциплины: как научиться мыслить
№
Учебное задание
Таксономия учебных задач по Блуму
( уровень)
Время в мин
Общее время: 45 мин
Организационная форма/форма оценивания
1
Открой учебник, прочитай и дополни:
Алгоритм составления химических уравнений :
в левой части уравнения…
в правой части после стрелки … ;
число атомов уравниваем с помощью ….
1 уровень
5 мин
Индивидуальная/самопроверка по ключу учителя
2
Завершите схемы химических уравнений следующих реакций: Na+S→
K+P→
Mg+O2 →
1 уровень
«Ромашка Блума».
4 мин
Работа в паре/ оценка учителя
3
Расставьте коэффициенты в уравнениях следующих реакций: K+CL2 →KCL
Ba+O2 →BaO Ag+S→Ag2 S
Al+CL2 →ALCL3
2 уровень
5 мин
Работа в паре/самопроверка по ключу учителя
4
Объясняющий вопрос: Почему масса реагентов и продуктов одинакова и неизменна? Объясните это с точки зрения атомно-молекулярного учения.
3 уровень
5 мин
Работа в паре/ оценка учителя
5
Вместо точек напиши формулы соответствующих веществ, и расставьте коэффициенты в следующих химических уравнениях:
…+ О2 → ZnO
…+O2 →CaO …+O2 →Cr2 O3
4 уровень
6 мин
Индивидуальная/ оценка учителя
6
Составьте уравнения реакций, зная, что образуется одно вещество:
а) барий + кислород (О2 )→
б) натрий + хлор (СL2 )→
в) калий + сера→
г) литий + кислород→
5 уровень
10 мин
Работа в паре/самопроверка по ключу учителя
7
В состав горючего газа, используемого в быту, в основном входит органическое вещество- пропан С3 Н8 . Составьте уравнение реакции пропана с кислородом.
6 уровень
10 мин
Работа в группе/ оценка учителя
Поставь себе оценку! Если ты выполнил верно задания с 1 по 4 поставь себе «3», с 1 по 6, то «4», с 1 по 7 оценку «5».
СПАСИБО ЗА РАБОТУ!
Номер задания/максимальное количество баллов
уровень
1/1 балл
Знание
2/1 балл
Знание
3/ 2 балла
Понимание
4/ 3 балла
Применение
5/4 баллов
Анализ
6/5 баллов
Синтез
7/6 баллов
Оценка
Итого всего баллов: 22 балла
Результат урока
Порядковый номер
1
2
3
4
5
6
7
8
9
10
11
Задания выполненные
4
4
6
4
6
7
6
6
4
6
4
Оценка за урок
3
3
4
3
4
5
4
4
3
4
3
ОЦЕНКА:
1. На сколько информация для вас была нова: 7
2. Полезность полученных знаний и навыков для реальной работы: 9
3. На сколько курс был интересен: 6
4. Сложность подачи материала: 5
5. Уровень вашей подготовки для внедрения курса в практику: 5