Соли, их классификация и свойства
( сдвоенный урок в 8 классе) Учитель Некрасова Т.Н.
Цели и задачи:
Образовательные:
- Сформировать знания учащихся о солях как классе неорганических соединений;
- Привести в систему знания учащихся о классификации солей;
- Познакомить со свойствами и применением солей.
Развивающие:
- Развить умения и навыки работы с лабораторным оборудованием и химическими реактивами;
- Правильно оформлять результаты опытов, составлять уравнения реакций;
- Развивать умения наблюдать и делать выводы.
Воспитательные:
- Формирование всесторонне развитой личности;
- Воспитывать любовь к родному краю;
- Воспитание трудолюбия, взаимовыручки, умение работать в парах.
Методы: рассказ, беседа, демонстрация презентации “Соли”, выполнение лабораторной работы в парах с реактивами, работа с цифровыми лабораториями.
Оборудование: Цифровые лаборатории «Архимед», компьютер, мультимедийная презентация по теме урока, раздаточный материал – карточки; образцы солей и минеральной воды; транспаранты для магнитной доски; этикетки от минеральной воды; пробирки, колбы, растворы NaCI, AgNO3, Na2CO3, CuSO4, Fe (гвозди), NaOH, H2SO4, BaCl2, Cu, FeSO4.
Тип урока: комбинированный.
Ход урока
1 этап. Оргмомент. Проверка домашнего задания:
- у доски работают учащиеся с домашними упражнениями
- упражнение №1 с.221
- Химические свойства оксида калия
- Химические свойства оксида серы (VI).
- с места: повторить номенклатуру кислотных остатков. Повторить правила: – закончить фразу…
реакция нейтрализации – это …
кислоты – это …
оксиды – это …
классификация оксидов …
2 этап. Работа по теме урока
На демонстрационном столе образцы:
- мел (карбонат кальция)
- сода техническая (карбонат натрия)
- медный купорос (сульфат меди)
- поваренная соль (хлорид натрия
О чем мы будем говорить сегодня на уроке? (О солях)
Заполните, пожалуйста, 2 первые колонки в карточках
Что знаю по теме урока?
Что хотел бы узнать?
Что узнал на уроке?
Соли – самый многочисленный класс веществ.
Задание: составить формулу, описать свойства солей.
- СаСО3 – твердое вещество, белого цвета, нерастворимо в воде.
- Na2CO3 – твердое вещество, белого цвета, хорошо растворимо.
- CuSO4 – твердое вещество, синего цвета, хорошо растворимо.
- NaCl – твердое вещество, белого цвета, хорошо растворимо.
Вывод: соли - твердые вещества, отличаются цветом, растворимостью в воде.
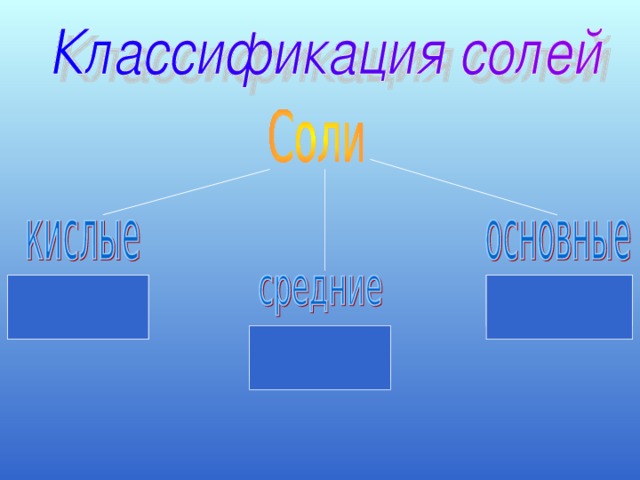
2 Классификация солей – учащиеся в парах работают с карточками
Na 2 CO3
Al OH Cl2
Cu SO4
Na H CO3
Cu OH Cl
Na HSO4
Выбрать знакомое, понятное и сгруппировать новые формулы. В итоге получается три группы формул.
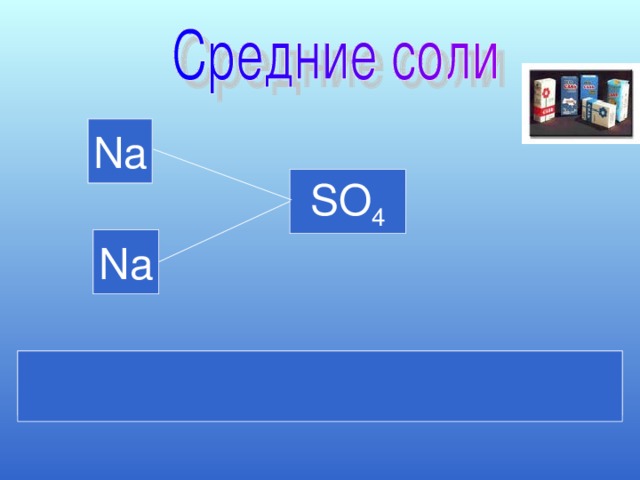
а) соли средние (нормальные): Na2CO3, CuSO4 на доске (магнитной) начинаем формировать схему. Записываем уравнение образования средней соли:
2NaOH + H2SO4 = Na2SO4 + 2H2O реакция обмена, нейтрализации.
Na2SO4 2Na+ + SO42- (1 cтупень)
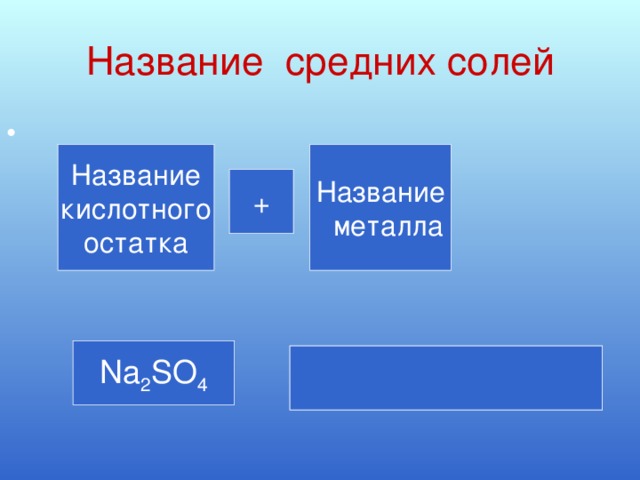
Название кислотного остатка и название металла
Na2SO4 Н Na
SO4 SO4
H Na
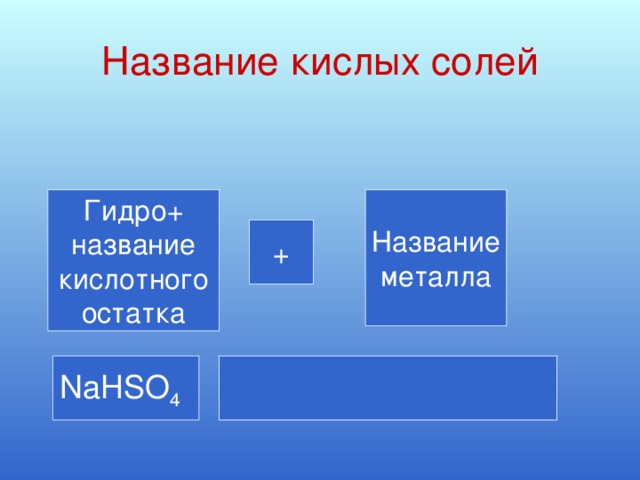
б) соли кислые: NaHСO3, NaHSO4 - результат неполного замещения атомов водорода в кислоте на атом металла.
NaOH + H2SO4 = NaHSO4 + H2O
NaHSO4 Na+ + HSO4- (1 степень)
HSO4 H+ + SO42- (2 степень) – эта степень с меньшей степенью диссоциации.
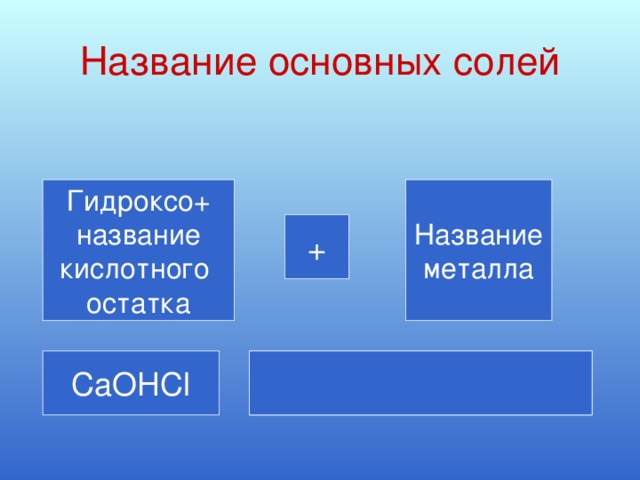
в) соли основные:
Ca(OH)2 + HCl = CaOHCI + H2O
CaOHCl CaOH+ + Cl- (1 ступень)
CaOH+ Ca2+ + OH- (2 ступень) очень незначительна.
Гидроксо +название кислотного остатка и название металла
3этап.
Закрепление: провести исследование состава минеральных вод Калининградской области, используя этикетки производителей. Работа выполняется на местах, парами – учащиеся получают карточку с заданиями и этикетку от конкретной воды.
В это же время ученики работают у доски с магнитами и карточками по этикеткам от минеральных вод
Задание 1. Используя этикетку от минеральной воды, исследуйте ее солевой состав:
- сделайте заголовок – название воды;
- найдите химический состав, в тетради запишите отдельно катионы (ионы +) и анионы (ионы - )
- составьте из ионов формулы солей (+) например: 2Na+ + SO42- Na2SO4
- подчеркните формулы кислых солей, назовите их.
- подсчитайте общее число получившихся формул солей
Обсудить полученные результаты.
- Где расположен источник?
- С какой глубины происходит подъем воды?
- К какому типу минеральных вод она относится?
- Какая еще информация есть на этикетке?
- Личное отношение к минеральным водам.
Выслушиваем несколько ответов.
3 группы работают в это время с «Архимедом», определяя рН и вывести результаты исследования на экран в презентацию.
Выслушиваем отчет групп и рекомендации по потреблению минеральной воды.
4 этап
Химические свойства солей (практическая работа по группам)
Проведение реакций по группам с реактивами, стоящими на столах.
2 свойства солей мы с вами уже изучили.
- Какие? С чем реагируют кислоты? (Ответы ребят и проведение опытов с кислотами и основаниями).
- Что получилось? Комментарии.
- А как вы думаете, с чем еще могут реагировать соли? (Друг с другом)
- Любые соли или есть условие протекания реакции? (Осадок)
- Проведите реакцию между нитратом серебра и хлоридом натрия.
- А как вы думаете, с чем еще могут реагировать соли? ( С металлами)
- Со всеми? (только, стоящими в ряду напряжений до водорода) проделываем опыт с гвоздем.
5 этап Подведение итогов
- Что нового узнали на уроке?
- Что было интересно?
- Выставление оценок
Домашнее задание: §41, упражнение № 1,5 стр. 225
Задача (если останется время, то на уроке; если нет, то домой)
Мы каждый день употребляем в пищу соль - хлорид натрия.
- Где она еще применяется?
Она применяется для обработки кожевенного и мехового сырья.
Ученые подсчитали, что человек в день употребляет 12-15г соли. Сколько соли съели вы за свою жизнь!
Сделаем следующий расчет потребления соли, взяв за основу
15г - в сутки.
За месяц 15г х 30 = 450г
За год 450г х 12 = 5400г
Теперь рассчитайте, сколько вы съели соли за свою жизнь. Для этого количество соли, которое вы употребили за год, умножьте на свой возраст.
- Сколько получилось?
Методическое руководство по выполнению практической работы «Химические свойства солей»
Проведите реакции, характеризующие общие свойства солей.
Порядок выполнения опытов:
1 опыт Взаимодействие сульфата меди (II) с гидроксидом натрия
2 опыт А) Взаимодействие хлорида бария с серной кислотой
Б) Взаимодействие карбоната натрия с серной кислотой
3 опыт Взаимодействие нитрата серебра и хлорида натрия
4 опыт Взаимодействие солей с металлами, стоящими в ряду напряжений
до водорода: сульфат меди (II) и железо;
сульфат железа (II) и медь.
После проведения опытов заполните таблицу:
Что делали
Наблюдения
Уравнения реакции (молекулярное и ионное)