Разработка урока для учащихся 10-го класса, пользующихся учебником О.С. Габриеляна. Цель урока – знакомство учащихся с особенностями строения, гомологическим рядом, изомерией, номенклатурой алканов, их получением. Урок разработан с использованием личностно ориентированного подхода, сопровождается презентацией. Имеет четкую методическую структуру, тип: изучение нового материала, содержит элементы контроля знаний.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
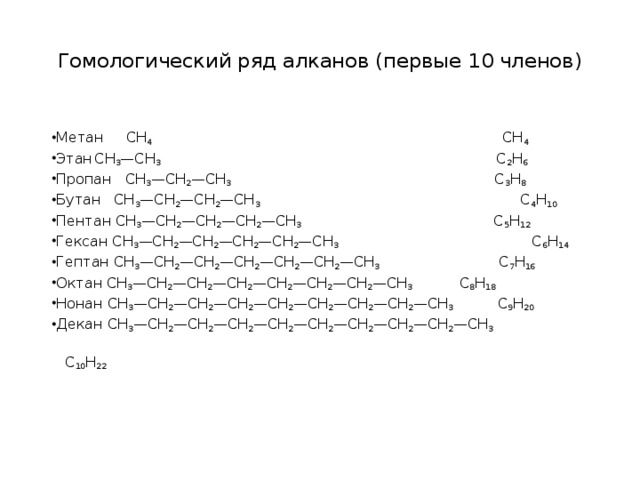
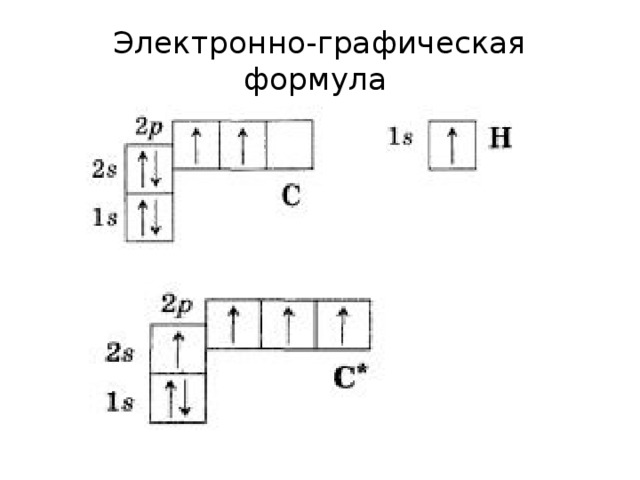
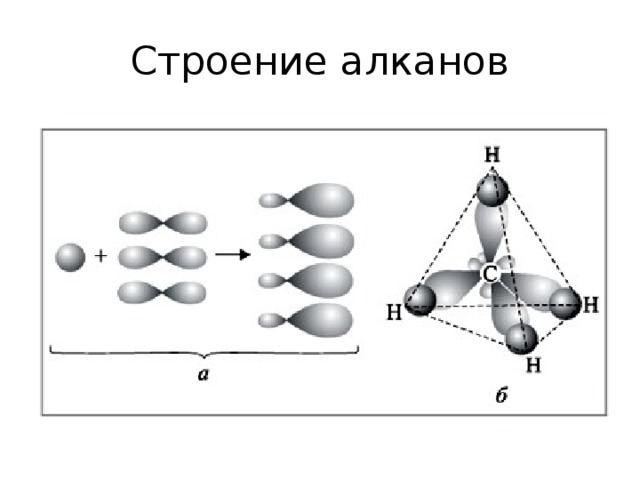
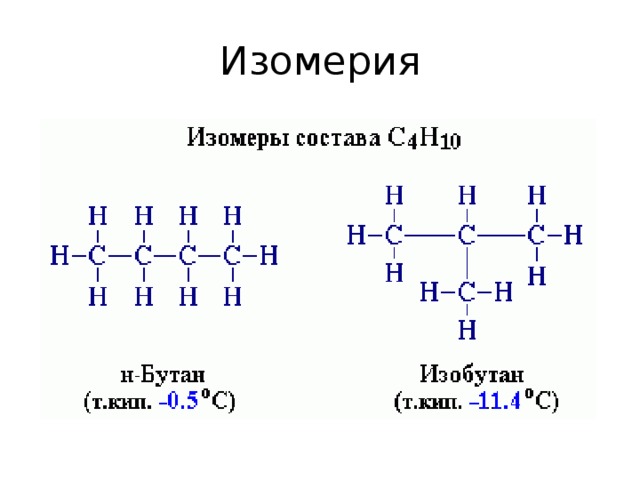
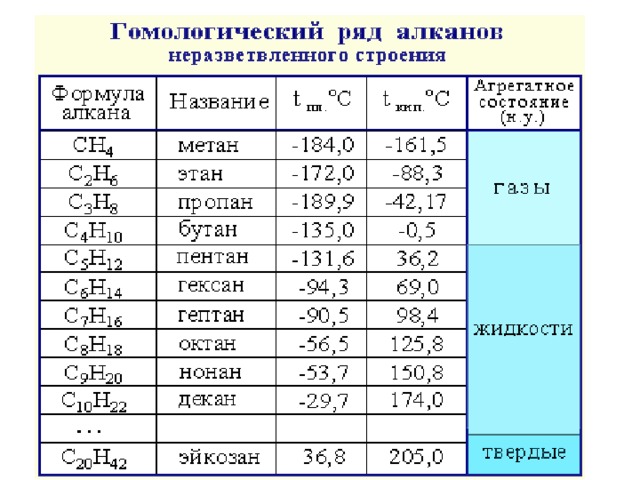
Алканы, состав, строение, получение
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Алканы, состав, строение, получение
»
Похожие файлы
Полезное для учителя
Распродажа видеоуроков!
1660 руб.
2760 руб.
1690 руб.
2820 руб.
1520 руб.
2530 руб.
1660 руб.
2760 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства