ТЕМА. КИСЛОТЫ В ПРИРОДЕ. ПРИМЕНЕНИЕ КИСЛОТ.
Цель: Способствовать умениям учащихся составлять уравнения химических реакций, которые характеризуют химические свойства кислот, углубить знания учащихся о их классификации, выяснить области применения кислот и нахождение их в природе;
создать условия для развития познавательных процессов: памяти, внимания, мышления, развитие умений работать вместе, развитие коммуникативных умений, навыков ориентироваться в информационном пространстве, развитие творческого и критического мышления;
способствовать формированию познавательной заинтересованности предметом, воспитание чувства уважения друг к другу.
Оборудование: карточки, компьютер, презентация, стихи о кислота, микрофон.
Тип урока. Комбинированный.
ХОД УРОКА.
I.ОРГАНИЗАЦИОННЫЙ МОМЕНТ.
II.ПРОВЕРКА ДОМАШНЕГО ЗАДАНИЯ.
Работа с классом у доски.
1. Осуществите превращения.
а) медь + серная кислота =
б) оксид натрия + азотная кислота=
в) натрий + азотная кислота=
г) углекислый газ + оксид магния=
д) оксид серы + вода =
2. Определите массовую долю серы в серной и сероводородной кислотах.
Работа по карточкам:
1)P-P2O5-K3PO4
↓
H3PO4
2) Ca-CaO-CaSO4
↓ ↓
Ca(OH)2
Работа с классом.
Расскажите о ПТБ при работе с кислотами.
Расскажите о смешивании кислот.
III.АКТУАЛИЗАЦИЯ ОПОРНЫХ ЗНАНИЙ.
Стихи о кислотах.
HNO3
Cредь кислот одна из главных,
Людям я служу исправно.
Если где-то там стреляют,
Поджигают и взрывают,
Это все свершила я—
Кислота азотная.
Но не только для солдат
Очень так стараюсь я.
Вы спросите у крестьян,
Пусть они признаются:
Чтобы вырос урожай
Помидоров в поле,
Обойтись никак нельзя
Без нитратной соли.
H3PO4
Фосфорная кислота
В обращении проста.
Служит людям много лет,
С ней достигнешь ты побед.
Чтоб растенья крепче были,
Не болели и не гнили,
Их бы нужно подкормить,
Удобренья применить.
И если рост дает азот,
То фосфор силу им дает.
А двойной суперфосфат
Вдвое больше даст заряд.
H2CO3
Очень вкусная всегда
Минеральная вода.
Но без углекислоты
Не получишь её ты.
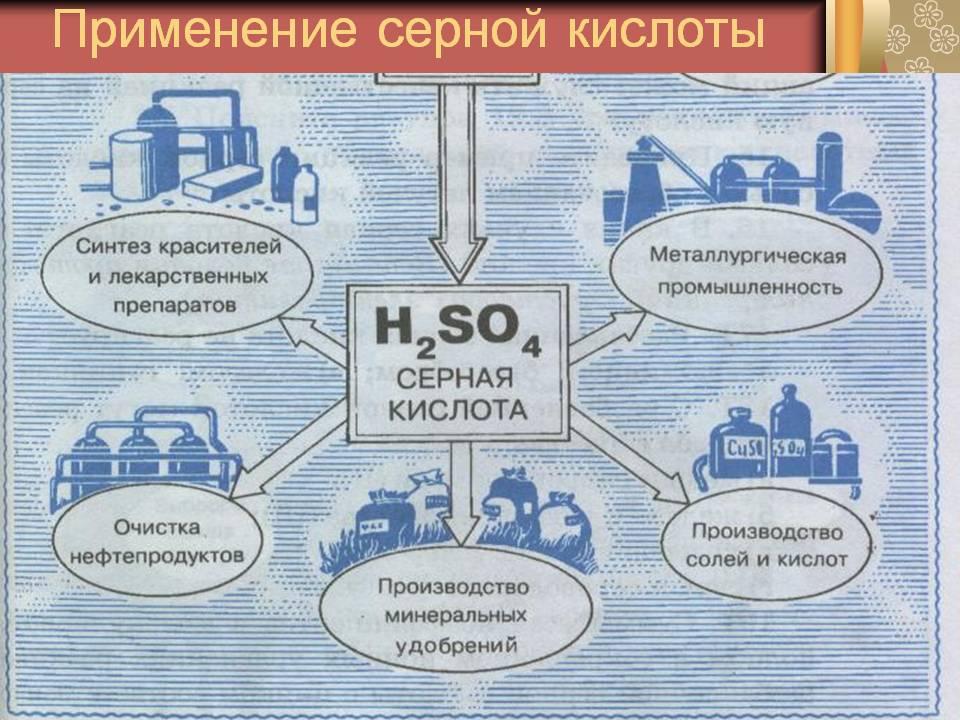
H2SO4
Известная в целом мире.
Её хоть и не знают,
Но всё же применяют.
Она очистит газы
И их осушит сразу,
Краситель образует
И взрыв организует,
Основа для лекарства
И сельского хозяйства,
Получит удобренья
И сахар для варенья.
Она - в аккумуляторе,
В химическом реакторе
И в производстве каждый час
Всегда важна, как кровь для нас.
Физкульт. минутка.
IV.ИЗУЧЕНИЕ НОВОГО МАТЕРИАЛА.
Учитель. Как вы уже, дети, догадались, сегодня мы с вами будем говорить о применении кислот. А так же мы посмотрим, где они встречаются в природе. Озвучивается тема и цели урока.
1. Кислоты в природе. Презентация.
2. Применение кислот. Презентация.
3. Применение кислот. Работа со схемой с 80.
V.ОБОБЩЕНИЕ И СИСТЕМАТИЗАЦИЯ ЗНАНИЙ.
Метод «Микрофон»
Ребята по очереди рассказывают где применяются кислоты.
VI.ДОМАШНЕЕ ЗАДАНИЕ.§16, с 80, проработать Рис. 12.
Подготовить сообщение:
1. группа соляная кислота.
2. группа серная кислота.
3. группа азотная кислота.
4. группа угольная кислота.
VII.ПОДВЕДЕНИЕ ИТОГОВ УРОКА