Учитель биологии и химии МОУ СОШ №5 г.Ртищево Саратовской области Гиря Т.В.
Интегрированный урок по теме: «Аминокислоты. Белки»
Цели урока:
1.Изучить строение, номенклатуру, химические свойства аминокислот и белков, продолжить формировать умение предполагать свойства вещества на основании его строения.
2. На основе межпредметных связей биологии и химии продолжить расширение и углубление знаний о важнейших органических веществах клетки на основе строения белков, сформировать знания о важнейшей роли белков в органическом мире.
Задачи урока:
Образовательные:
продолжить формирование у учащихся знаний о составе и строении аминокислот и белков, уметь объяснять функции белков на примерах, провести связь между биологическими и химическими процессами.
Развивающие:
развитие умений сравнивать состав и строение различных органических веществ (белков, жиров, углеводов), умение выполнять творческие задания.
Воспитательные:
продолжить формирование убежденности в познаваемости мира на основе знаний о строении, составе и свойствах органических веществ, признание ценности знаний для саморазвития, трудолюбия.
Универсальные учебные действия
| Технология проведения | Планируемые результаты |
| Предметные | УУД |
| I. Мотивация к учебной деятельности | Знать: значимость аминокислот; их открытие и способ получения для нормальной жизнедеятельности человека | Личностные:
уметь отражатьличное видениевопроса Регулятивные:
уметь вставить правильный ответ во время беседы Коммуникативные:
уметь общаться с учителем во время беседы Познавательные:
уметь применить во время беседы известные факты |
| II. Формулирование темы урока, постановка цели | Знать: функциональные группы аминокислот; основный характер аминогруппы; кислотный характер карбоксильной группы; амфотерность как двойственную природу взаимодействия; пример амфотерного неорганического и органического соединения | Личностные:
уметь быстро дать правильный ответ
Регулятивные:
уметь оперативно оценивать ответы (свои и своих одноклассников)
Коммуникативные:
умение работать на всю аудиторию
Познавательные:
узнать факты или дополнить свои знания
|
| III. Изучение нового | Знать: физические свойства аминокислот;
химические свойства аминокислот;
их номенклатуру;
гомологи и изомеры;
получение; применение
| Личностные:
умение проводить исследование
Регулятивные:
использование самопроверки и взаимопроверки и сравнение с образцом
Коммуникативные:
умение работать в группе и в паре
Познавательные:
умение применять получаемые знания на практике, при выполнении упражнений
|
| IV. Закрепление нового | Знать применение аминокислот; некоторые их специфические свойства; биологическую значимость и фармакологическую ценность некоторых аминокислот | Личностные:
умениеподготовить сообщение
Регулятивные:
уметь переработать материал в соответствии с поставленными условиями
Коммуникативные:
умение выступить перед классом
Познавательные:
применить материал для данной ситуации
|
| V. Контролирующее задание | Знать: номенклатуру соединений ряда аминокислот; их амфотерность и химические свойства; уметь составлять структурные формулы аминокислот; уметь применить на практике | Личностные:
умение понять формулировку задания
Регулятивные:
самопроверка теста
Коммуникативные:
умение признать свои ошибки или адекватно оценить правильный ответ
Познавательные:
умение сконцентрировать своё внимание на заданных вопросах
|
| VII. Рефлексия учебной деятельности на уроке | Знать: изученный материал в полном объёме; ход урока; деятельность на уроке свою и своих одноклассников; уметь давать оценку различным видам работы | Личностные:
уметь высказыватьличное мнение
Регулятивные:
уметь оценивать себя и других
Коммуникативные:
умение вести дискуссию
Познавательные:
уметь видеть в уроке и изучение теории, и этапы его ведения
|
Тип урока: изучение и первичное закрепление новых знаний.
Форма организации учебного процесса: работа в группах.
Технологии: личностно-ориентированные, частично-поисковая, проблемная.
Методы: объяснительно - иллюстративный, работа в группах, решение биологических задач с использованием технологии ТРИЗ, сообщения учащихся, лабораторная работа, методы контроля.
Основные понятия: полипептид, биополимеры, мономеры, аминокислоты, пептидная связь, структуры белков (первичная, вторичная, третичная, четвертичная), состав белков, денатурация, ренатурация, гидролиз белков. Цветные реакции на белки.
Планируемые результаты обучения: знать строение, состав аминокислот и белков, структуры белков. Знать понятия: денатурация, ренатурация. Знать каталитическую и ферментативную функцию белка. Знать, как от строения молекулы зависят ее свойства. Знать влияние факторов среды на белковые молекулы, уметь приводить примеры влияния среды на белковые тела. Уметь проводить реакции на белки, делать выводы.
Главная проблема урока.
Почему, по мнению ученых, белки являются носителями жизни?
Оборудование: компьютер, медиапроектор, презентация, раздаточный материал, опорный конспект, пробирки, спиртовка, держатель для пробирок.
Реактивы: глицин, растворы белка куриного яйца, гидроксида натрия, сульфата меди,соляной кислоты, метиловый оранжевый ,лакмус, концентрированная азотная кислота, этиловый спирт.
Ход урока
Эпиграф :
«С полным основанием можно утверждать, что эти вещества – самые важные из всех веществ, входящих в состав организмов животных и растений».
Л. Полинг
| Этапы урока | Содержание | Вид деятельности |
| I.Мотивация к учебной деятельности
II. Актуализация знаний:
| Здравствуйте, сегодня мы проведем с вами интегрированный урок по биологии и химии. На уроках биологии мы с вами познакомились с положениями клеточной теории. Одним из положений является то, что все живые организмы имеют сходный химический состав. Любой живой организм состоит из веществ, которые подразделяются на 2 группы. Какие это группы? (органические и неорганические). Заполните схему. К органическим веществам относят? (белки, жиры, углеводы и нуклеиновые кислоты), а к неорганическим (вода и минеральные соли). Прочитайте эпиграф урока. Обратите внимание на выделенные слова. На уроке мы определим, что это за вещества. А пока заслушаем сообщение об авторе этих строк. (Приложение 1) Отгадайте о каких же веществах пойдет речь на уроке? 1. В организме человека их около 5 миллионов. 2. В 2 раза их больше в животной клетке, чем в растительной. 3. Это органические вещества. 4. Составляют 50% сухой массы клетки. 5. Второе название протеины, латинское название Protos, что в переводе обозначает – первый. Совершенно верно, это белки. А из чего образуются белки в живых организмах? (Приложение2) Видеофрагмент(синтез белка) Правильно из аминокислот. Итак, тема урока «Аминокислоты . белки» Перед вами на слайде представлены цель и задачи урока, а также план работы на уроке. | Слушают учителя.
Заполняют схему. Заслушивают сообщение.
Определяют тему урока, цели и задачи , записывают в тетрадь. |
| III. Изучение нового материала
IVПервичное закрепление материала
V.Рефлексия
VI. Задание на дом.
| «Кирпичиками» белков являются аминокислоты. Организуется самостоятельная работа (Прилоложение 3) Задание 1.Найдите определение аминокислот в учебнике и запишите в тетрадь. Запишите общую формулу аминокислот. Ознакомьтесь с материалом учебника стр. 123 и определите, как образуются названия аминокислот. По систематической номенклатуре аминокислоты называют так же, как карбоновые кислоты, но сначала указывают положение и название аминогруппы. Например, 3 2 1 NH2─СН2─СН2─СООН 3-аминопропановая кислота Но существует и рациональная номенклатура, когда положение аминогруппы указывается буквами греческого алфавита. β α NH2─СН2 ─СН─СООН β–аминопропионовая кислота Часто аминокислотам организма, образующим белки, дают эмпирические названия: NH2─СН2─СООН глицин (аминоэтановая кислота, аминоуксусная кислота) СН3─СН─СООН │ NH2 аланин (α-аминопропионовая, 2-аминопропановая кислота) Назовите представленные аминокислоты. Физические свойства аминокислот Аминокислоты – бесцветные кристаллические вещества, хорошо растворимые в воде, температура плавления 230-3000, многие аминокислоты имеют сладкий вкус. Для изучения химических свойств аминокислот выполните лабораторную работу и ответьте на вопросы. Опыт 1. Отношение аминокислот к индикаторам. Реактивы и материалы: аминоуксусная кислота, раствор; метиловый оранжевый, раствор, лакмус, раствор. В пробирку помещают 2 капли раствора аминоуксусной кислоты и добавляют 1 каплю метилового оранжевого. Такой же опыт проделывают с лакмусом. Результат: Окраска индикаторов не меняется. Вывод: Аминокислоты обладают как кислотными, так и основными свойствами; кислотная группа - СООН и основная - NH2 взаимно нейтрализуются, следовательно, аминокислоты имеют структуру амфотерных, или биполярных, ионов (внутренние соли): H3N+-СН2-СОО-. Поэтому водные растворы одноосновных моноаминокислот нейтральны по отношению к индикаторам. Помимо этого кислоты способны вступать в реакцию друг с другом, образуя пептиды (реакция поликонденсации). Запишите это уравнение, опираясь на материал учебника стр. 125. Эта реакция лежит в основе синтеза белка. За счет, какой связи образуются пептиды? Запищите определение в тетрадь. О значение аминокислот мы заслушаем сообщение. (Приложение 4) Белки, по утверждению Ф. Энгельса, одна из форм существования жизни. История изучения белков. В начале XX века выяснил строение молекул белка немецкий химик Эмиль Герман Фишер.(стр.128). Он выдвинул пептидную теорию строения белка, согласно которой белки представляют собой цепи остатков аминокислот, соединенных пептидными связями. В 80-х годах XIX века русский биохимик Данилевский А.Я.(стр.129) обнаружил в белковой молекуле пептидные группы. Таким образом, белки – это сложные биополимеры, мономерами которых являются аминокислотные остатки. Известно несколько сотен аминокислот, но обычно только 20 из них используются организмом для биосинтеза белка, их называют незаменимыми аминокислотами. Из этих 20 аминокислот может быть образовано 2 432 902 008 176 640 000 комбинаций, то есть различных белков. Структуры белка. Самостоятельная работа с учебником 128-129. Задания Прочитайте материал на стр. 128-129. Ответьте на вопросы. 1. Назовите не менее четырех особенностей структуры молекулы белка. 2.Чем отличаются структуры молекула белка друг от друга? 3. Запишите в таблицу информацию о структуре белка, используя текст параграфа 17 на стр. 129 и табл. №4 | Структуры белка | Связи, образующие структуру | Конфигурация белка | |
|
|
| |
|
|
| Функции белка Задание Используя материал на стр. 131-132 и сопоставьте белки и их функции. | Функция | Название белка | Структурная | Гемоглобин | Ферментативная | Амилаза | Транспортная | Коллаген | Защитная | Альбумин | Сигнальная | Антитела | Энергетическая | Рецепторы | Учащимся предлагается решить следующие задачи: (Приложение 4) Задача 1. Известно, что для взрослого человека необходимо 1,5 г белка на 1 кг массы. Зная свою массу, определите норму необходимого потребления белка для своего организма. Задача 2. Известно, что при продолжительности жизни 70 лет обновление белка в организме происходит в среднем 200 раз. Зная свой возраст, предположите, сколько раз произошло обновление белка в вашем организме. Вывод: Белок является основным компонентом питания. Биологическая ценность белков определяется содержанием в них незаменимых аминокислот. Недостаток белков или нарушение процессов их усвоения (переваривание и всасывание) приводят к развитию жировых отложений в печени, к болезням крови и ослаблению иммунитета. Большое потребление белков ведет к образованию в желудочно-кишечном тракте продуктов неполного расщепления, что может вызвать интоксикацию организма, поэтому нужно помнить о рациональном питании и в пищу должны употреблять продукты, имеющие полноценное белковое содержание. Физико-химические свойства белков Выступление учащегося Природные белковые вещества крайне разнообразны: некоторые белки – твердые вещества, не растворимые в воде и солевых растворах, большинство белков жидкие или студнеобразные вещества, растворимые в воде (например альбумин(белок куриного яйца). Белки из растворов осаждаются концентрированными растворами аминокислотных солей и солей щелочных металлов. Если к раствору куриного белка прилить сульфата аммония – жидкость мутнеет и появляется осадок. Добавление к раствору белка солей тяжелых металлов Нд, Рв, Си и т.д приводит к осаждению белка не растворяющегося в воде. Поэтому для организма крайне вредны пары тяжелых металлов и их солей. Осаждение белков происходит так же концентрированными кислотами НNО3, Н2SО4, формалином и фенолом, а также этиловым спиртом, при действии радиации, даже сильного встряхивания- когда мы сбиваем белок в гоголь-моголь. При слабом нагревании белки свертываются. Химические свойства белков. Растворимость белков Гидролиз белков Цветные реакции белков: биуретовая, ксантопртеиновая Амфотерный характер белковых молекул (амфотерность белков) Лабораторная работа Опыт 1. К раствору белка добавить раствор сульфата меди (II); Пронаблюдать изменения, отнести их к определенным свойствам. Опыт 2. К раствору белка добавить столько же раствора гидроксида натрия. К смеси прилить 2-3 капли раствора сульфата меди (II). Пробирку встряхнуть и наблюдать изменение цвета. Опыт 3. прилить в пробирку 2 мл раствора белка. Добавить по каплям 0,5 мл раствора азотной кислоты (конц.). Нагреть пробирку. Наблюдать изменение цвета. Вывод: Процессы осаждения и свертывания белков связаны с разрушением их вторичной и третичной структур, потерей свойств. Такой процесс называется денатурацией белка. Процесс восстановления структуры белка называется ренатурацией. Для распознавания белковых веществ используются цветные реакции: стр. 130-131, рис.77-78 Биуретовая реакция белок + щелочь+ CuSO4 = фиолетовое окрашивание; Ксантопротеиновая реакция белок+ HNО3 = желтое окрашивание Значение белков многогранно. Рассмотрите схему (Приложение 3) Ответьте на вопрос: Почему же Ф.Энгельс определил белки как основу жизни на Земле? Так как они являются основными веществами, поддерживающими жизнь на Земле. Вывод. белки – это высокомолекулярные органические соединения, биополимеры, состоящие из мономеров - аминокислот; аминокислоты соединяются в полипептидную цепочку за счёт пептидной связи; аминокислоты заменимые и незаменимые; белки могут быть простыми и сложными; четыре структуры белка (первичная, вторичная, третичная и четвертичная); денатурация – это утрата белковой молекулой своей структурной организации; ренатурация - процесс восстановления структуры белка; из органических соединений, входящих в живую клетку, важнейшую роль играют белки, на их долю приходится около 50% массы клетки; белки выполняют разнообразные функции в живой материи. Проверь себя (Приложение 6) Главными носителями жизни являются … . … - это сложные высокомолекулярные соединения, построенные из … . Молекулярная масса белков изменяется от … до … . Многие белки растворимы в …, почти все растворяются в … . Нерастворимы белки, из которых построены В структуре белка различают … структуры. Функции белков в организме … . Ответы: 1. Белки. Белки; остатков α – аминокислот. Десяти тысяч, миллионов. Воде, растворах солей, кислот; щелочах. Ткани живых организмов: кожа, сухожилия, мышцы, ногти, волосы. Первичную, вторичную, третичную, четвертичную. Строительная, каталитическая, двигательная, транспортная, защитная, энергетическая. Критерии оценки: «5» - все ответы правильные «3» - 3 неверных ответа; «4» - 1-2 неверных ответа; «2» - 4 и более неверных ответов. Рефлексия «Классическая»: 1. Каковы были Ваши цели перед занятием, и насколько их удалось реализовать? 2. Перечислите трудности, с которыми Вы столкнулись: а) при изучении темы (раздела); б) при ответе на открытые задания. 3.Каким образом Вы преодолевали трудности? За счет чего? 4.Каков главный результат для Вас лично при изучении темы? 5. Чему Вы научились лучше всего? Выставление оценок. §17упр. 2, 10. Задача. Определите формулу аминокислоты, если массовые доли углерода, водорода, кислорода и азота соответственно равны: 48%, 9,34%, 42,67% и 18, 67%. Напишите все возможные структурные формулы и назовите их. Учитель. Вот и подошел к концу наш урок. Ваш багаж знаний пополнился еще одной темой. Всем спасибо за урок! | Работа с учебником п.17, стр. 122,123. Составляют опорный конспект.
Составляют формулу и называют вещество.
Учащиеся выполняют лабораторную работу
Учащиеся слушают учителя
Записывают уравнение реакции поликонденсации Записывают определение в тетрадь. Выступление учащегося.
Учащиеся слушают учителя
Выполняют задания
Просмотр презентации, подготовленной учащимся. Выполняют задание
Решают биологические задачи.
Результаты задач обсуждаются, делаются выводы.
Слушают выступление
Выполняют лабораторную работу и формулируют выводы.
Слушают учителя , наблюдают. Работают со схемой и отвечают на вопрос.
Формулируют вывод.
Выполняют проверочную работу(диктант)
Проводят самооценку своей деятельности на уроке.
Записывают домашнее задание.
|
Приложение 1
ПОЛИНГ (Pauling) Лайнус Карл (родился 28 февраля 1901, Портленд, штат Орегон, США — 19 августа 1994, Биг Сур, штат Калифорния), выдающийся американский химик и физик, общественный деятель. Полинг получил химическое образование в Орегонском государственном сельскохозяйственном колледже (1917-22), а затем в Калифорнийском технологическом институте в Пасадене (1922-25).
В 1925 он защитил докторскую диссертацию по результатам исследования в области рентгеноструктурного анализа неорганических соединений
Получив стипендию для совершенствования научной подготовки, он поехал в Европу (1926-27), где занимался изучением атомной физики и квантовой теории
В 1927 Полинг вернулся в Калифорнийский технологический институт в качестве ассистента профессора химии, с 1931 он занимал должность профессора химии, на которой работал до 1964. Научные работы Полинга посвящены главным образом изучению строения молекул и природы химической связи методами квантовой механики
Его первые исследования относились к кристаллографии.. За работы в этой области он первым получил премию И. Ленгмюра (1931).
Он создал (1931-33) теорию резонанса, которая исходит из того, что не каждую молекулу можно описать при помощи лишь одной электронной структуры . В 1939 Полинг выпустил книгу «Природа
химической связи», которая стала одной из самых известных монографий, посвященных современной структурной химии (на русском языке вышла в 1947).
С 1940-х годов Полинг заинтересовался вопросами биохимии. Он начал изучать структуру сложных молекул живых тканей. Совместно с Дж. Д. Берналом и У. Брэггом Полинг заложил основы структурного анализа белковых молекул (1946-50). Он разработал представления о структуре полипептидной цепи в белках, впервые высказал мысль о ее спиральном строении и дал описание альфа-спирали (1951, совместно с американским биохимиком Р. Б. Кори).
Приложение 2
Видеофрагмент –синтез белка
Приложение 3
Опорный конспект для работы на уроке
Задание 1.Найдите определение аминокислот в учебнике и запишите в тетрадь.
Запишите общую формулу аминокислот. 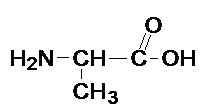
Ознакомьтесь с материалом учебника стр. 123 и определите, как образуются названия аминокислот.
Задание 2. Назовите аминокислоты.
1.СН3─СН─СООН
│
NH2
2. NH2─СН2─СН2─СООН
Задание 3 Лабораторная работа.
Опыт 1. Отношение аминокислот к индикаторам.
Реактивы и материалы: аминоуксусная кислота, раствор; метиловый оранжевый, раствор, лакмус, раствор.
В пробирку помещают 2 капли раствора аминоуксусной кислоты и добавляют 1 каплю метилового оранжевого. Такой же опыт проделывают с лакмусом.
Каковы ваши наблюдения и какой вывод вы можете сделать?
Задания 4
Прочитайте материал учебника на стр. 128-129.
Ответьте на вопросы.
1. Назовите не менее четырех особенностей структуры молекулы белка.
2.Чем отличаются структуры молекула белка друг от друга?
3. Запишите в таблицу информацию о структуре белка, используя текст параграфа 17 на стр. 129 и табл. №4
| Структуры белка | Связи, образующие структуру | Конфигурация белка |
|
|
|
|
Задание 5
Используя материал на стр. 131-132 и таблицу 4 ,сопоставьте белки с их функциями.
| Функция | Название белка |
Структурная | Гемоглобин |
Ферментативная | Амилаза |
Транспортная | Коллаген |
Защитная | Альбумин |
Сигнальная | Антитела |
Энергетическая | Рецепторы |
Задание 6 Лабораторная работа
Опыт 1.К раствору белка добавить раствор сульфата меди (II). Пронаблюдать изменения, отнести их к определенным свойствам.
Опыт 2.К раствору белка добавить столько же раствора гидроксида натрия. К смеси прилить 2-3 капли раствора сульфата меди (II). Пробирку встряхнуть и наблюдать изменение цвета.
Опыт 3.Прилить в пробирку 2 мл раствора белка. Добавить по каплям 0,5 мл раствора азотной кислоты (конц.). Нагреть пробирку. Наблюдать изменение цвета.
Задание 7 Рассмотрите схему
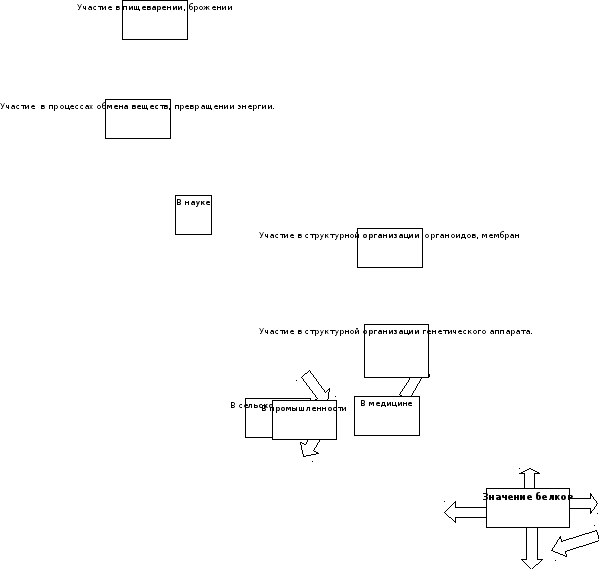
Ответьте на вопрос: Почему же Ф.Энгельс определил белки как основу жизни на Земле?
Приложение 4
Задача 1.
Известно, что для взрослого человека необходимо 1,5 г белка на 1 кг массы. Зная свою массу, определите норму необходимого потребления белка для своего организма.
Задача 2.
Известно, что при продолжительности жизни 70 лет обновление белка в организме происходит в среднем 200 раз. Зная свой возраст, предположите, сколько раз произошло обновление белка в вашем организме.
Приложение 5
Физико-химические свойства белков
Природные белковые вещества крайне разнообразны: некоторые белки – твердые вещества(кератины), не растворимые в воде и солевых растворах, большинство белков жидкие или студнеобразные вещества, растворимые в воде (например альбумин(белок куриного яйца).
Белки из растворов осаждаются концентрированными растворами аминокислотных солей и солей щелочных металлов. Если к раствору куриного белка прилить сульфата аммония – жидкость мутнеет и появляется осадок.
Добавление к раствору белка солей тяжелых металлов Нд, Рв, Си и т.д приводит к осаждению белка не растворяющегося в воде. Поэтому для организма крайне вредны пары тяжелых металлов и их солей. Осаждение белков происходит так же концентрированными кислотами НNО3, Н2SО4, формалином и фенолом, а также этиловым спиртом, при действии радиации, даже сильного встряхивания- когда мы сбиваем белок в гоголь-моголь. При слабом нагревании белки свертываются.
При простудных заболеваниях температура тела повышается выше 36,6. Как это отражается на состоянии нашего организма? Почему повышение температуры до 40 градусов очень опасно для человека. Почему у маленьких детей повышение температуры, считается более опасным, чем у взрослого человека?
Что же происходит при повышении температуры? Из курса физики 10-го класса мы знаем, что температура – величина, характеризующая интенсивность движения атомов. Температура прямо пропорциональна среднеквадратичной скорости атомов и среднекинетической энергии (Е = m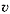 2/2 = 3/2kT). Поэтому повышение температуры (увеличение внутренней энергии движения) вызывает увеличение амплитуды колебаний атомов звеньев структуры. Следовательно, увеличивается расстояние между атомами, связываемыми водородной связью. При больших амплитудах колебаний водородная связь разрушается, при этом увеличивается нагрузка на соседние связи спиральной структуры, и в конечном итоге структура белка быстро распадается.
2/2 = 3/2kT). Поэтому повышение температуры (увеличение внутренней энергии движения) вызывает увеличение амплитуды колебаний атомов звеньев структуры. Следовательно, увеличивается расстояние между атомами, связываемыми водородной связью. При больших амплитудах колебаний водородная связь разрушается, при этом увеличивается нагрузка на соседние связи спиральной структуры, и в конечном итоге структура белка быстро распадается.
Поэтому при повышении температуры выше 40 градусов происходит процесс денатурации белка в организме человека, что приводит к изменению функций белка. Нарушение естественной, уникальной (свойственной только этому белку) структуры белковой молекулы называют денатурацией.
Денатурация может быть вызвана изменением температуры, обезвоживанием, облучением рентгеновскими лучами и другими воздействиями. Вначале разрушается самая слабая структура – четвертичная, затем третичная, вторичная и при наиболее жестких условиях – первичная.
Если при изменении условий среды первичная структура молекулы белка остаётся неизменной, то при восстановлении нормальных условий среды полностью восстанавливается и структура белка.
Процесс восстановления структуры белка называется ренатурацией.
Это свойство белков широко используется в медицинской и пищевой промышленности для приготовления медицинских препаратов, например вакцин и сывороток, для получения пищевых концентратов, сохраняющих в высушенном виде свои питательные функции.
Приложение 6
Задание 8 Проверь себя
Главными носителями жизни являются … .
… - это сложные высокомолекулярные соединения, построенные из … .
Молекулярная масса белков изменяется от … до … .
Многие белки растворимы в …, почти все растворяются в … .
Нерастворимы белки, из которых построены … .
В структуре белка различают … структуры.
Функции белков в организме … .
Критерии оценки:
«5» - все ответы правильные; «3» - 2-3 неверных ответа;
«4» - 1 неверный ответ; «2» - 4 и более неверных ответов.
Ответьте на вопросы и оцените свою работу на уроке
1. Каковы были Ваши цели перед занятием, и насколько их удалось реализовать?
2. Перечислите трудности, с которыми Вы столкнулись: а) при изучении темы (раздела); б) при ответе на открытые задания.
3.Каким образом Вы преодолевали трудности?
4.Каков главный результат для Вас лично при изучении темы?
5. Чему Вы научились лучше всего?
Приложение 7
Использованная литература:
1.Габриелян О.С. « Химия 10», Москва, Дрофа, 2009
2.Глинка Н.Л.Общая химия: учебное пособие/Н.Л.Глинка.-М.:КНОРУС,2011.-752с.
3.Габриелян О.С.Химия 10 класс: Настольная книга учителя/О.С.Габриелян, И.Г. Остроумов.-М.:Дрофа,2004.-480с.
4.ПономареваИ.Н.,КорниловаО.А.,ЧерноваН.М: учебник для учащихся 9 классов общеобразовательных учреждений/Под редакцией проф. И.Н.Пономаревой-М.:Вентана-Граф,2013-242с.
5. Единая коллекция цифровых образовательных ресурсов по химии
6.Интернет-ресурсы электронных учебников:
http://www.chemistry.ssu.samara.ru/ .
http://cnit.ssau.ru/organics/
9


















