
БҚО, Ақжайық ауданы,
Алғабас ауылы,
Алғабас ОЖББ мектебінің
химия пәнінің мұғалімі
Аманова Гүлбақша Ғинаятқызы

Үй тапсырмасын тексеру:
1. Алкендерден алкадиендердің айырмашылығы неде?
2. Диендер деп қандай көмірсутектерді атайды?
3. Диендерге қандай реакциялар тән? Мысал келтір.
4. Алкадиендерді ашқан кім?
5. Алкендерді қайда қолданамыз?
6. Каучукқа қандай физикалық қасиеттер тән?
7. Резеңкені каучуктан тәжірибе жүзінде қалай алуға болады?

«Қоқыс жәшігінен табылған жаңалық»
Қазіргі кезде кең қолданылатын кальций карбидін неміс химиигі Ф. Велер 1862 жылы кездейсоқ ашты. Ол қалай болды? Велер калцийді әктен көмір қатысында тотықсызданырып алмақшы болады. Нәтижесінде химик ешқандай металдық қасиеті жоқ қандай да бір күйген массаны алады. Өкінген Велер ол массаны қорадағы қоқысқа керексіз өнім ретінде лақтыра салады. Жаңбыр жауған кезде Велердің лаборанты өзі лақтырып тастаған тасты массадан газ бөлініп жатқанын байқады. Ол газ Велерді қызықтырды.
Сұрақ: Күйген масса қандай зат? Одан қандай газ бөлінді? Жауаптарынызды реакция теңдеулері арқылы дәлелдеңіз.

Жауабы: Талдау ол газдың 1836 жылы Э. Деви ашқан ацетилен екенін көрсетті. Осылайша кальций карбиді нің СаС 2 сумен әрекеттесіп, ацетилен бөлетін анықталып,ашылды:
СаО+3С→СаС 2 + СО
СаС 2 + 2Н 2 О→С 2 Н 2 ↑ + Са(ОН) 2
ацетилен

Сабақтың тақырыбы:
Алкиндер. Ацетилен .

Алкиндер. Ацетилен
Алкиндер – құрамында бір үш еселі байланысы бар жалпы формуласы С n H 2n-2 болатын қанықпаған көмірсутектер. Құрамында үш байланысы бар ең қарапайым көмірсутек – этин немесе ацетилен С 2 H 2 . Оның химиялық формуласын ұсынған – П. Бертло (1860 ж) Бірінші мүшесі ацетиленнен С 2 H 2 басталатындықтан, алкиндер ацетиленді көмірсутектері деп те аталады.

Ацетилен молекуласының моделі
Ацетилен молекуласындағы әр көміртек атомы бір сутек атомымен байланысады, өзара үш еселі байланыс арқылы жалғасады.
Ацетилен молекуласындағы екі көміртек атомының арасындағы үш байланыстың біреуі σ -, екеуі π - байланыстан тұрады.
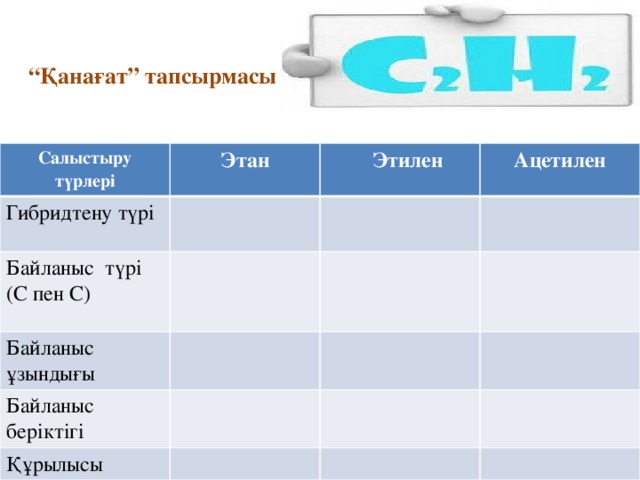
“ Қанағат” тапсырмасы
Салыстыру түрлері
Этан
Гибридтену түрі
Этилен
Байланыс түрі (C пен C)
Ацетилен
Байланыс ұзындығы
Байланыс беріктігі
Құрылысы
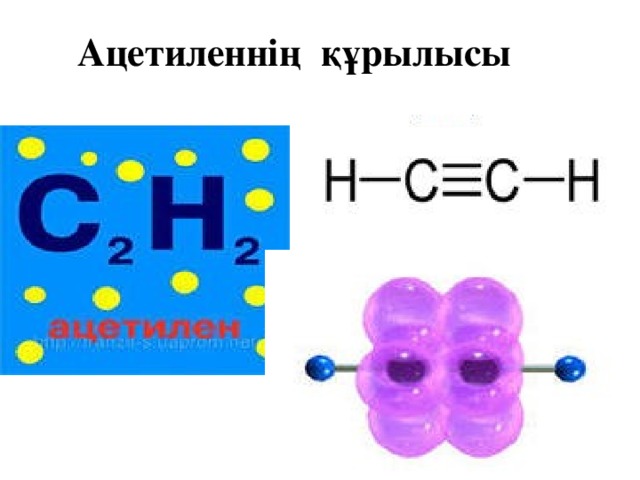
Ацетиленнің құрылысы
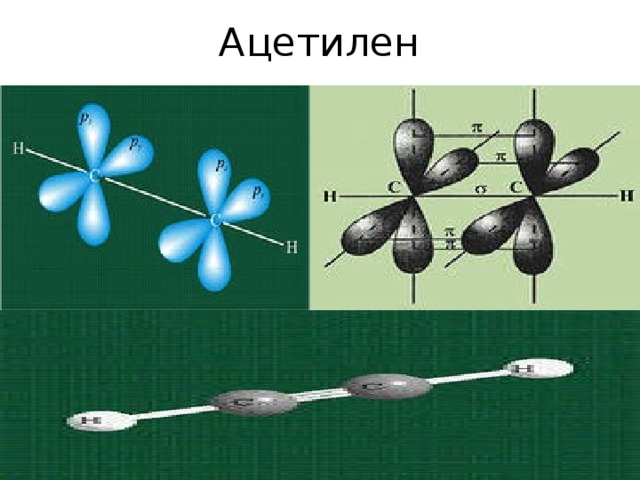
Ацетилен
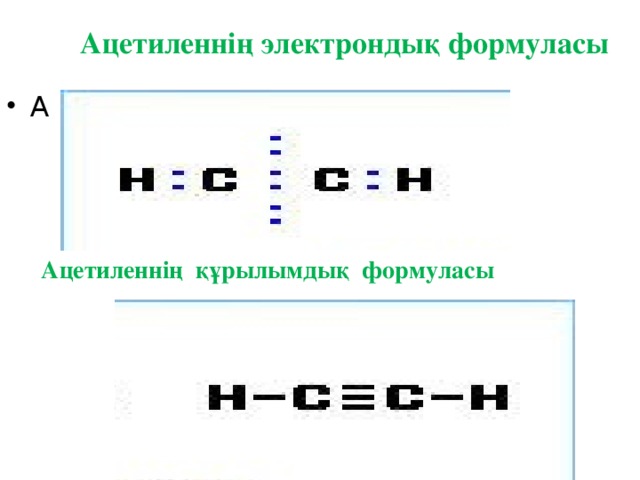
Ацетиленнің электрондық формуласы
Ацетиленнің құрылымдық формуласы

Ацетиленнің изомерлері
Көміртегі қаңқасы
Еселі байланыс орны
класаралық
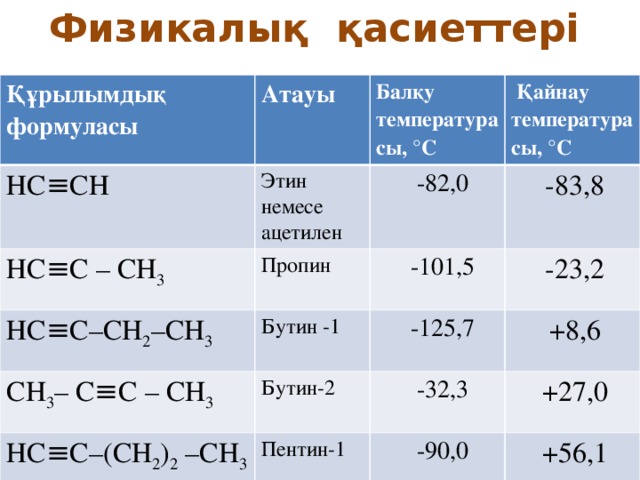
Физикалық қасиеттері
Құрылымдық формуласы
Атауы
НС≡СН
Балқу температура
Этин немесе ацетилен
НС≡С – CH 3
НС≡С – CH 2 – CH 3
сы, °С
Қайнау температура
-82,0
Пропин
CH 3 – С≡С – CH 3
Бутин -1
-101,5
-83,8
сы, °С
-23,2
-125,7
Бутин-2
НС≡С –( CH 2 ) 2 – CH 3
+8,6
-32,3
Пентин-1
+27,0
-90,0
+56,1
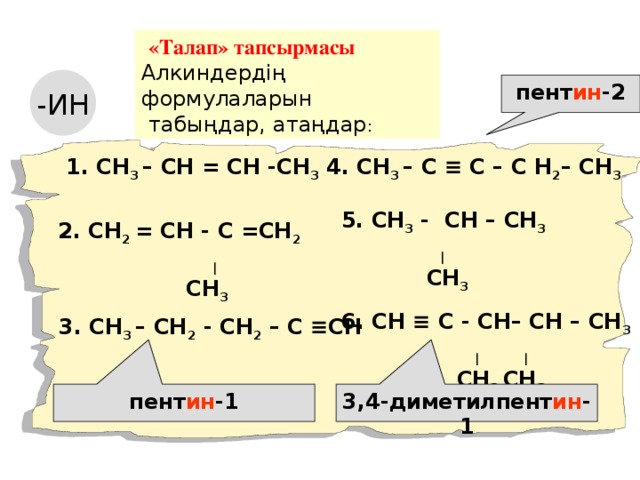
«Талап» тапсырмасы
Алкиндердің формулаларын
табыңдар, атаңдар :
-ИН
пент ин -2
4. СН 3 – С ≡ С – С Н 2 – СН 3
1. СН 3 – СН = СН -СН 3
5. СН 3 - СН – СН 3
∣
СН 3
2. СН 2 = СН - С =СН 2
∣
СН 3
6. СН ≡ С - СН– СН – СН 3
∣ ∣
СН 3 СН 3
3. СН 3 – СН 2 - СН 2 – С ≡СН
3,4-диметилпент ин -1
пент ин -1

Ацетиленді (алкиндерді) алу
№
Алыну әдістері
1.
Тиісті реакция теңдеулері
Алкандарды дегидрлеп алады
2.
3.
CH 3 – CH 3 → 2H 2 + CH≡ CH
Табиғи газдан алады. м:метаннан
4.
2CH 4 → 3H 2 + CH≡ CH
Кальций карбидінен
CаС 2 + H 2 O → Ca(OH) 2 + С 2 H 2 ↑
Галогентуынды-
лардан
CH 3 – CHCІ – CH 2 CІ + 2КОH → CH 3 – С≡СН + 2КСІ + 2 H 2 O
![Ацетиленнің тотығу реакциялары 1.Ацетиленге оттегі жіберсе, толық жанады. 2C 2 Н 2 + 5 О 2 → 4CO 2 + 2 Н 2 О Өте көп жылу бөлінеді, t-сы 3000°С 2. Қосымша жағдайлар жасалмаса, күйелі жалынмен жанады: C 2 Н 2 + О 2 → C + CO + Н 2 О 3. Ацетиленді КМnO 4 ерітіндісі арқылы өткізсе, ерітінді түссізденеді. Бұл реакция еселі байланыстардың сапалық реакциясы: НС≡СН + 4[ О] → HOOC – CO O Н қымыздық қышқылы](https://fsd.kopilkaurokov.ru/uploads/user_file_551b6e7b31cee/img_user_file_551b6e7b31cee_0_15.jpg)
Ацетиленнің тотығу реакциялары
1.Ацетиленге оттегі жіберсе, толық жанады.
2C 2 Н 2 + 5 О 2 → 4CO 2 + 2 Н 2 О
Өте көп жылу бөлінеді, t-сы 3000°С
2. Қосымша жағдайлар жасалмаса, күйелі жалынмен жанады:
C 2 Н 2 + О 2 → C + CO + Н 2 О
3. Ацетиленді КМnO 4 ерітіндісі арқылы өткізсе, ерітінді түссізденеді. Бұл реакция еселі байланыстардың сапалық реакциясы:
НС≡СН + 4[ О] → HOOC – CO O Н
қымыздық қышқылы

Ацетиленнің қосылу реакциялары
- 1. Гидрленуі. Ni, Pt, Pd өршіткі қатысында жүреді:
А. НС≡СН + Н 2 → Н 2 С = C Н 2 этилен
B. Н 2 С = C Н 2 + Н 2 → Н 3 С – C Н 3 этан
- 2. Галогенденуі. Галогендермен әрекеттесуі сатылап жүреді. Броммен әрекеттесуі сапалық реакциясы.
А. НС≡СН + Br 2 → BrН С = C НBr 1,2-дибромэтен
B. BrН С = C НBr + Br 2 → Br 2 HC – C НBr 2
1,1,2,2- тетрабромэтан
- 3. Галогенсутектерді қосып алуы .
НС≡СН + НСІ → Н 2 С = C НСІ винилхлорид
![Орынбасу реакциялары Үш байланыс шеткі С атомында орналасқан алкиндер “қышқылдық” қасиет көрсетіп, сутек атомдары металл атомдарына алмасады. НС≡СН + Ag 2 O → Ag С ≡ C Ag + H 2 O күміс ацетилениді түзіледі. Реакцияның толық теңдеуі: НС≡СН + 2[Ag(NH 3 ) 2 ]OH → Ag С ≡ C Ag + 4NH 3 +2H 2 O Алкиндерде sp -гибридтелген көміртек атомдарының электртерістілігі жоғары болғандықтан, – С ≡С← Н байланыстың полюстігі үлкен болады да, электрон тығыздығы С-ке қарай ығысып, Н атомы орынбасу реакциясына түсе алады.](https://fsd.kopilkaurokov.ru/uploads/user_file_551b6e7b31cee/img_user_file_551b6e7b31cee_0_17.jpg)
Орынбасу реакциялары
Үш байланыс шеткі С атомында орналасқан алкиндер “қышқылдық” қасиет көрсетіп, сутек атомдары металл атомдарына алмасады.
НС≡СН + Ag 2 O → Ag С ≡ C Ag + H 2 O
күміс ацетилениді түзіледі.
Реакцияның толық теңдеуі:
НС≡СН + 2[Ag(NH 3 ) 2 ]OH →
Ag С ≡ C Ag + 4NH 3 +2H 2 O
Алкиндерде sp -гибридтелген көміртек атомдарының электртерістілігі жоғары болғандықтан, – С ≡С← Н байланыстың полюстігі үлкен болады да, электрон тығыздығы С-ке қарай ығысып, Н атомы орынбасу реакциясына түсе алады.
![Гидратация реакциясын зерттеуші, ғалым Гидратация реакциясы сынап (II) сульфатының қатысында жүреді. Оны 1881 жылы М.Г.Кучеров ашқан. Өнеркәсіпте осы жолмен алынады. Аралық тұрақсыз өнім – винил спирті түзіліп, ол изомерленіп, ацетальдегидке айналады: НС≡СН + H – OH→ [H 2 С = C H – OH] → H 2 C – C= O | H М.Г. Кучеров – ұлы орыс халқының органик-химигі. Органикалық заттарды синтездеуде көп еңбек сіңірді. Михаил Григорьевич Кучеров 3.06.1850 – 26.06.1911](https://fsd.kopilkaurokov.ru/uploads/user_file_551b6e7b31cee/img_user_file_551b6e7b31cee_0_18.jpg)
Гидратация реакциясын зерттеуші, ғалым
Гидратация реакциясы сынап (II) сульфатының қатысында жүреді. Оны 1881 жылы М.Г.Кучеров ашқан. Өнеркәсіпте осы жолмен алынады. Аралық тұрақсыз өнім – винил спирті түзіліп, ол изомерленіп, ацетальдегидке айналады:
НС≡СН + H – OH→
[H 2 С = C H – OH] → H 2 C – C= O
|
H
М.Г. Кучеров – ұлы орыс халқының органик-химигі. Органикалық заттарды синтездеуде көп еңбек сіңірді.
Михаил Григорьевич Кучеров
3.06.1850 – 26.06.1911

Марковников ережесі
Марковников ережесі бойынша сутек атомы сутек атомы көбірек көміртек атомына, ал галоген атомы сутек атомы азырақ көміртек атомына қарай тартылады.
В.В. Марковников – орыс органик-химигі. Ол еңбектерін мұнай химиясына, органикалық синтезге арнады. Нафтендерді зерттеді.
Владимир Васильевич
Марковников

“ Терең ой” тапсырмасы
- Құрамында 25% қосасы бар 500 кг калций карбидінен ацетиленнің қандай көлемін (қ.ж.) алуға болатынын есептеңдер.
2. Көлемі 11,2 л (қ.ж.) ацетиленді толық жағу үшін ауаның қандай көлемі қажет болатынын есептеп табыңдар

Ацетиленнің қолданылуы
Ацетилен жанғанда өте көп мөлшерде жылу бөлінетіндіктен, металдарды кесу және дәнекерлеу үшін қолданылады. Өнеркәсіпте ацетиленнен сірке қышқылы, синтетикалық көксағыз, пластмассалар, еріткіштер, т.б. алынады.

Қорытындылау
Алкиндер – молекула құрамындағы көміртек атомдары өзара үш байланыс арқылы жалғасқан қанықпаған көмірсутектер. Олардың ең қарапайым өкілі – ацетилен. Алкиндер табиғатта кездеспейді, оларды алкандардан, кальций карбидінен алады.

Үйге тапсырма: §4.5. §4.5. 106-114 бет. №6-10 жаттығулар.

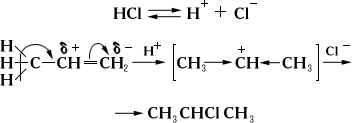















![Ацетиленнің тотығу реакциялары 1.Ацетиленге оттегі жіберсе, толық жанады. 2C 2 Н 2 + 5 О 2 → 4CO 2 + 2 Н 2 О Өте көп жылу бөлінеді, t-сы 3000°С 2. Қосымша жағдайлар жасалмаса, күйелі жалынмен жанады: C 2 Н 2 + О 2 → C + CO + Н 2 О 3. Ацетиленді КМnO 4 ерітіндісі арқылы өткізсе, ерітінді түссізденеді. Бұл реакция еселі байланыстардың сапалық реакциясы: НС≡СН + 4[ О] → HOOC – CO O Н қымыздық қышқылы](https://fsd.kopilkaurokov.ru/uploads/user_file_551b6e7b31cee/img_user_file_551b6e7b31cee_0_15.jpg)

![Орынбасу реакциялары Үш байланыс шеткі С атомында орналасқан алкиндер “қышқылдық” қасиет көрсетіп, сутек атомдары металл атомдарына алмасады. НС≡СН + Ag 2 O → Ag С ≡ C Ag + H 2 O күміс ацетилениді түзіледі. Реакцияның толық теңдеуі: НС≡СН + 2[Ag(NH 3 ) 2 ]OH → Ag С ≡ C Ag + 4NH 3 +2H 2 O Алкиндерде sp -гибридтелген көміртек атомдарының электртерістілігі жоғары болғандықтан, – С ≡С← Н байланыстың полюстігі үлкен болады да, электрон тығыздығы С-ке қарай ығысып, Н атомы орынбасу реакциясына түсе алады.](https://fsd.kopilkaurokov.ru/uploads/user_file_551b6e7b31cee/img_user_file_551b6e7b31cee_0_17.jpg)
![Гидратация реакциясын зерттеуші, ғалым Гидратация реакциясы сынап (II) сульфатының қатысында жүреді. Оны 1881 жылы М.Г.Кучеров ашқан. Өнеркәсіпте осы жолмен алынады. Аралық тұрақсыз өнім – винил спирті түзіліп, ол изомерленіп, ацетальдегидке айналады: НС≡СН + H – OH→ [H 2 С = C H – OH] → H 2 C – C= O | H М.Г. Кучеров – ұлы орыс халқының органик-химигі. Органикалық заттарды синтездеуде көп еңбек сіңірді. Михаил Григорьевич Кучеров 3.06.1850 – 26.06.1911](https://fsd.kopilkaurokov.ru/uploads/user_file_551b6e7b31cee/img_user_file_551b6e7b31cee_0_18.jpg)





















