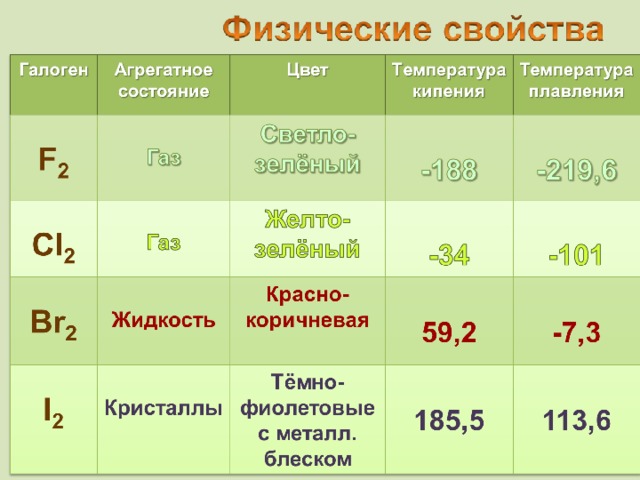
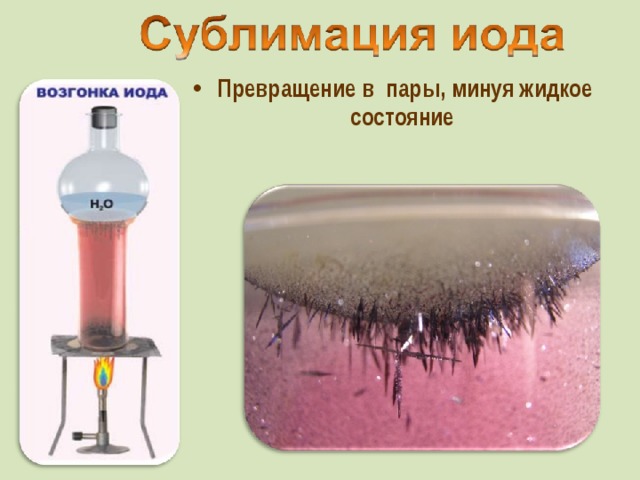
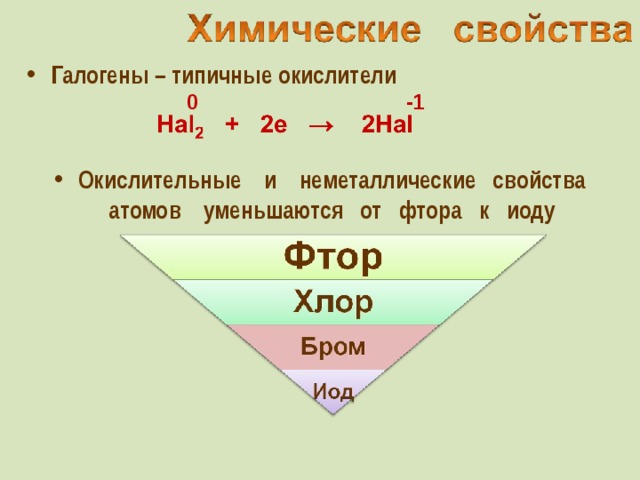
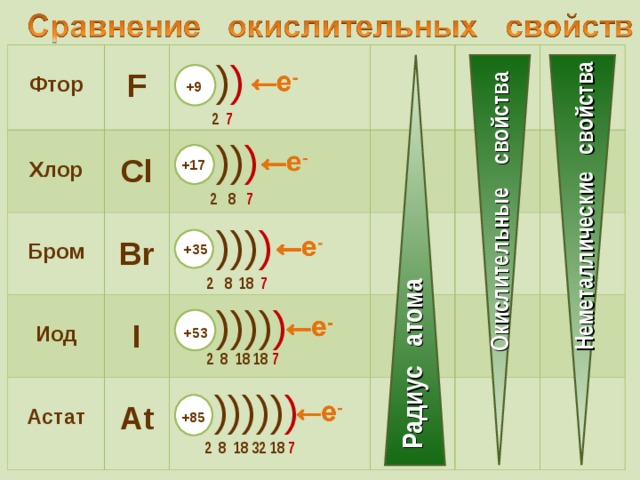
ПРЕЗЕНТАЦИЯ СОДЕРЖИТ МАТЕРИАЛ О НАХОЖДЕНИИ В ПРИРОДЕ, ФИЗИЧЕСКИХ И ХИМИЧЕСКИХ СВОЙСТВАХ, СПОСОБАХ ПОЛУЧЕНИЯ, КАЧЕСТВЕННЫХ РЕАКЦИЯХ ГАЛОГЕНОВ, А ТАКЖЕ УПРАЖНЕНИЯ ДЛЯ ЗАКРЕПЛЕНИЯ МАТЕРИАЛА.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
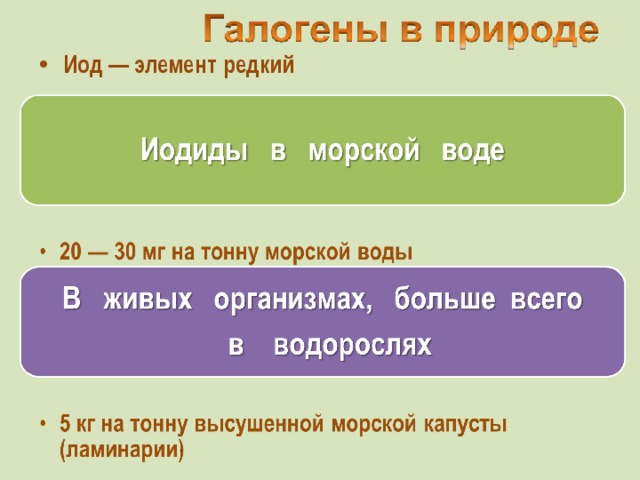
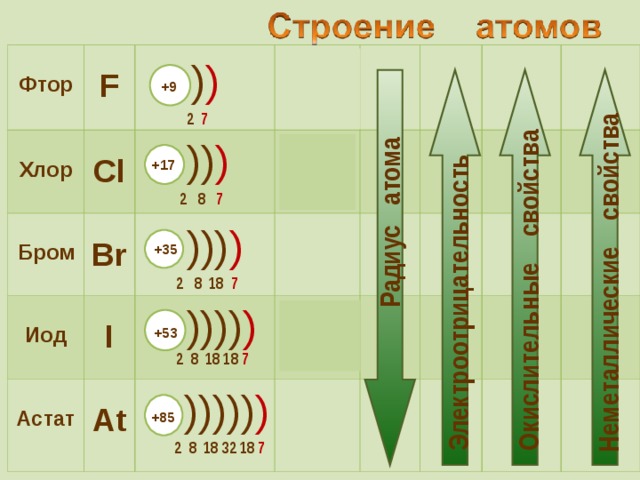
Презентация по химии на тему "галогены" 9 класс
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Презентация по химии на тему "галогены" 9 класс»
Похожие файлы
Полезное для учителя
Распродажа видеоуроков!
1660 руб.
2760 руб.
1660 руб.
2760 руб.
1520 руб.
2530 руб.
1880 руб.
3140 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства