Использование презентации на уроке есть применение наглядного метода иллюстраций во взаимосвязи с другими методами, позволяющими развивать мышление учащихся и активизировать их познавательную деятельность. Иллюстрации особенно необходимы тогда, когда объекты не доступны непосредственному наблюдению, а слово учителя оказывается недостаточным, чтобы дать представление об изучаемом объекте или явлении. Информация, размещенная на слайде и появляющаяся в нужные моменты объяснения, проведения опытов, экспериментов, доказательств и т.д. заставляет учащихся пройти через все этапы мышления, использовать различные мыслительные операции. По сравнению с традиционной формой ведения урока, заставляющей учителя постоянно обращаться к мелу и доске, использование таких презентаций высвобождает большое количество времени, которое можно употребить для дополнительного объяснения материала.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
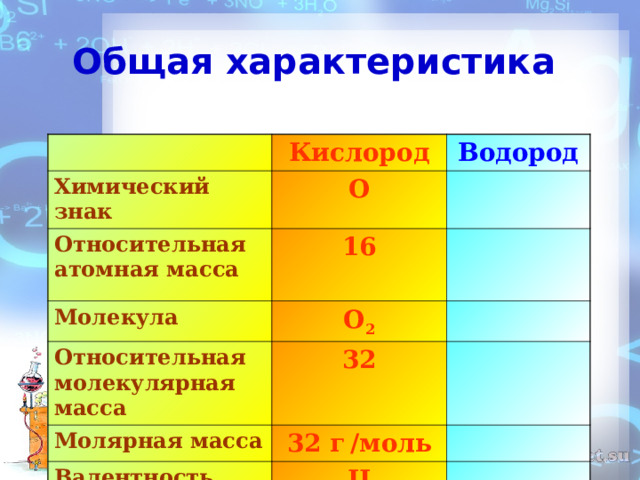
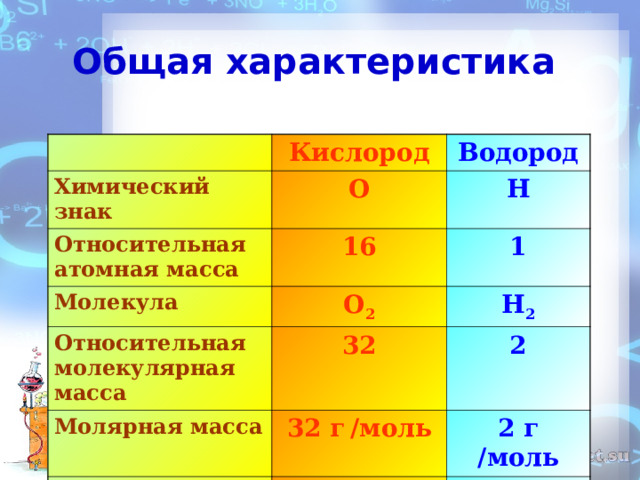
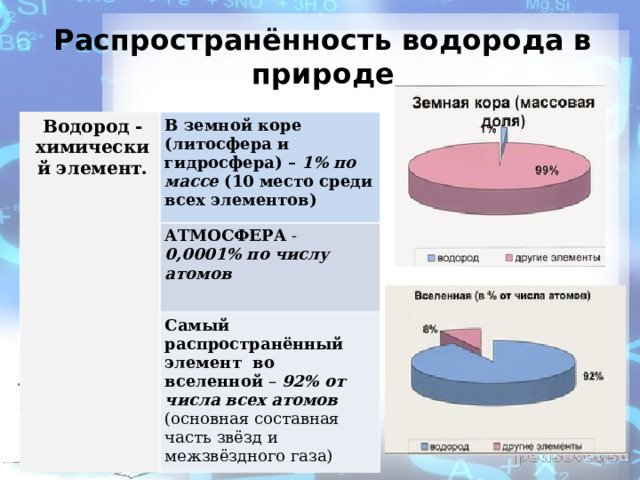
Презентация по теме "Водород - общая характеристика, нахождение в природе, получение"
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Презентация по теме "Водород - общая характеристика, нахождение в природе, получение"»
Полезное для учителя
Распродажа видеоуроков!
1700 руб.
2840 руб.
1660 руб.
2760 руб.
1660 руб.
2760 руб.
1700 руб.
2840 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства