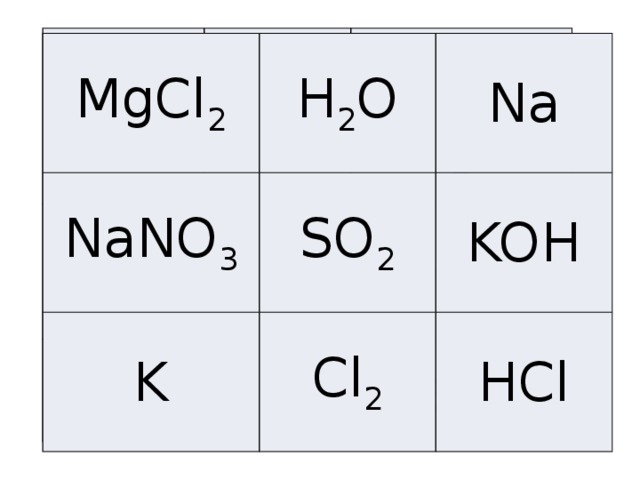
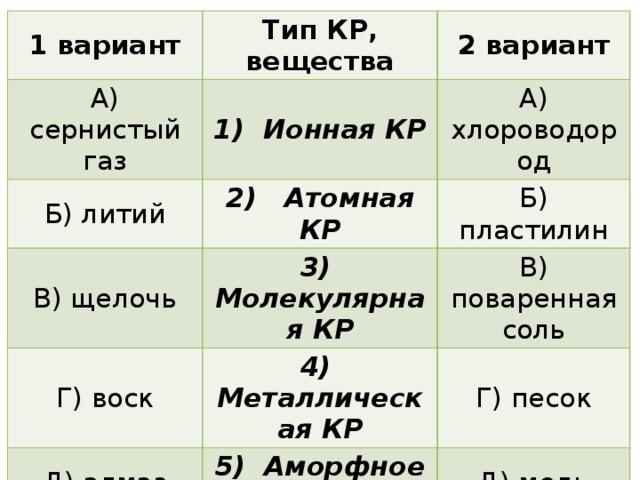
Мультимедийная презентация к уроку по теме «Кристаллические решетки» по программе О.С. Габриеляна «Химия-8» (§ 22). Предлагаются элементы фронтального опроса для повторения пройденного ранее материала. Для закрепления знаний введена игра на распознавание типов кристаллических решеток.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
Кристаллические решетки
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Кристаллические решетки »
Полезное для учителя
Распродажа видеоуроков!
1930 руб.
2760 руб.
1930 руб.
2760 руб.
1930 руб.
2760 руб.
2200 руб.
3140 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства