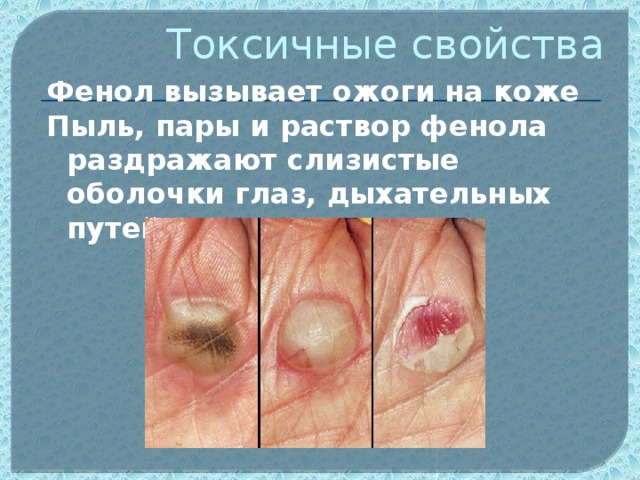
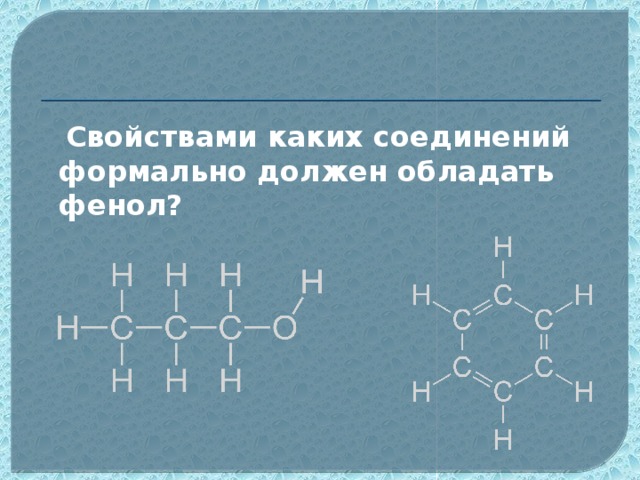
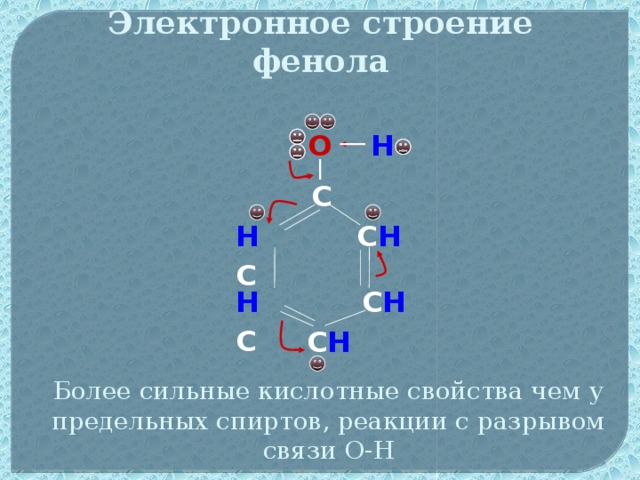
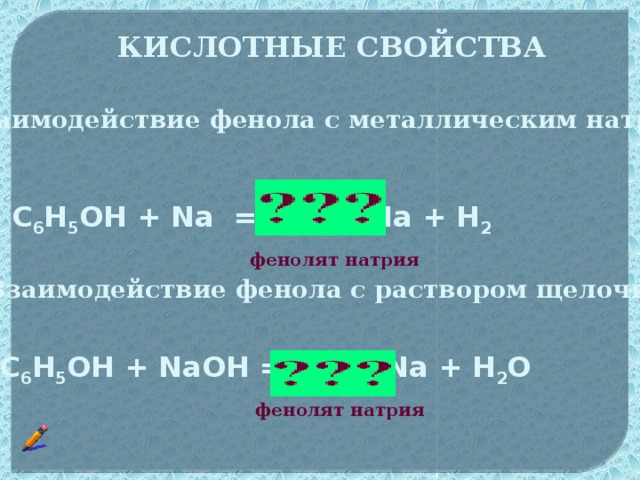
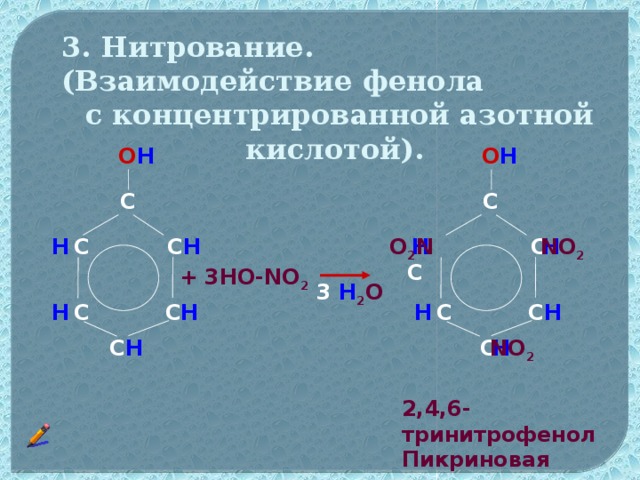
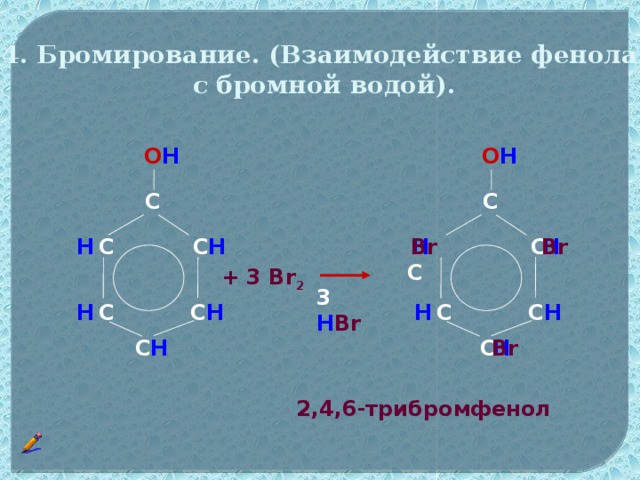
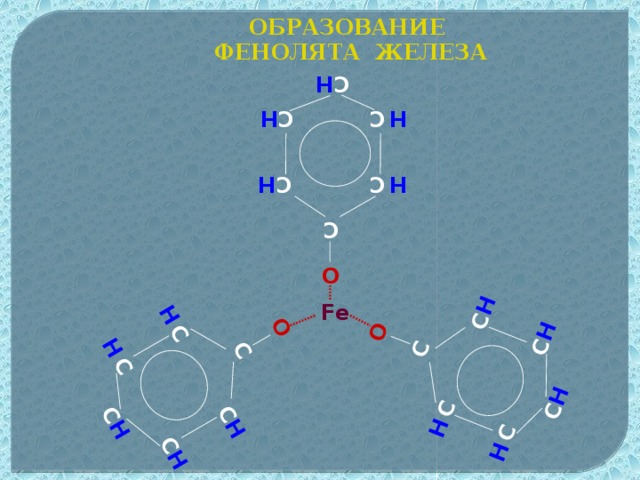
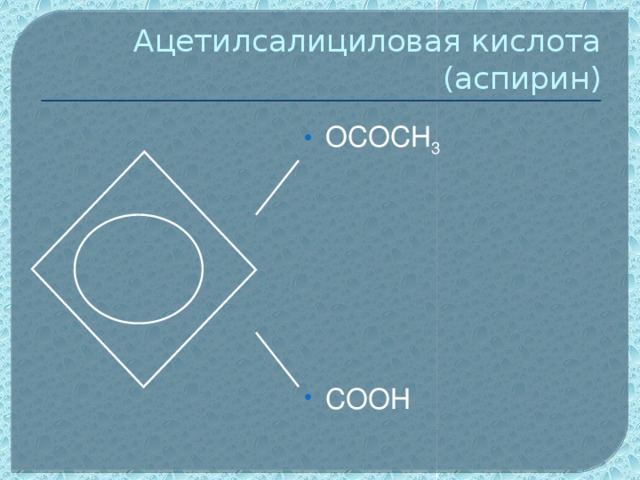
Данная презентация может быть использована при изучении органического вещества фенол в 10 классе. В данном материале отражены следующие методические приёмы,которые может использовать учитель на уроке: метапредметный подход, проблемное изучение материала, экспериментальная часть,а также тестирование для осуществлении рефлексии. На основе этих методик учитель,используя анимационные фрагменты урока, поможет учащимся самим сформулировать строение данного вещества,а также предсказать свойства фенола. В презентации предусмотрено также подтверждение доказательства третьего положения теории химического строения Александра Михайловича Бутлерова о взаимном влиянии атомомов и групп атомов в молекулах органических веществ.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
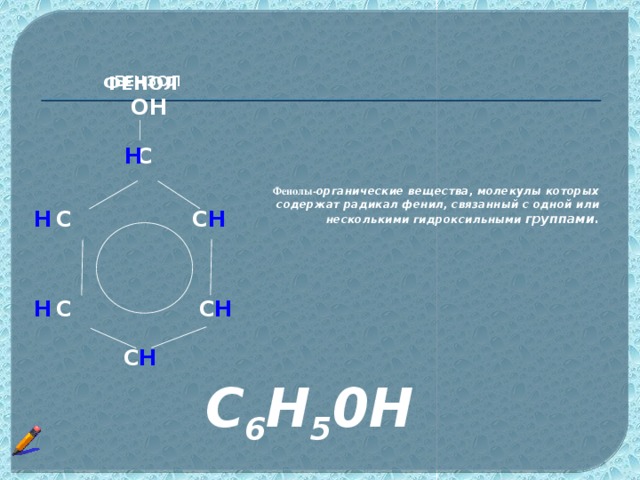
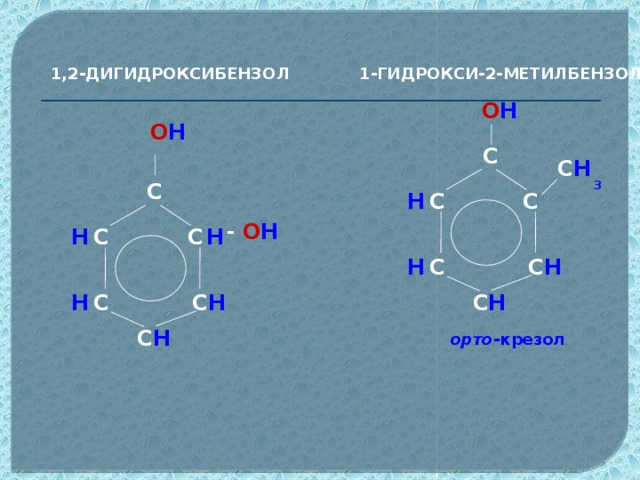
Фенол
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Фенол»
Полезное для учителя
Распродажа видеоуроков!
1660 руб.
2760 руб.
1660 руб.
2760 руб.
1520 руб.
2530 руб.
1690 руб.
2820 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства