Муниципальное казенное общеобразовательное учреждение
Хлебородненская средняя общеобразовательная школа

Автор: учитель физики
Бакотин Роман Владимирович
с. Хлебородное, 2014
Цель урока: изучить строение атома.
Задачи урока:
Образовательные:
Развивающие:
Отработать навыки определения состава атома, состава ядра атома по периодической системе химических элементов.
Продолжить развитие навыков работы с опорным конспектом, таблицами и схемами.
Развивать интеллектуальные и творческие способности учащихся.
Воспитательные:
Тип урока: урок изучения нового материала.
Ход урока.
Организационный момент.
Фронтальный опрос.
Какие агрегатные свойства вещества вы знаете?
Что такое молекула?
Какие ещё существуют частицы?
Приведите примеры известных вам молекул.
Как на основе знаний о мельчайших частицах можно объяснить переходы вещества из одного состояния в другое?
Изучение нового материала.
Итак, мы сказали, что самой маленькой частицей вещества является атом. Мы также знаем, что при делении заряда остаётся наименьшая заряженная порция, которую назвали электрон. Следовательно, возникает вопрос: есть ли другие мельчайшие частицы и какова структура атома?
Узнать структуру атома пытались многие учёные, одним из которых был английский физик Томсон.
(Ученик рассказывает биографию Томсона – Приложение 1)
По мысли Томсона, положительный заряд атома занимает весь объем атома и распределен в этом объеме с постоянной плотностью. Простейший атом – атом водорода - представляет собой положительно заряженный шар радиусом около 10-8 см, внутри которого находится электрон. У более сложных атомов в положительно заряженном шаре находится несколько электронов, так что атом подобен кексу, в котором роль изюминок играют электроны.
Однако модель атома Томсона оказалась в полном противоречии с опытами по исследованию распределения положительного заряда в атоме. Эти опыты, произведенные впервые Резерфордом, сыграли решающую роль в понимании строения атома.
(Демонстрация батона с изюмом)
(Запись в тетрадь)
Положительный заряд атома занимает весь объём атома и распределён по его объёму с постоянной плотностью.
(Ученик рассказывает биографию Э. Резерфорда – Приложение 2)
Опыт Резерфорда.
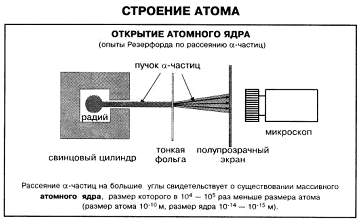
Радиактивный препарат, например радий, помещался внутри свинцового цилиндра, вдоль которого был высверлен узкий канал. Пучок альфа-частиц из канала падал на тонкую фольгу из исследуемого материала (золото, медь и пр). После рассеяния альфа частицы попадали на полупрозрачный экран, покрытый сульфидом цинка. Столкновение каждой частицы с экраном сопровождалось вспышкой света, которую можно было наблюдать в микроскоп. Весь прибор размещался в сосуде, из которого был откачан воздух.
При хорошем вакууме внутри прибора в отсутствии фольги на экране возникал светлый кружок, состоящий из сцинтилляций, вызванных тонким пучком альфа частиц. Но когда на пути пучка помещали фольгу, альфа частицы из-за рассеяния распределялись на экране по кружку большей площади.
Модифицируя экспериментальную установку, Резерфорд пытался обнаружить отклонение альфа частиц на большие углы. Совершенно неожиданно оказалось, что небольшое число альфа частиц (примерно одна из двух тысяч) отклонилось на углы, большие 90 градусов.
Определение размеров атомного ядра.
Резерфорд понял, что альфа частица могла быть отброшена назад лишь в том случае, если положительный заряд атома и его масса сконцентрированы в очень малой области пространства. Так Резерфорд пришёл к идее атомного ядра тела малых размеров, в котором сконцентрированы почти вся масса и весь положительный заряд атома.
(Запись в тетрадь)
Ядро имеет малый размер, в котором сосредоточена почти вся масса и весь положительный заряд.
Работа с физическим словарём.
Найти следующие физические понятия:
Сцинтилляция
Альфа частица
Строение атома.
Строение атома имеет следующую структуру:
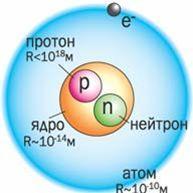
Работа в группах.
Задание для 1 группы: из цветной бумаги сделать модель атома.
Задание для 2 группы: сделать модель солнечной системы.
(После выполнения заданий, работы каждой группы сравниваются, делаются выводы).
Повторение изученного материала.
Разгадаем кроссворд.
3 Э
Л
Е
4 П
К
Н
2 Г
Р
Т
Р
Е
З
Е
Д
Р
О
Ф
Р
Й
Л
Т
О
Р
И
О
Н
О
Й
Н
Н
Нейтрально заряженная частица.
Альфа частица.
Отрицательно заряженная частица.
Положительно заряженная частица.
Учёный, предложивший планетарную модель атома.
Ответьте на вопросы:
Назовите две модели строения атома.
Что можно сказать о массе атома и массе ядра?
Домашнее задание.
Ответить на вопросы параграфа о строении атома. Подготовить сообщение по теме «Электронный микроскоп».
Подведение итогов.





















