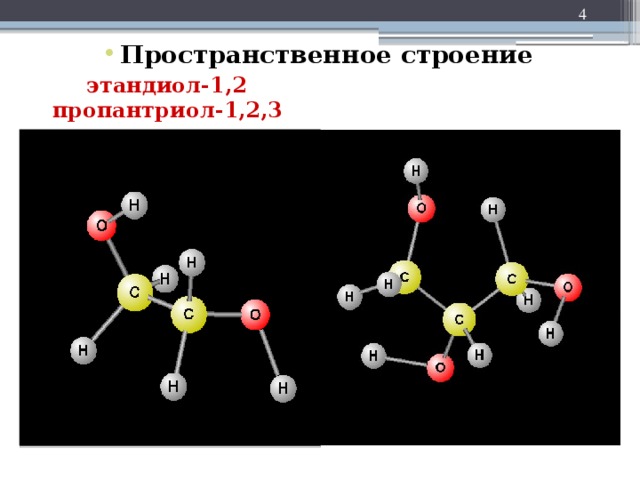
Организационный этап. Взаимное приветствие учеников и учителя, фиксация отсутствующих, проверка готовности к уроку. Актуализация знаний учащихся. Вопросы по изученному материалу: -Что является функциональной группой спиртов? (ОН-группа). -Какой признак лежит в основе классификации спиртов? (Число ОН-групп: одноатомные спирты—одна ОН-группа, двухатомные —две ОН-группы, трехатомные—три ОН-группы. ОН-группы должны находиться при разных атомах углерода). -Как называются первые представители многоатомных спиртов по систематической и тривиальной номенклатуре? (Этандиол-1,2—этиленгликоль, пропантриол-1,2,3—глицерин). Мотивация и целеполагание. Зная состав и строение многоатомных спиртов, попытаемся предположить, а затем и подтвердить на основе эксперимента физические и химические свойства этих веществ. Тема урока: «Многоатомные спирты». Цель урока: Раскрытие взаимосвязи строения и свойств веществ на примере многоатомных спиртов, как одного из положений теории химического строения А.М.Бутлерова.
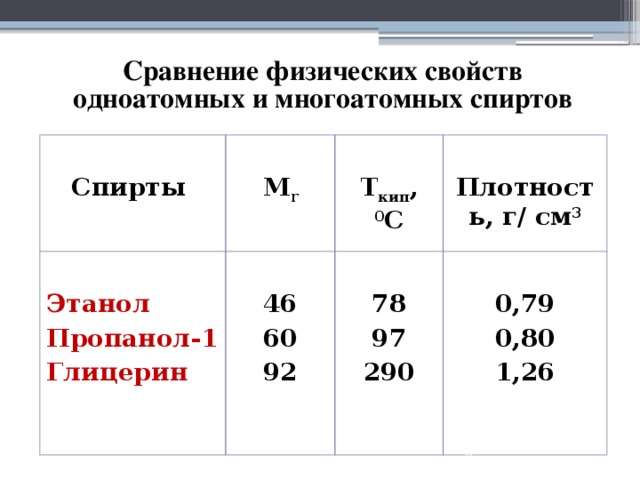
Изучение нового материала. 4.1 Физические свойства многоатомных спиртов. Сравнение физических свойств многоатомных и одноатомных спиртов. (В молекуле глицерина имеется 3 ОН-группы, значит число атомов водорода, способных к образованию водородной связи, в 3 раза больше, чем в молекулах одноатомных спиртов. Поэтому сила межмолекулярной связи в молекулах глицерина гораздо больше. В случае глицерина нужна более высокая температура для того, чтобы ослабить связи между молекулами до такой степени, чтобы они перешли в газообразное состояние. По этой причине многоатомные спирты более вязкие и температуры их кипения выше, чем у соответствующих одноатомных спиртов).
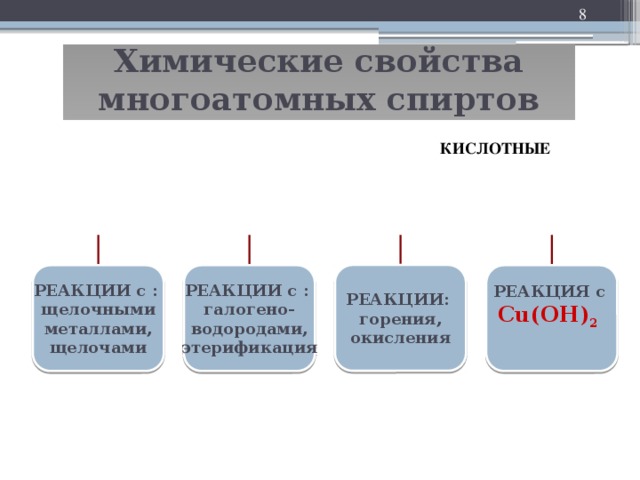
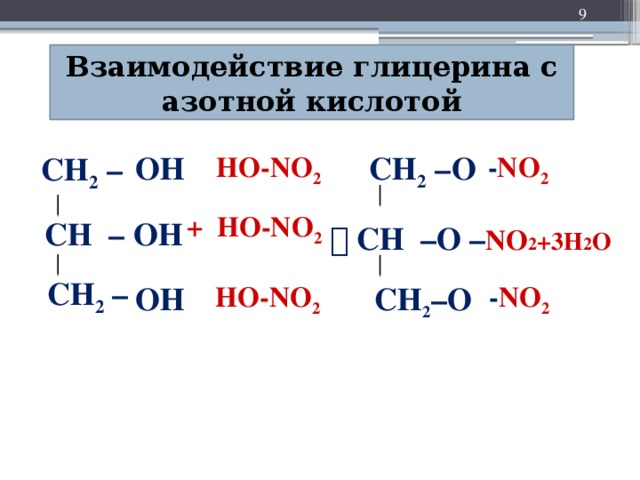
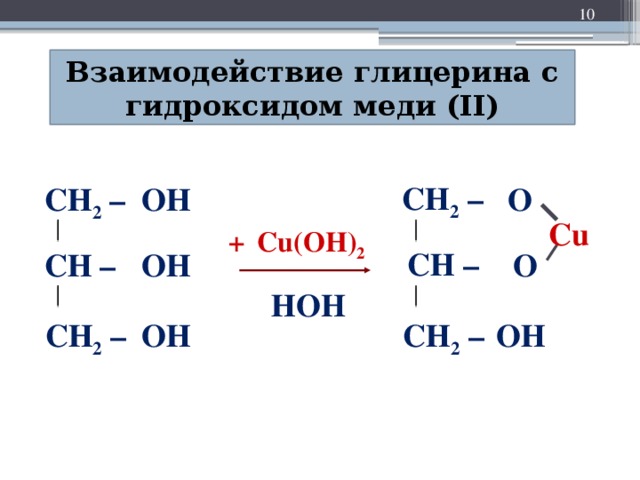
Химические свойства многоатомных спиртов. а) Изучение общих свойств, характерных для спиртов с помощью слайда 7. б) Взаимодействие глицерина с азотной кислотой рассматривается на слайде 8 (уравнение реакции записывается в тетрадь). в) Перед учащимися ставится вопрос: влияет ли количество ОН-групп на химические свойства спиртов? Ответ помогает найти реакция взаимодействия глицерина с гидроксидом меди (II). Реакция многоатомных спиртов с гидроксидом меди (II) доказывает наличие у них более выраженных кислотных свойств, что объясняется большей подвижностью атомов водорода в ОН-группах. Данная реакция считается качественной на многоатомные спирты. С помощью слайда 9 разбирается уравнение реакции и записывается в тетрадь (сокращенная запись уравнения)
Получение многоатомных спиртов. а) Подобно одноатомным спиртам, многоатомные спирты могут быть получены из соответствующих углеводородов через их галогенопроизводные. б) Диолы и триолы можно получить при окислении алкенов. в) Глицерин получают расщеплением жиров или синтетическим способом из пропилена, образуещегося при крекинге нефтепродуктов.
4.4 Применение глицерина и этиленгликоля. Вопрос разбирается с помощью слайдов 10-11. На слайде 12 используется таблица, в которой заполнена только графа «Области применения многоатомных спиртов». Контроль знаний по изученной теме в форме тестирования (тест содержится в приложении к проекту)
Выводы по уроку. На уроке были изучены физические и химические свойства многоатомных спиртов, рассмотрены вопросы получения и обсуждены области применения важнейших веществ данного класса: глицерина и этиленгликоля. Особое внимание было уделено взаимосвязи понятий «строение» и «свойства» веществ, как одного из положений теории химического строения А.М.Бутлерова. Теоретические предположения нашли подтверждение в эксперименте.
|
Настраивает учащихся на работу.
Обеспечивает актуализацию элементов знаний, необходимых для изучения новой темы.
В качестве мотивации использует эпиграф: Кто хочет съесть ядро ореха, Должен расколоть его скорлупу. Плавт Поясняет цель урока, называет задачи урока.
Предлагает познакомиться с внешним видом и растворимостью в воде глицерина и этиленгликоля. Показывая слайд 5, обращает внимание на различие в физических свойствах многоатомных и одноатомных спиртов. Подводит учащихся к самостоятельному выводу.
Предлагает предположить химические свойства многоатомных спиртов по аналогии с одноатомными. Обращает внимание на взаимодействие глицерина с азотной кислотой с образованием нитроглицерина.
Разъясняет условия проведения реакции глицерина с гидроксидом меди (II). На доске учитель записывает и разъясняет полное уравнение этой реакции.
Знакомит учащихся с важнейшими областями применения этиленгликоля и глицерина.
Учащимся предлагается ответить на вопросы рефлексии («да», «нет»): а) Интересной ли тебе показлась тема урока? б) Все ли сделанные на уроке выводы осознаны тобой до конца? в) Все ли уравнения реакций ты смог написать самостоятельно? |
Настраиваются на работу.
Повторяют изученный материал для лучшего усвоения новой темы. Правильность ответов проверяют с помощью слайдов 1-3
Записывают тему урока. Вникают в цель урока и убеждаются в значимости и необходимости изучения темы.
Проводят лабораторные опыты. Соотносят свои наблюдения с материалом слайдов 4-5.
Формулируют вывод (записывают в тетрадь): Большее число ОН-групп обуславливают некоторые особенности физических свойств многоатомных спиртов, что объясняется образованием водородных связей.
Высказываются реакции: горения , замещении водорода в ОН-группе на щелочной металл, обмен ОН-группы на галоген. Предполагается реакция этерификации.
Проводят лабораторный опыт. Наблюдают образование темно-синего раствора.
Уравнения реакций учащиеся записывают самостоятельно (1-ая часть домашнего задания).
Графа «Свойство спирта, на котором основано применение» заполняется учащимися самостоятельно (2-ая часть домашнего задания).
Результаты рефлексии (по ответу «да») а) 85%
б) 76,8%
в) 65,3%
|