Местоположение кремния в ПСХЭ Д.И. Менделеева, его валентные состояние, химические свойства.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
Кремний и его соединения.
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Кремний и его соединения.»
Полезное для учителя
Распродажа видеоуроков!
1690 руб.
2820 руб.
1880 руб.
3140 руб.
1880 руб.
3140 руб.
1660 руб.
2760 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства






![Химические свойства кремния Типичный неметалл, инертен. Как восстановитель: 1) С кислородом Si 0 + O 2 t˚ → Si +4 O 2 2) С фтором (без нагревания) Si 0 + 2F 2 → SiF 4 3) С углеродом Si 0 + C t˚ → Si +4 C (SiC - карборунд - твёрдый; используется для точки и шлифовки) 4) С водородом не взаимодействует. Силан (SiH 4 ) получают разложением силицидов металлов кислотой: Mg 2 Si + 2H 2 SO 4 → SiH 4 + 2MgSO 4 5) С кислотами не реагирует (только с плавиковой кислотой Si+4HF=SiF 4 +2H 2 Растворяется только в смеси азотной и плавиковой кислот: 3Si + 4HNO 3 + 18HF → 3H 2 [SiF 6 ] + 4NO + 8H 2 O 6) Со щелочами (при нагревании): Si 0 + 2NaOH + H 2 O t ˚ → Na 2 Si +4 O 3 + 2H 2 Как окислитель: 7) С металлами (образуются силициды): Si 0 + 2Mg t˚ → Mg 2 Si -4](https://fsd.kopilkaurokov.ru/up/html/2026/03/13/k_69b3b052da20b/img_user_file_69b3b054b51ce_6.jpg)

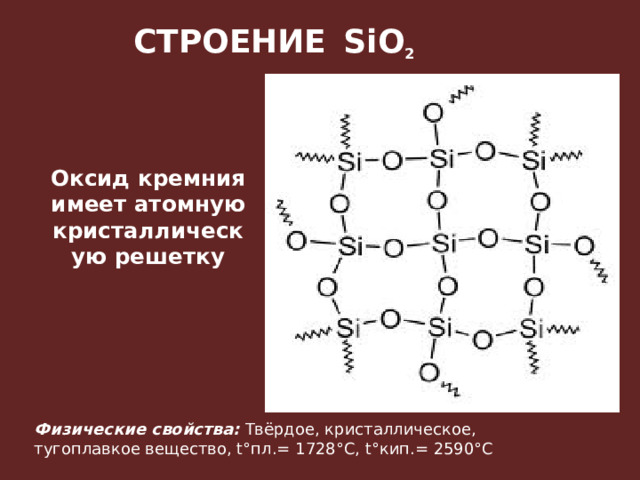
![Химические свойства оксида кремния: Кислотный оксид. При сплавлении взаимодействует с основными оксидами, щелочами, а также с карбонатами щелочных и щелочноземельных металлов: 1) С основными оксидами: SiO 2 + CaO t˚ → CaSiO 3 2) Со щелочами: SiO 2 + 2NaOH t˚ → Na 2 SiO 3 + H 2 O 3) С водой не реагирует 4) С солями: SiO 2 + CaCO 3 t˚ → CaSiO 3 + CO 2 SiO 2 + K 2 CO 3 t˚ → K 2 SiO 3 + CO 2 5) С плавиковой кислотой: SiO 2 + 4HF t˚ → SiF 4 + 2H 2 O SiO 2 + 6HF t˚ → H 2 [SiF 6 ] (гексафторкремниевая кислота) + 2H 2 O (реакции лежат в основе процесса травления стекла).](https://fsd.kopilkaurokov.ru/up/html/2026/03/13/k_69b3b052da20b/img_user_file_69b3b054b51ce_10.jpg)



















