~Цель данного мероприятия - ~повысить интерес к предмету, подвести к самостоятельным выводам и
обобщениям, сформировать умение проводить химический эксперимент, а также
обогатить кругозор и интеллект учащихся дополнительными знаниями.
Мероприятие проводится в рамках Недели химии.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
Внеклассное мероприятие "Удивительный мир химии"
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«БУЦ (из опыта работы)(книжка)»
Просмотр содержимого документа
«Методическая разработка внеклассного мероприятия»
Просмотр содержимого документа
«высказывания»
Просмотр содержимого документа
«программа вечера»
Просмотр содержимого документа
«Умение решать задачи есть искусство»
Просмотр содержимого презентации
«Уход за волосами, кожей, ногтями»
Просмотр содержимого презентации
«Уход за кожей. Болезни кожи»
Просмотр содержимого презентации
«хатынь»
Просмотр содержимого презентации
«Maket_igra»
Просмотр содержимого презентации
«игра по химии»
Похожие файлы
Полезное для учителя
Распродажа видеоуроков!
1660 руб.
2760 руб.
1700 руб.
2840 руб.
1660 руб.
2760 руб.
1660 руб.
2760 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства















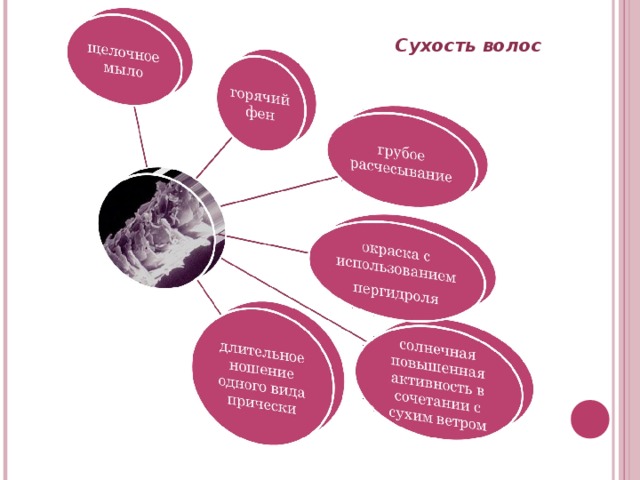




















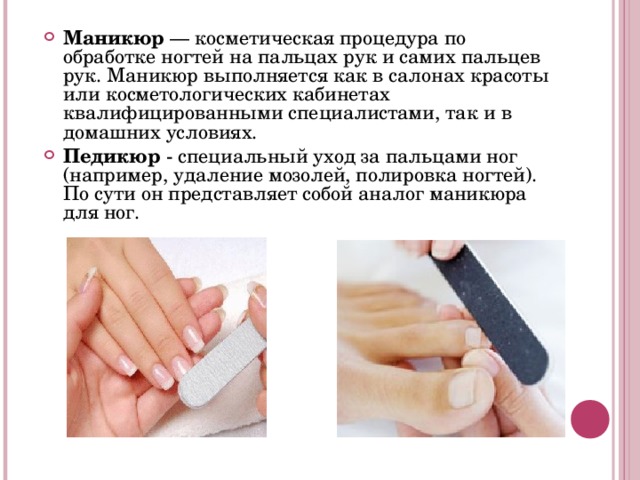













 пересыхают, ломкие, выпадают не охлаждать = увеличение слоя ПЖК = нарушение кровоснабжения = облысение" width="640"
пересыхают, ломкие, выпадают не охлаждать = увеличение слоя ПЖК = нарушение кровоснабжения = облысение" width="640"

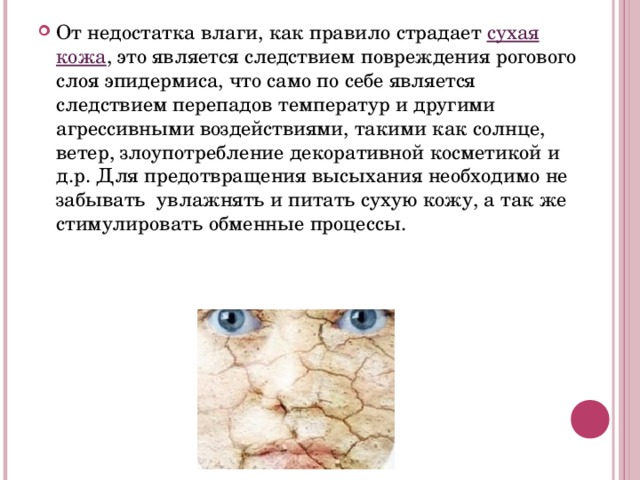
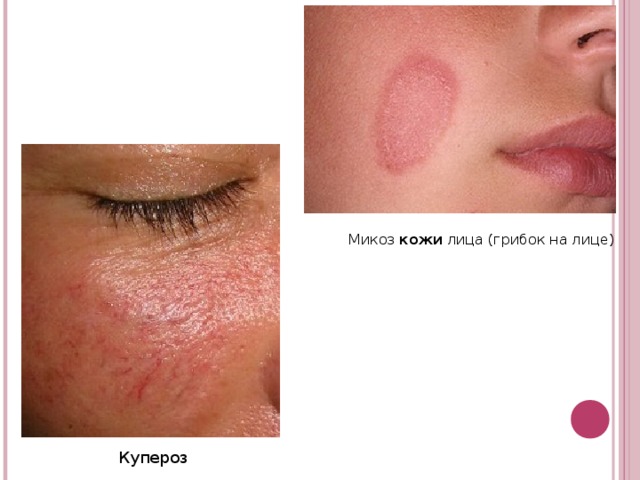
 избыточное питание = краснеет, сальный вид алкоголь = отечность, дряблость. недостаток витаминов: гиповитаминоз А = сухая, шероховатая гиповитаминоз В 2 = трещины в углах рта, ногти ломкие гиповитаминоз С = мелкоточечные кровоизлияния гормональные нарушения:" width="640"
избыточное питание = краснеет, сальный вид алкоголь = отечность, дряблость. недостаток витаминов: гиповитаминоз А = сухая, шероховатая гиповитаминоз В 2 = трещины в углах рта, ногти ломкие гиповитаминоз С = мелкоточечные кровоизлияния гормональные нарушения:" width="640"


























 " width="640"
" width="640"
 " width="640"
" width="640"
 " width="640"
" width="640"
 " width="640"
" width="640"
 " width="640"
" width="640"
 Закончить 50/50 100 Цена вопроса" width="640"
Закончить 50/50 100 Цена вопроса" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"
 Закончить" width="640"
Закончить" width="640"