Урок "Безопасное обращение с веществами". Интегрированный урок для учащихся 8-11 классов. Изучаются правила обращения с веществами на уроках химии и в быту. Проходит работа в группах. проводится практическая работа. На уроке рассматривается работа с едкими, горючими и ядовитыми веществами. Предлагается изучить средства бытовой химии, выявить опасные вещества. Также каждая группа оказывает первую медицинскую помощь при получении химического и термического ожога.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
Урок "Безопасное обращение с веществами"
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Задания для групп.»
Просмотр содержимого документа
«Факультатив. Безопасное обращение с веществами. 2014г.»
Просмотр содержимого презентации
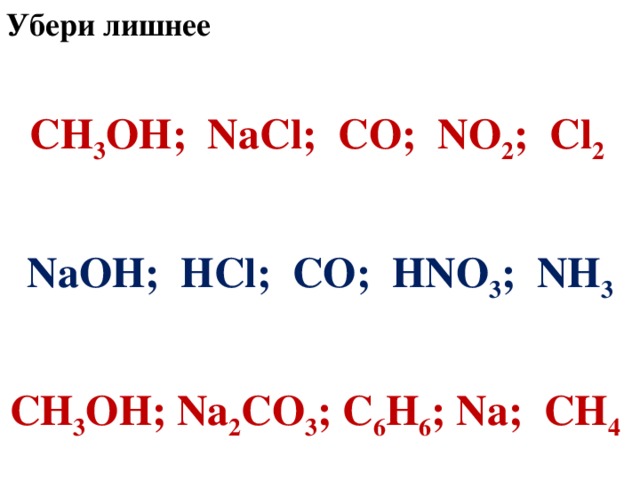
«Урок. Безопасное обращение с веществами.»
Похожие файлы
Полезное для учителя
Распродажа видеоуроков!
1660 руб.
2760 руб.
1660 руб.
2760 руб.
1690 руб.
2820 руб.
1700 руб.
2840 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства