Урок химии в 8 классе
«Чистые вещества и смеси»
Цели урока: 1. Закрепить знания номенклатуры неорганических веществ разных классов.
2. Сформировать понятия о чистом веществе и смеси веществ.
3. Раскрыть значение смесей в природе и жизни человека.
4. Познакомить со способами разделения смесей.
Формы организации познавательной деятельности учащихся: фронтальная, парная, групповая.
Оборудование:
- Химия 8 – учебник для 8 класса общеобразовательных учреждений под редакцией О.С.Габриеляна – М., Дрофа, 2007 г.
- Презентация в MS Power Point (приложение)
- Компьютер, проектор
Реактивы
- Смесь порошков железа и серы, раствор поваренной соли, смесь песка и воды, раствор метилового оранжевого; фильтры, выпаривательная чашка, лабораторный штатив с кольцом, спиртовка, воронка, стеклянная палочка, химические стаканы, колбы, магнит, пипетка.
Демонстрационный эксперимент:
- Разделение смеси фильтрованием;
- Разделение смеси магнитом;
- Хроматография;
- Разделение смеси веществ выпариванием.
Карточки с заданием для групповой работы.
Разделение смеси (раствора) растворимого вещества и растворителя:
Раствор поваренной соли, лабораторный штатив с кольцом, фарфоровая чашка (выпаривательная), спиртовка, тигельные щипцы, стеклянная палочка.
Разделение смеси нерастворимого в воде вещества и растворителя (растворимого вещества):
Лабораторный штатив с кольцом, воронка, фильтровальная бумага, стеклянная палочка, колба или стакан химический.
Разделение смеси железа и серы:
Железные опилки, порошок серы, магнит , 2 фильтра.
Хроматография:
Фильтр, раствор метилоранжа, пипетка.
Ход урока
I.Организационный момент. Проверка домашнего задания.
1.Беседа:
- Какие соединения называются оксидами? (Оксиды – это сложные соединения, состоящие из двух элементов, один из которых кислород со степенью окисления (-2))
- Какие соединения называются кислотами? (Кислоты – это сложные вещества, состоящие из атомов водорода и кислотного остатка)
- Какие соединения называются основаниями? (Основание – это сложные вещества, состоящие из атомов металла и одной или нескольких гидроксогрупп OH-)
- Какие соединения называются солями? ( Соли – это сложные вещества, состоящие из атомов металла и кислотных остатков)
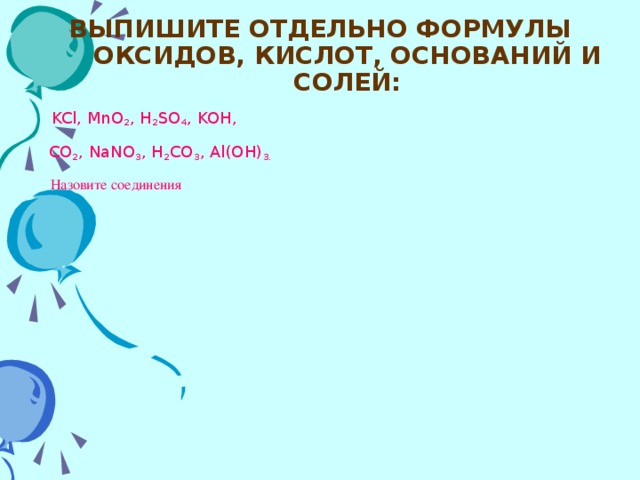
2.Проверочная работа (5-7 минут) на листках. На слайдах 1-2 - вопросы проверочной работы.
3.Проверочная работа сдается учителю (результаты объявляются на следующем уроке).
II.Подготовка к восприятию нового материала. Объявление темы.
1. Беседа
1. Нам хорошо знакомо, что такое чистота. Чистая тетрадь, чистые руки, чистый лист … А какое вещество считается чистым? Есть ли в природе чистые вещества? Чем отличается чистое вещество от смеси веществ?
2. Как вы думаете, что будет темой нашего урок сегодня? (слайд 3)
2. Запись даты и темы урока учащимися в тетради.
Как вы думаете, что мы должны сегодня выяснить на уроке?
Цели урока обсуждаются с учащимися.
Учащиеся предлагают: выяснить, какое вещество считается чистым и что такое смесь; узнать, где применяются чистые вещества и смеси; узнать, как разделить вещества.
В результате обсуждения - слайд 4.
3. Объяснение нового материала.
На данном этапе урока учитель формирует понятие о чистом вещества и смеси. Учащимся известно понятие «вещество» (это то, из чего состоят физические тела). Поэтому, вначале даем определение «смеси веществ».
Учитель предлагает ученикам рассмотреть смеси, находящиеся на демонстрационном столе и примеры смесей, представленные на слайде 5.
Далее ребята дают определение смеси, как системы из их нескольких веществ, находящихся в непосредственном контакте друг с другом. Эта формулировка появляется на слайде после щелчка мыши.
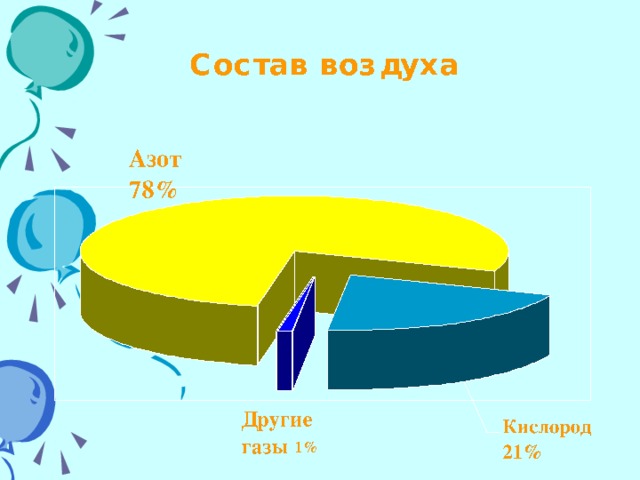
Учитель дополняет, что в природе нет абсолютно чистых веществ. Вещества встречаются преимущественно в виде смесей. Учитель приводит примеры смесей, ребята записывают их в тетради: воздух, морская вода, молоко, сплавы металлов, растворы, туман и др. Он рассказывает о воздухе, как смеси, которая состоит из газов – азота, кислорода, аргона и др. (слайд 6).
Посмотрите внимательно на смеси, находящиеся на столе. В чем разница между ними?
Далее рассматривается классификация смесей (слайда 7).
Смеси
Однородные
Неоднородные
Раствор сахара в воде, растворы солей, воздух
Смесь Fe +S, песок и сахар, глина с водой, песок с водой
Неоднородными называются смеси, в которых невооруженным глазом или при помощи микроскопа видны частицы веществ, составляющих смесь.
Однородными называют смеси, в которых нельзя заметить частицы веществ, входящих в смесь (даже при помощи микроскопа).
Для научных исследований и промышленности, в основном требуются чистые вещества. Некоторые примеси даже в небольших количествах способны сильно поменять свойства веществ. Например, в полупроводниковой технике применяют сверхчистые вещества, где примеси составляют всего 1 атом на миллион атомов основного элемента (Si, Ge). Превышение нормы ведет к резкому ухудшению полупроводниковых свойств этих веществ. В тоже время, необходимо выделить, что невозможно получить абсолютно чистое вещество, т.к. любое чистое вещество содержит, хотя ничтожное малое количество примесей.
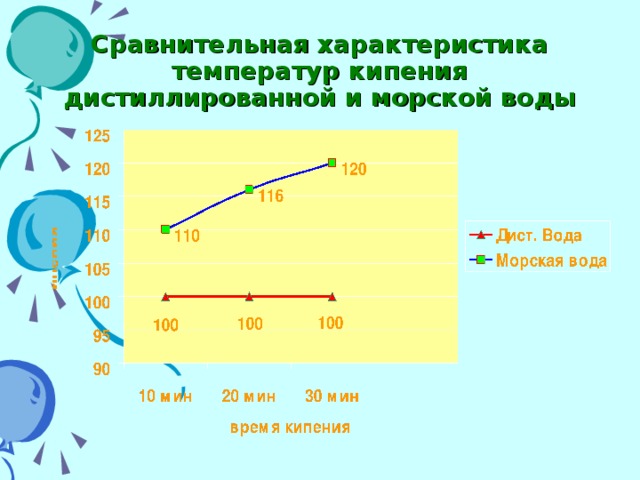
Как вы думаете, морская вода и чистая дистиллированная вода будут обладать одинаковыми свойствами? (ребята предполагают, что нет). Слайд 8. Учитель объясняет условия эксперимента: в 2-х сосудах нагревали до кипения дистиллированную и морскую воду. Через определенное время измеряли температуры кипения в этих сосудах с помощью датчиков «Архимед». Вместе обсуждаем результаты эксперимента. Встает проблема: «Почему у морской воды t кип не постоянная в разные промежутки времени по сравнению с t кип дистиллированной водой?»
Учащиеся высказывают предположение, что соленость морской воды влияет на tкип.
Далее учитель предлагает дать определение «чистого вещества».
С помощью учителя формулируется определение «Чистым веществом называется такое вещество, у которого постоянные физические свойства (температуры кипения, температуры плавления, плотность).
В тетрадях ребята записывают определение «чистое вещество»
Чистым называется вещество, которое обладает постоянными физическими свойствами.
Учитель дополняет, что в чистом веществе примеси, хотя и есть в незначительных количествах, но они не влияют на физические и химические свойства. Пример чистого вещества - дистиллированная вода.
Демонстрируется слайд 9.
Ребята записывают в тетрадях выводы.
Педагог обращает внимание детей на отличительную особенность смесей «В смесях каждое из составляющих их веществ сохраняет свои индивидуальные свойства. Для подтверждения этого учитель проводит опыты:
- Демонстрация разделение смеси железа и сера с помощью магнита (отработать с ребенком заранее методику выполнения опыта и тогда демонстрацию проводит ученик)
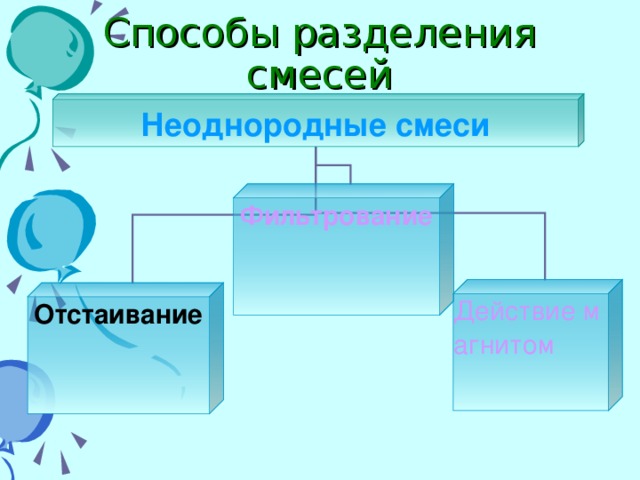
Следующий этап урока – знакомство с основными способами разделения смесей, которые представлены в виде схемы: Слайд 10.
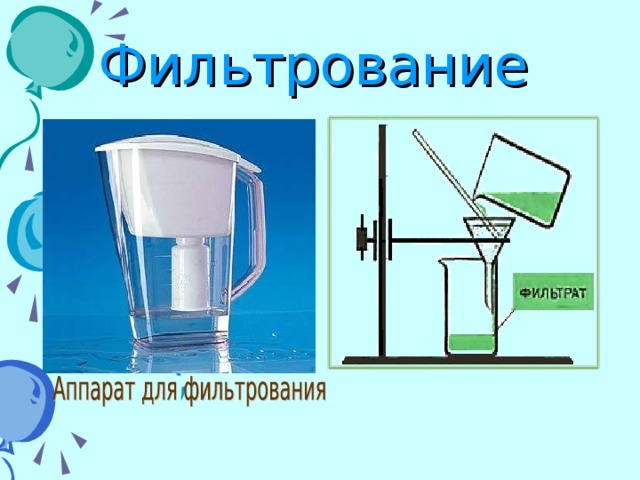
Одновременно уточняется, на каких физических свойствах веществ основан каждый способ разделения. На слайдах 11- 13 показаны области применения разных способов очистки неоднородных смесей.
Демонстрация разделения смеси песка и воды фильтрованием. Обращается внимание на правильность выполнения эксперимента (Слайд 11).
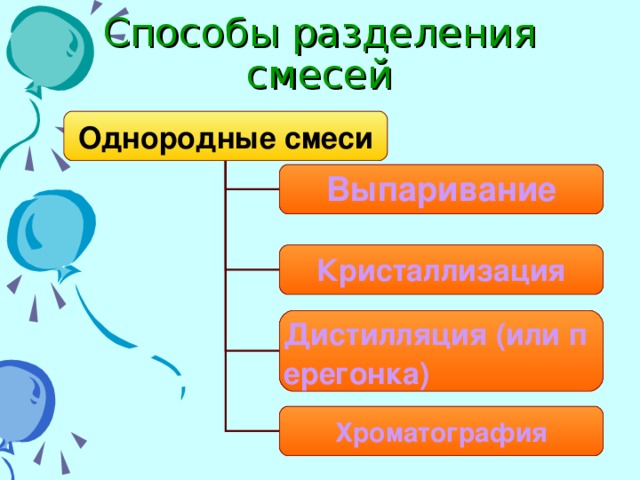
Знакомство со способами разделения однородных смесей продолжается с помощью слайда 14, акцентируется внимание учащихся на физических свойствах веществ, применяемых в данном способе разделения.
На слайдах 14-18 показаны области применения разных способов очистки однородных смесей.
4. Закрепление
1. Групповая работа.
Каждая группа получила задание « Как разделить смесь?»
Нужно было описать свои действия. Через 1 минуту каждая группа озвучила свой ответ. В заданиях были использованы жизненные ситуации, где требовалось очистить воду в походных условиях и т.п.
2. Ответить на вопросы, представленные на слайдах 19 – 21
5. Рефлексия.
Беседа:
Что нового вы узнали сегодня на уроке?
Что запомнилось?
Что понравилось, а что не удалось, на ваш взгляд?
6.Подведение итогов
7. Домашнее задание: § 23 упр. 1,2,4
Творческое задание.
1. Составьте задания на разделение смеси.
2. Вам выдали смесь, состоящую из соли и мела.
Предложите способы разделения этой смеси.