Тема урока «Изопроцессы в газах»
Тип урока : изучение нового материала.
Цель урока:
Образовательная: установить зависимость между двумя термодинамическими параметрами при неизменном третьем.
Развивающая: сформировать элементы творческого поиска на основе приема анализа ранее изученного материала.
Воспитательная: показать значение причинно-следственных связей в познаваемости явлений, развитие коммуникативных способностей учащихся.
Задачи урока:
Образовательные:
? способствовать формированию навыков в анализе условий поставленной проблемы;
? развивать умения делать выводы на основе анализа поставленной задачи;
? развитие умений в построении математических действий ведущих к решению поставленной задачи;
? на основе повторения ранее изученного материала углубить знания по данной теме,
? способствовать развитию умений систематизировать полученные знания.
Развивающие:
? развивать умения высказывать свою точку зрения, вести аргументированный разговор;
? способствовать развитию навыков в умении переходить от общих законов и явлений к частным случаям(анализировать);
? способствовать повышению уровня самостоятельности мышления школьников;
? формирование элементов творческого поиска;
? развитие абстрактного мышления.
Воспитательные:
? побудить учащихся к активности;
? создать условия для формирования навыков самооценки и самоанализа.
Оборудование:
? презентация, таблицы, компьютер, ноутбук, проектор; лаборатория L- микро для демонстрации опытов.
Просмотр содержимого документа
«презентация по теме "Изопроцессы в газах"»

Prezentacii.com
ИЗОПРОЦЕССЫ В ГАЗАХ
10 класс
.

ЦЕЛЬ:
установить зависимость между двумя макроскопическими параметрами газа при неизменном третьем.

ИЗОПРОЦЕСС -
процесс, при котором один из макроскопических параметров состояния данной массы газа остается постоянным.
V, p, Т
ИЗО – (ПОСТОЯННЫЙ)
Изобарный
изопроцессы
Изохорный
Изотермический

ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС -
ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ.
const
Т
const
m
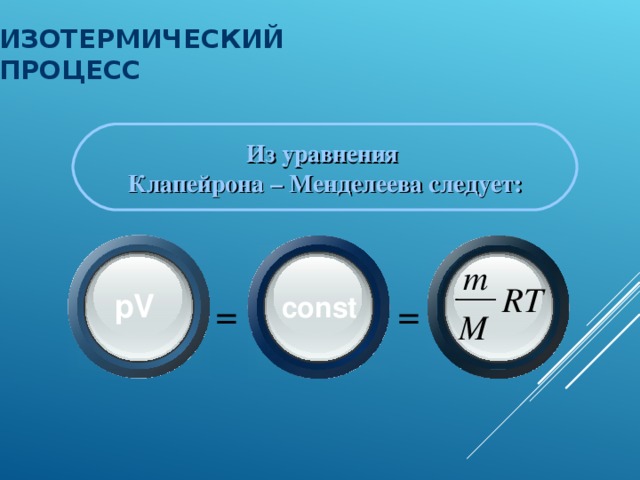
ИЗОТЕРМИЧЕСКИЙ ПРОЦЕСС
Из уравнения
Клапейрона – Менделеева следует:
m
RT
pV
=
=
const
M

ЗАКОН БОЙЛЯ – МАРИОТТА.
Закон экспериментально получен в:
- 1662 г. Р. Бойлем;
- 1676 г. Э. Мариоттом.
Р. Бойль
T - const
Для газа данной массы при постоянной температуре произведение давления газа на его объем постоянно:
p 1 V 1 = p 2 V 2
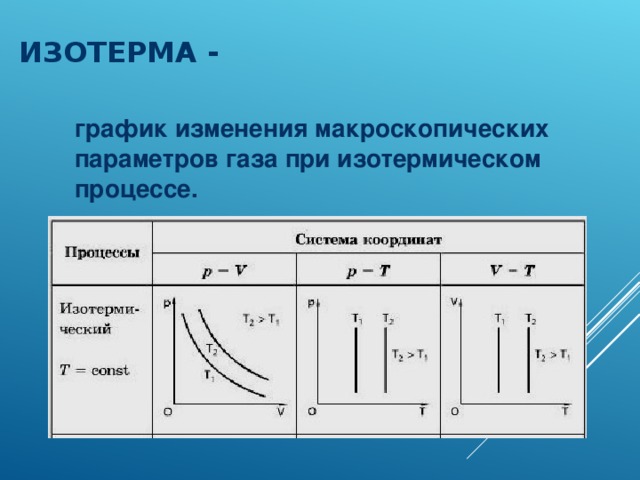
ИЗОТЕРМА -
график изменения макроскопических параметров газа при изотермическом процессе.

ИЗОБАРНЫЙ ПРОЦЕСС -
ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ.
const
P
const
m

ИЗОБАРНЫЙ ПРОЦЕСС
Из уравнения
Клапейрона – Менделеева следует:
m R
V
=
=
const
M p
T

ЗАКОН ГЕЙ-ЛЮССАКА.
Закон экспериментально
получен в 1802 г.
p - const
ГЕЙ-ЛЮССАК
Жозеф Луи
Для газа данной массы при постоянном давлении отношение объема газа к его термодинамической температуре постоянно:
V 1 / T 1 = V 2 / T 2
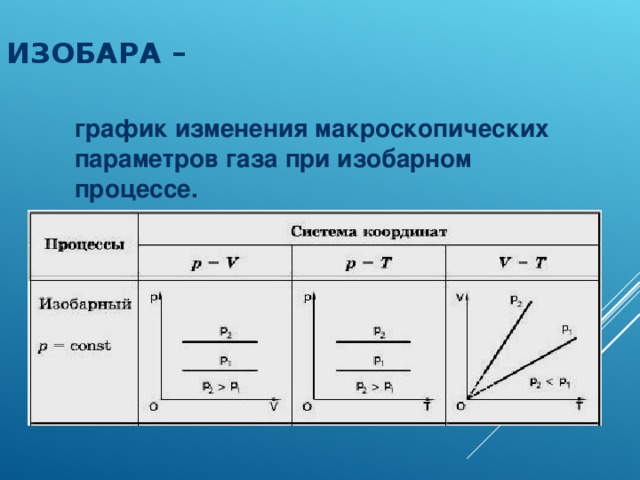
ИЗОБАРА –
график изменения макроскопических параметров газа при изобарном процессе.

ИЗОХОРНЫЙ ПРОЦЕСС -
ПРОЦЕСС ИЗМЕНЕНИЯ СОСТОЯНИЯ ОПРЕДЕЛЕННОЙ МАССЫ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ.
const
V
const
m

ИЗОХОРНЫЙ ПРОЦЕСС
Из уравнения
Клапейрона – Менделеева следует:
m R
p
=
=
const
M V
T

ЗАКОН ШАРЛЯ.
Закон экспериментально
получен в 1787 г.
V - const
Для газа данной массы при постоянном объеме отношение давления газа к его термодинамической температуре постоянно:
p 1 / T 1 = p 2 / T 2
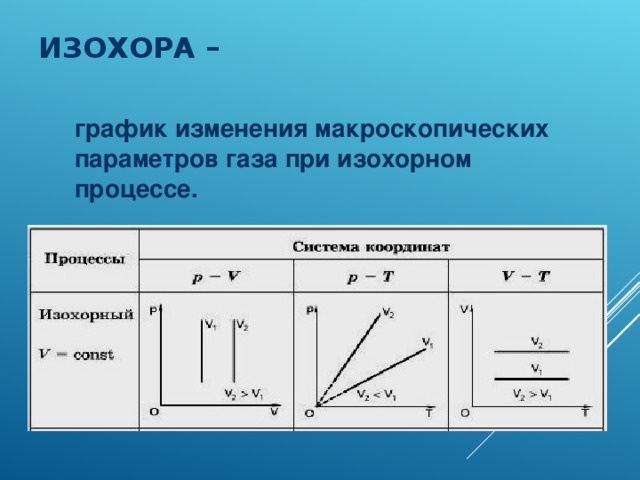
ИЗОХОРА –
график изменения макроскопических параметров газа при изохорном процессе.


ДОМАШНЕЕ ЗАДАНИЕ
§ 69 ,используя интернет, познакомиться с законом Дальтона( в чем заключается данный закон и при каких условиях он применим)


































