ПРОЕКТ «КРИСТАЛЛЫ И ИХ ПРИМЕНЕНИЕ»
Введение
Поэзия! Завидуй кристаллографии! Кусай ногти в гневе и бессилии!
О. Мандельштам
Мы живем в мире, в котором большая часть веществ находится в твердом состоянии. Мы пользуемся различными механизмами, инструментами, приборами. Мы живем в домах и квартирах. Имеем мебель, бытовые приборы, современнейшие средства связи: радио, телевидение, компьютеры и т. д. А ведь все это твердые тела. С физической точки зрения, человек - твердое тело. Так что же такое твердые тела?
В отличие от жидкостей, твердые тела сохраняют не только объем, но и форму, т. к. положение в пространстве частиц, составляющих тело, стабильно. Из-за значительных сил межмолекулярного взаимодействия частицы не могут удаляться друг от друга на значительные расстояния.
В природе часто встречаются твердые тела, имеющие форму правильных многогранников. Такие тела назвали кристаллами. Изучение физических свойств кристаллов показало, что геометрически правильная форма - не главная их особенность.
Знаменитое изречение академика А. Е. Ферсмана «Почти весь мир кристалличен. В мире царит кристалл и его твердые прямолинейные законы» полностью согласуется с неугасающим научным интересом ученых всего мира и всех областей знания к данному объекту исследования. Так, в конце 60-х годов прошлого века начался серьезный научный прорыв в области жидких кристаллов, породивший «индикаторную революцию» по замене стрелочных механизмов на средства визуального отображения информации. Позже в науку вошло понятие биологический кристалл (ДНК, вирусы и т. д.), а в 80-х годах XX века - фотонный кристалл.
Что такое кристаллы? Какими свойствами они обладают? Что такое кристаллическая решетка? Как растут кристаллы? Как и где они применяются в настоящее время и каковы перспективы их применения в будущем? Вот эти вопросы заинтересовали нас, и мы попытались найти на них ответы сами, т. к. в учебнике этой теме отводится только один параграф и ответов на эти вопросы мы не нашли, или эти ответы были неполными и из них не было видно, почему именно благодаря кристаллам произошел «серьезный прорыв» в науке и технике.
Чтобы наиболее полно и всесторонне изучить эту проблему, мы создали четыре группы: теоретики, инженеры, ювелиры и экспериментаторы. Перед каждой группой стояли свои цели и решались определенные задачи.
Мы предлагаем результаты нашей работы вашему вниманию.
ОТЧЕТ ГРУППЫ ТЕОРЕТИКОВ
Цели: проследить эволюцию взглядов на природу кристаллов; изучить строение и физические свойства кристаллов, благодаря которым они нашли такое широкое применение.
Задачи: познакомиться с представлениями ученых о твердых кристаллах на протяжении нескольких столетий; рассмотреть особенности пространственных решеток и классифицировать их по сингониям; изучить физические свойства кристаллов: изотропность, анизотропность, полиморфизм, симметрию.
Кристаллы
1. Понятие «кристалл». Знания человека о кристаллах.
Слово «кристаллос» у древних греков обозначало лед. Так же назывался и водяно-прозрачный кварц (горный хрусталь), ошибочно считавшийся тогда «окаменевшим льдом». Впоследствии этот термин был распространён на все кристаллические тела.
В школьных учебниках кристаллами обычно называют твердые тела, образующиеся в природных или лабораторных условиях и имеющие вид многогранников, которые напоминают самые непогрешимо строгие геометрические построения. Поверхность таких фигур ограничена более или менее совершенными плоскостями - гранями, пересекающимися по прямым линиям -ребрам. Точки пересечения ребер образуют вершины. Однако стоит заметить, что данное определение нельзя назвать правильным и оно требует ряд существенных поправок, так как охватывает не все кристаллические образования.
2. Разнообразие форм кристаллов. Симметрия в кристаллах.
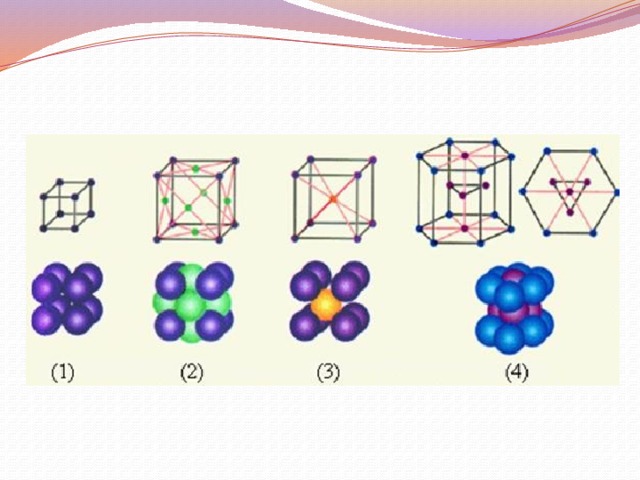
Как известно, форма является вторичной по отношению к содержанию. В соответствии с этим и кристаллографы всегда подчеркивают, что форма кристалла прежде всего зависит от его внутреннего строения, т. е. от кристаллической структуры (под структурой понимается пространственное расположение всех материальных частиц: атомов, молекул, ионов, слагающих кристалл).
Такую структуру схематично изображают в виде пространственной решетки. При этом вершины, ребра и грани кристалла соответствуют узлам, рядам и плоским сеткам решетки. «Важнейшие» грани, лучше всего развитые и чаще всего встречающиеся на кристаллах какого-либо вещества, совпадают с плоскими сетками, наиболее густо покрытыми частицами. Этот закон, открытый французским ученым Огюстом Браве (1811-1863), дает понятие о зависимости формы кристалла от его структуры. Вместе с тем не стоит забывать о том, что на формирование кристаллического тела накладывает свой отпечаток и питающая его среда.
Обратимся теперь к самим формам кристаллов и познакомимся с тем, как кристаллографы научились их определять и даже наперед предсказывать. Подчеркнем, что ими был создан строго математический вывод всех возможных на свете кристаллических форм.
В течение долгих столетий геометрия кристаллов казалась таинственной и неразрешимой загадкой. Не случайно на гравюре великого немецкого художника Альбрехта Дюрера (1471-1528) изображена Меланхолия в виде печального ангела, безнадежно всматривающегося в огромный кристалл. Вплоть до XVII в. дальше описаний «удивительных угловатых тел» дело не шло.
В 1619 г. великий немецкий математик и астроном Иоганн Кеплер (1571—1630) обратил внимание на шестерную симметрию снежинок. Он попытался объяснить ее тем, что кристаллы построены из мельчайших одинаковых шариков, теснейшим образом присоединенных друг к другу (вокруг центрального шарика можно вплотную разложить только шесть таких же шариков). По пути, намеченному Кеплером, пошли впоследствии Роберт Гук (1635-1703) и М. В. Ломоносов (1711-1765). Они также считали, что элементарные частицы внутри кристаллов можно уподобить плотно упакованным шарикам. В наше время принцип плотнейших шаровых упаковок лежит в основе структурной кристаллографии, только сплошные шаровые частицы («корпускулы») старинных авторов заменены сейчас сферами действия атомов и ионов.
Через 50 лет после Кеплера (в 1669 г.) датский геолог, кристаллограф и анатом Николаус Стеной (1638-1686) впервые сформулировал основные понятия о формировании кристаллов: «Рост кристалла происходит не изнутри, как у растений, но путем наложения на внешние плоскости кристалла мельчайших частиц, приносящихся извне некоторой жидкостью». Эта идея о росте кристаллов в результате отложения на гранях все новых и новых слоев вещества сохранила свое значение и до сих пор.
Внимательно разглядывая реальные кристаллы кварца, Стеной обратил также внимание на их отклонения от идеальных геометрических многогранников с плоскими гранями и прямыми ребрами. В своем трактате он впервые ввел в науку реальный кристалл с его несовершенствами и отклонениями от идеализированных схем. Однако все эти отклонения не помешали ученому открыть на тех же кристаллах кварца основной закон геометрической кристаллографии - закон постоянства углов. К сожалению, написал он об этом очень кратко в пояснениях к рисункам, приложенным к его сочинению.

Рис.4
Закон постоянства углов окончательно утвердился в науке после выхода в свет «Кристаллографии» (1783 г.) французского естествоиспытателя Ж. Б. Роме де Лиля (1736-1790): «Грани кристалла могут изменяться по своей форме и относительным размерам, но их взаимные наклоны постоянны и неизменны для каждого рода кристаллов». В этой формулировке Роме де Лиль обобщил свои многолетние труды по измерению многочисленнейших углов на кристаллах разнообразных веществ (см. рис. 4). Закон постоянства углов явился надежным фундаментом для развития геометрической кристаллографии и дал богатейший материал для установления истинной симметрии кристаллических тел. Впоследствии он лег в основу специ- альных методов Е. С. Федорова, А. К. Болдырева, Т. Баркера и др. Эти методы позволяют по углам между гранями, т. е. по внешней форме кристаллов, определять их вещество.
Старательно изучая кристаллы и измеряя их характерные углы, Роме де Лиль не позволял себе углубляться в рассуждения об их внутреннем строении. Гораздо смелее в этом отношении был его младший современник и удачливый соперник Рене Жюст Гаюи (1743-1822). «Все найдено!», - воскликнул он, заметив, что случайно выпавший из его рук большой кристалл кальцита раскололся на множество маленьких параллелепипедальных (ромбоэдрических) осколков (кальцит обладает хорошей спайностью - способностью раскалываться - по ромбоэдру). В этот именно момент в его уме зародилась новая теория строения кристаллов. В отличие от Кеплера, Гука и Ломоносова, Гаюи предположил, что кристаллы построены не из мельчайших шариков, а из молекул параллелепипедальной формы и что предельно малые спайные осколки и являются этими самыми молекулами. Иными словами, кристаллы представляют собой своеобразные кладки из молекулярных «кирпичиков» (см. рис. 5)
![]()
Несмотря на всю свою наивность с современной точки зрения, эта теория сыграла в свое время большую историческую роль, дав толчок к зарождению теории решетчатого строения кристаллов. Этим не исчерпываются заслуги Гаюи. Впервые обратил он внимание на то, что наблюдателю, разглядывающему кристалл с разных сторон, нередко кажется, что перед ним как бы повторяется одна и та же картина. Объясняется это тем, что такой кристалл состоит из повторяющихся равных частей. Иными словами, Гаюи одним из первых уловил симметричное строение множества кристаллических тел. Ему же принадлежит способ математической характеристики кристаллических граней, с помощью которого можно было даже предсказать, какие именно грани возможны для данного кристалла.
Прямым продолжателем Гаюи явился французский кристаллограф Браве. Будучи моряком-метеорологом, Браве заинтересовался формами снежинок и стал углубленно заниматься наукой о кристаллах. В отличие от своих предшественников, приписывавших элементарным частицам в кристаллах шаровую или параллелепипедальную форму, Браве отказался от всяких предположений относительно таинственных и недоступных тогда форм молекул или атомов. Молекулярные «кирпичики» Гаюи были заменены Браве точками - центрами их тяжести. Легко понять, что, выделив в кирпичной кладке центры тяжести всех кирпичиков, мы получим уже знакомую нам пространственную решетку.
Высказав гипотезу о решетчатом строении всех вообще кристаллических тел, Браве заложил основу современной структурной кристаллографии задолго до экспериментальных исследований кристаллических структур с помощью рентгеновских лучей. Исходя из его гипотезы, ставшей в настоящее время общепринятой теорией, легко доказать ряд основных положений геометрической кристаллографии.
Именно так устанавливается важнейший закон кристаллографической симметрии, согласно которому для кристаллов возможны оси симметрии лишь первого, второго, третьего, четвертого и шестого порядков (этот закон относится не только к простым, но и к сложным - инверсионным и винтовым - осям). Тем самым на кристаллических фигурах никогда не бывает осей симметрии пятого порядка, а также осей симметрии порядка выше шестого, так как они невозможны в решетках.
Так был найден важнейший закон, проводящий границу между симметрией кристаллов и симметрией растений и животных. Для кристаллов пятерные оси и оси порядка выше шестого категорически запрещены. В 1830 г., задолго до Браве, немецкий профессор Иоганн Фридрих Гессель (1796-1872) опубликовал в физическом словаре большую статью под названием «Кристаллометрия», в которой дал полный вывод совокупностей элементов симметрии для конечных фигур в самом широком смысле этого понятия. Судьба замечательной статьи Гесселя оказалась трагической: ее никто не понял и не оценил. Отчасти в этом виноват был и сам автор, уж очень тяжеловесно и громоздко описал он свои открытия. В результате многие десятки лет работа Гесселя лежала без движения в пыли старых библиотек.
Лишь в 1890 г., через 60 лет после опубликования этого груда и через 18 лет после смерти его автора, кристаллографы заново открывают вывод Гесселя. «В это время, - по горестному замечанию Е. С. Федорова, - кости Гесселя давно успели рассыпаться и истлеть в могиле».
В 1867 г. наш соотечественник, крупный военный специалист, профессор артиллерийского училища академик А. В. Га-долин (1828-1892), не подозревая о существовании трудов Гесселя и Браве, снова взялся за вывод законов симметрии. К тому времени минералоги и кристаллографы собрали огромный материал по кристаллическим формам минералов. В России особенно много работал в этом направлении академик Н. И. Кокшаров (1818 - 21 декабря 1892 (2 января 1893)) - автор 11-томных «Материалов для минералогии России» и обширного атласа с многочисленными и точными изображениями кристаллов русских минералов.
![]()
А. В. Гадолин, дружески связанный с Н. И. Кокшаровым, был также большим любителем и знатоком минералов и их кристаллических форм. В связи с этим он и обратил все свое внимание на симметрию кристаллов. В его классическом труде «Вывод всех кристаллографических систем и их подразделений из одного общего начала» раз и навсегда было установлено существование 32 видов симметрии для конечных кристаллографических фигур (т. е. для кристаллических многогранников). Простой и изящный вывод А. В. Гадолина, иллюстрированный наглядными примерами из мира минералов, завоевал всеобщее признание.
Дальнейшим шагом в учении о симметрии кристаллов явился опубликованный в 1890 г. гениальный вывод Е. С. Федорова 230 совокупностей элементов симметрии для бесконечно
протяженных кристаллических систем с их трансляциями, винтовыми осями и плоскостями скользящего отражения (годом позже со своим выводом 230 пространственных групп выступил немецкий математик Артур Шенфлис). Федоровские группы, соответствующие геометрическим законам расположения атомов в кристаллических структурах, лежат в основе современной структурной кристаллографии. Таким путем после многих затруднений, проб и ошибок учение о симметрии кристаллов достигло своего высшего расцвета.
Однако необходимо вернуться к 32 видам конечной кристаллографической симметрии, так как именно они являются основой математического вывода форм, возможных для кристаллов. Сначала придется поговорить о том, как выводятся сами виды симметрии.
При переходе к собственно кристаллическим видам симметрии задача существенно упрощается. Ведь кристаллические тела не могут обладать осями симметрии пятого порядка, а также всеми осями порядка выше шестого. Следовательно, на кристаллах встречаются лишь следующие оси симметрии: Li, Ъ, Ьз, L4, L6. К простым осям следует добавить инверсионные оси тех же порядков.
Рассматривая инверсионные оси первого и второго порядков как центр и плоскость симметрии, получим следующий полный набор элементов симметрии для конечных кристаллических фигур (кристаллических многогранников):
С, Р, Li, L?, L3, L4, Ьб, L14, Li6.
Перебрав все возможные комбинации перечисленных элементов симметрии, мы и получим 32 комбинации - 32 вида симметрии.
Виды симметрии подразделяются на три категории (низшую, среднюю и высшую) и на семь систем г- сингоний, совпадающих с горизонтальными строчками таблицы.
«Сингония» - по-гречески сходноугольность. Название «триклинная» указывает также по-гречески на три косых угла (система координатных осей для триклинных кристаллов является целиком косоугольной). «Моноклинная» - один косой угол (в системе координатных осей один угол косой и два прямых). «Ромбическая» сингония обнаруживает часто наличие ромбических сечений в кристаллах. «Тригональная» - треугольная; «тетрагональная» - четырехугольная; «гексагональная» - шестиугольная. Эти названия также связаны с характерными сечениями кристаллических форм. Название «кубическая» сингония происходит от главной формы — куба.
Монокристаллы и поликристаллы
Кристаллические тела могут быть монокристаллами и поликристаллами. Монокристаллом называют одиночный кристалл, имеющий макроскопическую упорядоченную кристаллическую решётку. Монокристаллы обычно обладают геометрически правильной внешней формой, но этот признак не является обязательным.
Большинство встречающихся в природе и получаемых в технике твердых тел представляют собой совокупность сросшихся друг с другом хаотически ориентированных маленьких кристаллов - кристаллитов. Такие тела называются поликристаллами. В отличие от монокристаллов поликристаллы изотропны, т. е. их свойства одинаковы во всех направлениях.
Полиморфизм
![]()
![]()
Очень многие вещества в кристаллическом состоянии могут существовать в двух или более фазовых разновидностях (модификациях), отличающихся физическими свойствами. Это явление называется полиморфизмом. Каждая модификация устойчива в определенном интервале температур и давлений. Из 9 кристаллических фаз воды только одна устойчива при атмосферном давлении. Остальные 8 фазовых состояний льда существуют при высоких давлениях и имеют плотность большую, чем у воды. Одна из них при давлении 2-Ю9 Па имеет температуру плавления +80 °С, т. е. существует «горячий лед».
Упорядоченное расположение атомов или молекул в кристалле определяется действием сил межатомного или межмолекулярного взаимодействия. Тепловое движение атомов и молекул нарушает эту упорядоченную структуру. При каждом сочетании давления и температуры реализуется тот тип укладки частиц, который в данных случаях наиболее устойчив и энергетически выгоден, т. е. то или иное фазовое состояние.
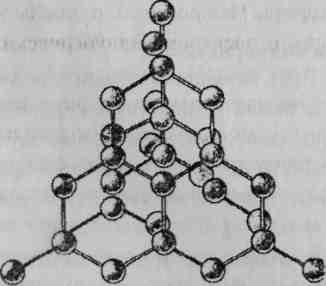
Превращения кристаллов одного и того же вещества с различным типом решетки друг с другом происходят в соответствии с фазовыми переходами типа плавления и испарения. Каждому давлению соответствует определённая температура, при которой оба типа кристаллов сосуществуют. При изменении этих условий происходит фазовый переход. Хорошим примером данного явления является углерод. В природе встречаются три аллотропические модификации углерода: алмаз, графит и карбин.
Алмаз (пространственная решетка алмаза) - кристаллическое вещество с атомной кристаллической решеткой. Каждый атом в кристалле алмаза связан прочными ковалентными связями с четырьмя соседними атомами. Это обусловливает исключительную твердость алмаза. Алмаз широко применяют для обработки особо твердых материалов: для резки стекла, при буровых работах, для вытягивания проволоки и др. Производительность труда при использовании алмазного обрабатывающего инструмента в промышленности возрастает в 2-5 раз.
Алмаз практически не проводит электрический ток, плохо проводит тепло. Прозрачные образцы алмаза сильно преломляют лучи света и при огранке красиво блестят, из таких алмазов делают украшения (бриллианты).
Графит (пространственная решетка графита) непрозрачен, серого цвета, обладает металлическим блеском. В кристаллической решетке графита атомы углерода расположены слоями, состоящими из шестичленных колец. В них каждый атом углерода связан прочными ковалентными связями с тремя соседними атомами. За счет четвертого валентного электрона каждого слоя возникает металлическая связь. Этим объясняется металлический блеск и довольно хорошая электрическая проводимость и теплопроводность графита. Из графита изготовляют электроды для электрохимических и электрометаллургических процессов.

Между слоями в графите действуют межмолекулярные силы. Поэтому графит легко расслаивается на чешуйки. Даже при слабом трении графита о бумагу на ней остается серый след («графит» от латинского «пишущий»). Графит применяют для изготовления грифелей карандашей, в технике - в качестве смазочного материала.
Графит тугоплавок, химически весьма устойчив. Из смеси графита с глиной изготовляют огнеупорные тигли для выплавки металлов в металлургии. Графит применяют как материал для труб теплообменников в химической промышленности. В ядерных реакторах его используют в качестве замедлителя нейтронов.

Карбин стал известен сравнительно недавно. Он был получен советскими учеными, а уже позднее обнаружен в природе. Это черный порошок. Кристаллическая решетка построена из линейных углеродных цепочек. По электрической проводимости карбин занимает промежуточное положение между алмазом (диэлектрик) и графитом (проводник): карбин - полупроводник.
Аллотропические модификации углерода взаимопревращаемы. При нагревании алмаз постепенно переходит в графит. Для превращения графита в алмаз требуются очень высокое давление (порядка 1-10" Па) и высокая температура (1500-3000 °С). В настоящее время искусственное получение алмазов из графита проводится в производственных масштабах.
Много внимания уделял человек изучению кристаллов и их свойств. Современные знания о кристаллах не являются полными, но эти знания позволяют использовать кристаллы во многих сферах человеческой деятельности.
Анизотропия
Плотность расположения частиц в кристаллической решетке не одинакова по различным направлениям. Это приводит к зависимости свойств монокристаллов от направления - анизотропии.
Анизотропия - зависимость физических свойств вещества от направления. Физические свойства поликристаллов не зависят от направления: они изотропны.
Изотропия- независимость физических свойств вещества от направления.
Простейший пример анизотропии кристаллов - неодинаковая их прочность по разным направлениям. Это свойство наглядно проявляется при дроблении кристаллических тел.
История показала, что тепловые, электрические и оптические свойства также не одинаковы по различным направлениям. Анизотропия физических свойств кристаллов и правильная внешняя форма получили объяснение на основе атомно-молекуляриой теории строения вещества.
Различна в разных направлениях и теплопроводность монокристаллов. У графита теплопроводность вдоль слоев в четыре раза больше, чем по нормали к слоям: тепло легче передается в тех плоскостях и направлениях, где атомы плотнее упакованы.
Графит - пример кристалла с так называемой слоистой структурой, у него различие структуры вдоль слоев и поперёк них бросается в глаза. В других структурах эти различия могут быть не так уж очевидны, но всегда от симметрии структуры, от расположения атомов, от сил связи между ними зависит анизотропия свойств кристалла.
Особенно наглядна анизотропия механических свойств кристаллов. Кристаллы со слоистой структурой - слюда, гипс, графит, тальк - в направлении слоев совсем легко расщепляются на тонкие листочки, но невозможно разрезать или расколоть их в других плоскостях.
Бесцветные кристаллы каменной соли прозрачны, как стекло. А вот разбиваются они совсем не как стекло. Если ударить ножом или молоточком по кристаллу, он разбивается на кубики с ровными, гладкими, плоскими гранями. Это явление спайности, т. е. способности раскалываться по ровным, гладким плоскостям, так называемым плоскостям спайности. Кристаллы кальцита тоже обладают весьма совершенной спайностью: при ударе они всегда разбиваются на так называемые ромбоэдры с гладкими, плоскими гранями. Ромбоэдр - это косоугольный параллелепипед, или, можно сказать, куб, вытянутый вдоль одной из его диагоналей.
Спайность - это проявление анизотропии прочности кристаллов: силы сцепления между атомами в некоторых симметрично расположенных плоскостях очень малы, и кристаллы раскалываются по этим плоскостям.
Выводы
1. Представления о кристаллах, их строении и свойствах развивались на протяжении нескольких веков. Точкой отсчета истории кристаллов может быть известие о существовании изумрудов в Индии за 2 тыс. лет до н. э., алмазов за 1000-500 лет до н. э., рубинов Цейлона за 600 лет до н. э. Человек пытается разгадать природу кристалла с XIII-XIV веков н. э., а в середине XX века весь мир удивили жидкие кристаллы, в конце XX века сенсацией стало известие об открытии фотонных кристаллов. Чем более совершенными знаниями и инструментами исследования владеет человечество, тем более новые горизонты в познании природы и кристаллов, в частности, нам раскрываются.
2. В учебнике «Физика-10» (авторы: Г. Я. Мякишев, Б. Б. Буховцев, Н. Н. Сотский) на с. 193 дается определение кристаллов: кристаллы - это твердые тела, атомы или молекулы которых занимают определенные положения в пространстве. А далее следует фраза: поэтому кристаллы имеют плоские грани.
На основании наших исследований, мы можем утверждать, что это утверждение не совсем правильно, т. к. оно охватывает не все кристаллические образования. Доказательством этого служат так называемые «були».
3. Самый важный вывод нашей работы: все физические свойства, благодаря которым кристаллы так широко применяются, зависят от их строения - их пространственной кристаллической решетки.
ОТЧЕТ ГРУППЫ ЮВЕЛИРОВ
Цель: выяснить, почему человек издавна обращает внимание на некоторые кристаллы и называет их драгоценными, за какие их свойства и качества.
Задачи: выяснить толкование ювелирами терминов: самоцвет, драгоценный камень, полудрагоценный камень, поделочный камень, ювелирное украшение; проследить историю применения человеком ювелирных камней, их происхождение; изучить физические свойства кристаллов, благодаря которым они применяются в ювелирном деле и высоко ценятся: спайность, плотность, цвет, преломление света, дисперсия, спектры поглощения.
Основные понятия
Самоцвет, или д р а г о ц е н н ы й камень. Всю эту группу камней отличает одна объединяющая их черта - особая красота. Прежде самоцветами называли лишь немногие камни. Ныне число их резко возросло и продолжает увеличиваться. В большинстве своем это минералы, гораздо реже - минеральные агрегаты (горные породы). К драгоценным камням относят также некоторые материалы органического происхождения: янтарь, кораллы, жемчуг. Даже ископаемые органические останки (окаменелости) используются в качестве украшений. По своему назначению к драгоценным камням близок ряд других ювелирных материалов: дерево, кость, стекло и металл. Воспроизведение природных самоцветов путем синтеза, а также искусственное получение камней, не имеющих аналогов в природе, еще больше расширило многообразие драгоценных камней.
Для ношения пригодны, в первую очередь, твердые камни; камни помягче преимущественно оседают в коллекциях специалистов и любителей. Одни и те же минералы, различающиеся окраской или внешним строением, называют разновидностями драгоценных камней.
Полудрагоценный камень - понятие, пока еще бытующее в торговле, однако ввиду заложенного в нем умаляющего смысла употреблять его не следует. Прежде полудрагоценными называли менее ценные и не очень твердые камни, противопоставляя их «настоящим» драгоценным камням.
Учение о драгоценных камнях развилось в особую научную дисциплину - геммологию. Это часть науки о полезных ископаемых, охватывающая происхождение, строение, классификацию и обработку драгоценных камней.
Поделочный камень. Это собирательный термин, который относится ко всем камням, используемым как в качестве украшения, так и для производства камнерезных изделий. Иногда поделочными называют менее ценные или непрозрачные камни. На практике его часто применяют просто как синоним термина «драгоценный камень», ибо нет убедительных оснований для четкого разграничения «ювелирных» и «прочих» камней.
Ювелирное изделие. Под ювелирным изделием понимают украшение, состоящее из одного или нескольких драгоценных камней, оправленных в благородный металл. Иногда ювелирными изделиями называют и шлифованные камни без оправы, а также украшения из драгоценных металлов без камней.
Самоцветы и поделочные камни
Самоцветы известны человеку уже более семи тысячелетий. Первыми из них были: аметист, горный хрусталь, янтарь, нефрит, кораллы, лазурит, жемчуг, серпентин, изумруд и бирюза. Эти камни долгое время оставались доступными лишь представителям привилегированных классов и не только служили украшением, но и символизировали общественный статус их владельцев. Княжеские регалии, усеянные драгоценными камнями, свидетельствовали о богатстве и могуществе феодалов. И поныне в различных сокровищницах и музеях мы любуемся великолепными драгоценностями былых эпох.
Разумеется, и в наши дни находятся люди, которые надевают оправленный в золото или платину драгоценный камень, чтобы продемонстрировать свою состоятельность, но чаще ювелирные украшения служат нашему собственному удовольствию, доставляя радость своей красотой и гармонией.
Даже сегодня мы приобретаем тот или иной самоцвет, испытывая к нему какую-то непонятную симпатию или склонность. Поэтому неудивительно, что в прежние, менее просвещенные времена драгоценным камням приписывалась таинственная сила. Самоцветы служили амулетами и талисманами, якобы защищавшими от враждебных сил их обладателя и приносили ему счастье. Одни камни оберегали от зла, другие сохраняли здоровье, служили противоядием, спасали от чумы, вызывали милость владык или способствовали благополучному возвращению из плаванья.
Вплоть до начала XIX в. драгоценные камни использовали даже в лечебных целях. В одних случаях считалось достаточным иметь определенный камень, в других - его накладывали на больное место, в третьих - толкли в порошок и принимали внутрь. Старинные лечебники содержат «точные» сведения, какой камень может помочь от той или иной болезни. Лечение драгоценными камнями получило название литотерапии. Порой оно приносило успех, однако его следует приписывать не самому камню, а психологическому внушению, оказавшему благотворное действие на больного. Неудачи в лечении объяснялись тем, что камень оказался «ненастоящим». В Японии и сегодня в медицинских целях продаются таблетки из истолченных в порошок жемчужин (то есть в основном из углекислого кальция).
Прямым следствием бытовавшего представления о сверхъестественных силах, присущих драгоценным камням, явилась их связь с астрологией: их «приписывали» к зодиакальным созвездиям. Отсюда возникли «счастливые» камни рождения детей, то есть самоцветы, которые надлежало носить людям, рожденным под тем или иным знаком Зодиака. Эти камни должны всегда сопутствовать своим владельцам, якобы защищая их от всякого рода напастей. Впоследствии такие самоцветы стали «счастливыми» камнями месяцев. Равным образом существуют камни, которые связывают с Солнцем, Луной и планетами Солнечной системы. С течением времени «приписка» драгоценных камней неоднократно менялась. Совсем недавно некоторые страны избрали себе в качестве государственного символа драгоценный камень, добываемый на их территории.
И в современных религиях драгоценным камням отведено определенное место. Так, четырьмя рядами драгоценных камней украшен нагрудник иудейского первосвященника. Подобные камни сверкают на тиарах и митрах папы и епископов христианской церкви, а также на ковчегах, дароносицах, раках и окладах икон.
Но зачастую самоцветы рассматриваются исключительно как помещение капитала. И действительно, высокая стоимость драгоценных камней, заключенная в столь малую форму, доказала свою стабильность во всех экономических бурях последних десятилетий.
Меры массы драгоценных камней
Карат - единица массы, бытующая в торговле драгоценными камнями и в ювелирном деле с античных времен. Не исключено, что само слово «карат» происходит от местного названия (kuara) африканского кораллового дерева, семена которого использовались для взвешивания золотого песка, но более вероятно, что оно ведет начало от греческого названия (keration) широко распространенного в Средиземноморье рожкового дерева, плоды которого изначально служили «гирьками» при взвешивании драгоценных камней (масса одной гирьки в среднем примерно равна карату). В 1907 году Международным комитетом мер и весов на конференции в Париже был введен метрический карат, равный 200 мг, или 0,2 г. До этого масса карата, принятого в крупнейших центрах мировой торговли драгоценными камнями, несколько различалась. Отсюда расхождения в массе исторических алмазов, встречающихся в литературе. Сокращенное обозначение карата - кар. Доли карата выражают в виде простых или десятичных дробей. При взвешивании самых мелких алмазов используется также единица массы, называемая «пункт» и равная 0,01 карата. Не следует путать карат как единицу массы драгоценных камней с каратом как мерой чистоты (пробности) золота, употребляемой в ювелирном деле. В этом втором случае карат служит не единицей массы, а мерой качества золотого сплава. Чем больше число каратов, тем выше содержание чистого золота в ювелирном изделии, а масса его может быть при этом какой угодно.
Грамм - единица массы, используемая в торговле ювелирными камнями для менее дорогих камней, и особенно для необработанного камнецветного сырья (например, группы кварца).
Гран - мера массы жемчуга. Соответствует 0,05 г, то есть 0,25 кар. Сейчас гран все более вытесняется каратом. Употребляемая прежде в торговле жемчугом японская мера массы «момма» (= 3,75 г = 18,75 кар) теперь в европейской торговле практически не используется.
Цена. В торговле драгоценными камнями обычно указывается цена за 1 карат. Чтобы вычислить полную стоимость камня, надо перемножить цену и его массу в каратах. При продаже камня конечному потребителю обычно называется полная цена. Стоимость одного карата прогрессивно возрастает с увеличением размеров и массы камней: если, скажем, бриллиант-каратник (массой 1 кар) стоит определенную сумму, то двухкаратник (при том же качестве) оценивается не вдвое дороже, а гораздо выше.
Оптические свойства
В ряду физических свойств драгоценных камней оптические свойства играют главенствующую роль, определяя их цвет и блеск, сверкание, «огонь» и люминесценцию, астеризм, иризацию и прочие световые эффекты. При испытании и идентификации драгоценных камней также все большее место отводится оптическим явлениям.
Цвет
Цвет - первое, что бросается в глаза при взгляде на всякий драгоценный камень. Однако для большинства камней их цвет не может служить диагностическим признаком, так как многие из них окрашены одинаково, а некоторые выступают в нескольких цветовых обличиях.
Причиной различных окрасок является свет, то есть электромагнитные колебания, лежащие в определенном интервале длин волн. Человеческий глаз воспринимает только волны так называемого оптического диапазона - примерно от 400 до 700 нм. Эта область видимого света подразделяется на семь главных частей, каждая из которых соответствует определенному цвету спектра: красному, оранжевому, желтому, зеленому, голубому, синему, фиолетовому. При смешении всех спектральных цветов получается белый цвет. Если, однако, какой-либо интервал длин волн абсорбируется, из смеси остальных цветов возникает определенная - уже не белая - окраска. Камень, пропускающий все длины волн оптического диапазона, кажется бесцветным; если же, напротив, весь свет поглощается, то камень приобретает самую темную из видимых окрасок - черную. При частичном поглощении света по всему видимому диапазону волн камень выглядит мутно-белым или серым. Но если, наоборот, абсорбируются только вполне определенные длины волн, то камень приобретает окраску, соответствующую смешению оставшихся не поглощенными частей спектра белого света. Главными носителями цвета - хромофорами, обусловливающими окраску драгоценных камней, - являются ионы тяжелых металлов: железа, кобальта, никеля, марганца, меди, хрома, ванадия и титана, способные абсорбировать определённые длины волн в видимой области. Эти ионы часто присутствуют в столь малых количествах, что даже не находят отражения в химических формулах.
Окраска циркона и некоторых других минералов вызывается не ионами-хромофорами, а деформациями кристаллической решётки, точнее, возникновением в ней радиационных дефектов под воздействием радиоактивного излучения, что вызывает селективное (избирательное) поглощение света.
На поглощение света и тем самым на окраску кристалла влияет также длина пути, проходимого в нем световыми лучами. Соответственно, при шлифовке необходимо стремиться использовать это обстоятельство к максимальной выгоде для камня. Светлоокрашенные камни шлифуются более толстыми, а при огранке фасеты наносятся с таким расчетом, чтобы удлинить путь прохождения лучей сквозь камень, то есть усилить абсорбцию. Слишком темные камни, наоборот, следует шлифовать потоньше, чтобы несколько высветлить их. К примеру, темно-красный гранат-альмандин при шлифовке кабошоном высверливают с нижней стороны, чтобы сделать полым.
Цвет драгоценных камней зависит также от освещения, поскольку спектры искусственного (электрического) и дневного (солнечного) света различны. Существуют камни, на окраску которых искусственный свет оказывает неблагоприятное влияние (сапфир), и такие, которые при вечернем (искусственном) свете только выигрывают, усиливая свое сияние (рубин, изумруд). Но резче всего перемена цвета выражена у александрита: днем он выглядит зеленым, вечером - красным.
Несмотря на то, что для драгоценных камней цвет играет столь большую роль, практические способы его объективней оценки (кроме случая алмаза) не разработаны. Сравнительные таблицы цветов - лишь весьма скудный суррогат, оставляющий широкий простор для субъективных суждений. Применяемые в научном цветоведении измерительные методы для ювелирной промышленности и торговли чересчур сложны и требуют больших затрат.
Цвет черты
Цветовой облик драгоценных камней, относящихся к одной и той же группе минералов, может широко варьировать. Так, бериллы бывают всех цветов спектра, вплоть до бесцветных. Именно эта бесцветность и есть истинная, исходная, как говорят, собственная окраска берилла, отвечающая его химической формуле. Все другие цвета обусловлены присутствием посторонних примесных элементов - хромофоров. Собственные окраски, будучи постоянными, могут служить диагностическими признаками драгоценных камней. Если с нажимом провести камнем по пластинке неглазурованного шершавого фарфора-бисквита, то цвет оставленной на фарфоре черты выявит эту собственную окраску, так как тонко растертый порошок ведет себя в отношении оптических свойств подобно тончайшей просвечивающей пластинке минерала. Например, серо-стальной гематит дает вишнево-красную черту, латунно-желтый пирит -черную, голубой содалит - белую. При определении более твердых минералов рекомендуется сначала стальным напильником соскоблить немного порошка, а затем растереть его на бисквитной пластинке. Этот способ диагностики представляет собой интерес для коллекционеров. У ограненных камней во избежание их повреждения цвет черты определять не следует.
Светопреломление
Еще в детстве нам не раз приходилось видеть, что палка, под острым углом не до конца погруженная в воду, как бы «переламывается» у водной поверхности. Нижняя часть палки, находящаяся в воде, приобретает иной наклон, чем верхняя, находящаяся в воздухе. Это происходит вследствие преломления света, всегда проявляющегося при переходе светового луча из одной среды в другую, то есть на границе двух веществ, если луч направлен косо к поверхности их раздела.
Величина светопреломления всех кристаллов драгоценных камней одного и того же минерального вида постоянна (иногда она слегка колеблется, но в пределах весьма узкого интервала). Поэтому числовое выражение этой величины - показатель преломления (часто называемый просто преломлением или светопреломлением) - используется для диагностики драгоценных камней. Показатель преломления определяется как отношение скоростей света в воздухе и в кристалле. Дело в том, что отклонение светового луча в кристалле вызывается именно уменьшением скорости распространения этого луча в оптически более плотной среде.
Иными словами, в алмазе свет распространяется в 2,4 раза медленнее, чем в воздухе. Показатели преломления драгоценных камней находятся в интервале 1,2-2,6. В зависимости от цвета и месторождения драгоценного камня его преломление может несколько варьировать. Двупреломляющие камни имеют два или даже три показателя светопреломления.
Измерение показателей преломления на практике производится с помощью рефрактометра. Их значения непосредственно считываются со шкалы прибора. Однако на обычном рефрактометре можно измерять только показатели преломления не выше 1,80, притом лишь у камней, имеющих плоские грани или фасеты. Для кабошонов специалистам с помощью особых приемов удается получать приближенные данные.
Без больших технических трудностей и затрат можно измерять светопреломление иммерсионным методом - погружая камень в жидкости с известным показателем преломления и наблюдая границы раздела. По тому, насколько светлыми и резкими кажутся контуры камня или ребра между фасетами, а также по видимой ширине границ раздела можно довольно точно оценивать показатель преломления драгоценного камня.
Дисперсия
При прохождении сквозь кристалл белый свет не только испытывает преломление, но и разлагается на спектральные цвета, так как показатели светопреломления кристаллических веществ зависят (притом в разной степени) от длины волны падающего света. А поскольку отдельным цветам спектра белого света соответствуют разные длины волн, то они преломляются неодинаково. Скажем, у алмаза показатель преломления для красных лучей (длина волны 589 нм) - 2,417, для зеленых (длина волны 527 нм) - 2,427 и для фиолетовых (длина волны 397 нм) - 2,465. Явление разложения белого света кристаллом на все цвета радуги называется дисперсией.
Особенно велико значение цветовой дисперсии у алмаза, который именно ей обязан своей великолепной игрой цветов -знаменитым «огнем», составляющим главную прелесть этого камня.
Дисперсия бывает хорошо заметна только у бесцветных камней. Природные и синтетические камни с высокой дисперсией (например, фабулит, рутил, сфарлерит, титанит, циркон) используются в ювелирном деле как заменители алмаза. В качестве числовой меры дисперсии драгоценных камней обычно принимается разность показателей преломления для длин волн красной (линия В: 687 нм) и фиолетовой (линия G:430,8 нм) частей спектра.
Спектры поглощения
К числу важнейших средств диагностики драгоценных камней принадлежат спектры поглощения. Это разложенные на спектральные цвета полосы световых волн, выходящие из цветного камня. При прохождении сквозь кристалл определенные длины волн (то есть цветовые компоненты) света поглощаются, вследствие чего драгоценный камень и приобретает свой цвет (как результат сложения остаточных волн исходного белого цвета). Однако человеческий глаз не в состоянии различить все тонкие цветовые оттенки. Нам очень легко обмануться, приняв за драгоценный рубин такие похожие на него по цвету камни, как красный турмалин или красный гранат и даже красное стекло. Однако спектры поглощения (абсорбции) однозначно «разоблачают» эти камни или стекла, которыми, может быть, в самом деле пытались подменить рубин. Ведь большинство видов драгоценных камней имеет весьма характерный, присущий только данному виду спектр абсорбции, отличающийся от спектров других камней числом и расположением вертикальных черных линий или широких полос поглощения.
Особое преимущество этого метода исследования состоит в том, что он позволяет однозначно диагностировать камни одинаковой плотности и близкие по светопреломлению. Метод в равной мере пригоден для определения необработанных камней, кабошонов и даже ограненных камней, вставленных в оправу. Все более широкое приложение метод находит при отделении природных камней от искусственных и от их имитаций.
Наилучшие результаты этот метод дает применительно к интенсивно окрашенным прозрачным цветным камням. Спектры поглощения непрозрачных камней могут быть получены на очень тонких и потому пропускающих свет срезах (как в случае гематита), а также на просвечивающих краях или же с помощью света, отраженного от поверхности камня.
Прибором для наблюдения спектров служит спектроскоп. Он позволяет устанавливать длины волн погашенного, то есть поглощенного света. Единицей измерения длин волн служит нанометр; еще недавно для этой цели использовался, а потому часто встречается в литературе ангстрем. Ввиду того, что линии и полосы поглощения не всегда бывают выражены одинаково четко, принято указывать различия в их интенсивности особыми пометами, относящимися к числовым значениям соответствующих длин волн.
Выводы
После проработки понятий: драгоценный камень, полудрагоценный, самоцвет, поделочный камень - мы пришли к выводу, что в настоящее время нет убедительных оснований для разграничения этих понятий.
Что касается происхождения всех драгоценных камней, то они принадлежат миру минералов, т. е. выращены природой в недрах Земли из растворов, расплавов или путем перекристаллизации. Химический состав таких кристаллов выражается формулой. Отношение человека к драгоценным камням за многие столетия претерпело изменения: от обожествления и применения в медицине до демонстрации своей состоятельности или доставления эстетического удовольствия от красоты и гармонии камня.
Все физические свойства учитываются при изготовлении ювелирных украшений:
спайность - при дроблении и распилке больших кристаллов;
плотность и твердость - при обработке и шлифовке;
оптические свойства: цвет, преломление, дисперсия - при огранке камней.
Именно оптические свойства в ювелирных украшениях наиболее ценны.
ОТЧЕТ ГРУППЫ ЭКСПЕРИМЕНТАТОРОВ
Цели: выращивание кристаллов и наблюдение за процессом их роста.
Задачи: рассмотреть промышленные и лабораторные способы выращивания кристаллов и выбрать способ, приемлемый для выращивания кристаллов в домашних условиях; по мере роста кристаллов соотносить свои наблюдения с закономерностями, известными из теории кристаллов; сравнить формы выращенных кристаллов с формами их кристаллических решеток.
Методы выращивания кристаллов
Первым монокристаллом, полученным в лаборатории, был, наверное, рубин. Д. И. Менделеев не мог пройти мимо такого важного события и в примечаниях к тексту своих «Основ химии» писал: «Фреми (1890) получил прозрачные рубины, кристаллизующиеся в ромбоэдрах и не отличающиеся по своей твердости, цвету, величине и другим свойствам от природных. Для получения рубина накаливалась смесь безводного глинозема, содержавшего большую или меньшую примесь едкого калия, с фтористым барием и двухромокалиевой солью. Последняя прибавляется для того, чтобы вызвать окраску рубина, и берется в незначительном количестве (самое большее до 4 вес. ч. на 100 ч. окиси алюминия). Смесь помещается в тигель из глины и накаливается (от 100 часов до 8 суток) в отражательных печах при температуре до 1500°. По окончании опыта в тигле оказывается кристаллическая масса, причем стенки покрыты кристаллами рубина прекрасного розового цвета. Для реакции оказывается необходимым доступ влажного воздуха. Образование при этом рубина может быть объяснено, по Фреми, происхождением фтористого алюминия, который под влиянием влажного воздуха при высокой температуре дает рубин и фтористый водород». Здесь же автор «Основ химии» упомянул и другие способы: «В жару электрических печей или при температуре, достигаемой при горении А1 с Fe203, т. е. около 3000°, глинозем легко плавится и дает иногда кристаллы, тождественные с рубином». В 31-м томе словаря Брокгауза - Ефрона (1895), в статье «Корунд», утверждается, что некоторое время «в торговле обращались красивые карминово-красные рубины значительной величины, несомненно, искусственно полученные, однако ни об ав торе, ни о способе получения ничего не известно». Согласно современным представлениям, рубин - это кристалл АЬОз с примесью Сг и Fe, а камни, о которых писали в Брокгаузе и Ефроне, появились на рынке в 1885 году и действительно были получены искусственно. В настоящее время существует ряд способов изготовления синтетических камней.
Синтез драгоценных ювелирных и технических камней по способу М. А. Вернейля считается классическим и является первым промышленным методом выращивания кристаллов корунда, шпинели и других синтетических кристаллов. В мире ежегодно выпускается около 200 т синтетического корунда и шпинели. Метод Вернейля заключается в следующем: к горелке с направленным вниз соплом через внешнюю трубу подводится водород, а через внутреннюю - кислород. В ток кислорода попадается измельченный порошок окиси алюминия зернистостью около 20 мкм, полученный прокаливанием алюмоаммиачных квасцов, который при этом нагревается до определенной температуры и затем попадает в водородно-кислородное пламя гремучего газа, где он расплавляется. Внизу под соплом располагается стержень из спеченного корунда, выполняющего роль кри-сталлоносца. На него стекает расплавленная окись алюминия, образуя шарик расплава. Стержень кристалл о нос ца постепенно опускается со скоростью 5-10 мм/ч, при этом обеспечивается постоянное нахождение расплавленной растущей части корунда в пламени. На рисунке показана принципиальная схема установки для выращивания кристаллов этим методом.
Диаметр образовавшихся кристаллов (булек) обычно достигает 20 мм, длина 50-80 мм, иногда их размеры гораздо больше. Бульки представляют собой поликристаллы. Для получения монолитного монокристалла бульку оплавляют путем подачи кислорода. При этом на оплавленной поверхности бульки часть кристаллов остается не разрушенной и они при последующем охлаждении бульки начинают расти за счет оплавленных разрушенных кристаллов. Для получения рубина к порошку окиси алюминия добавляют окись хрома, для синтеза сапфира – окись железа и титана, для синтеза александритоподобного корунда - соли ванадия. Этим же методом выращивают синтетический рутил и титанат стронция.
Второй распространенный метод выращивания синтетических кристаллов драгоценных камней - способ Чохральского. Он заключается в следующем: расплав вещества, из которого предполагается кристаллизовать камни, помещают в огнеупорный тигель из тугоплавкого металла (платины, родия, иридия, молибдена или вольфрама) и нагревают в высокочастотном индукторе. В расплав на вытяжном валу опускают затравку из материала будущего кристалла, и на ней наращивается синтетический материал до нужной толщины. Вал с затравкой постепенно вытягивают вверх со скоростью 1-50 мм/ч с одновременным выращиванием при частоте вращения 30-150 об/мин. Вращают вал, чтобы выровнять температуру расплава и обеспечить равномерное распределение примесей. Диаметр кристаллов - до 50 мм, длина - до 1 м. Методом Чохральского выращивают синтетический корунд, шпинель, гранаты, ниобат лития и другие искусственные камни.
Часто применяется метод кристаллизации из раствора в расплаве с использованием флюсов. При этом камни кристаллизуются из смешанного расплава, состоящего из раствора соединения и флюсов - молибдатов, боратов, фторидов, окиси свинца и др. Кристаллизуют вещества обычно в платиновом тигле при температуре от 600 до 1300 °С (в зависимости от вида кристаллов). В расплав опускают затравку, а затем его охлаждают со скоростью 0,1-1 °С/ч. На затравке постепенно наращивается кристалл. Скорость роста невелика - за несколько недель кристалл вырастает на 3-4 см. Этот метод по эффективности не может конкурировать со способом Чохральского и применяется в тех случаях, если кристалл плавится инконгруэнтно или испытывает деструктивное фазовое превращение в твердом состоянии. Очень эффективен гидротермальный способ выращивания кристаллов драгоценных камней. Процесс осуществляется в автоклавах при давлении 7Т0000000-14Т0000000 Па и темпера туре 300-900 °С. Автоклав заполняют раствором соответствующего минерала. В нижней части автоклава температура более высокая; когда насыщенный раствор поднимается вверх и попадает в условия с пониженной температурой, вещество осаждается на затравку природного кристалла. Нижняя и верхняя части автоклава разделены диафрагмой. Последние два метода применяют для выращивания синтетических изумрудов, бериллов. Гидротермальным методом синтезируют разновидности кварца и корунда, а методом флюса - иттрий-алюминиевые гранаты, корунды, шпинель.
Сверхтвердые синтетические минералы и материалы получают другими способами. Для выращивания алмаза необходимы давление 50-100000000-100-100000000 Па и температура более 1600 °С. Процесс синтеза алмазов осуществляется из графита в присутствии катализаторов - металлов. В зависимости от времени синтеза получают кристаллы алмазов различных размеров. Такими же методами синтезируют другие сверхтвердые материалы: гексанит, эльбор, СВ и другие, которые широко применяются в технике. В ювелирном деле синтетические алмазы и сверхтвердые материалы до сих пор не применяются.
Охлаждение насыщенного горячего раствора.
![]() При каждой температуре в данном количестве растворителя (например, в воде) может раствориться не более определенного количества вещества. Например, в 100 г воды при 90 °С может раствориться 200 г алюмокалиевых квасцов. Такой раствор называется насыщенным. Будем теперь охлаждать раствор. С понижением температуры растворимость большинства веществ уменьшается. Так, при 80 °С в 100 г воды можно растворить уже не более 130 г квасцов. Куда же денутся остальные 70 г? Если охлаждение вести быстро, избыток вещества просто выпадет в осадок. Если этот осадок высушить и рассмотреть в сильную лупу, то можно увидеть множество мелких кристалликов. При охлаждении раствора частички вещества (молекулы, ионы), которые уже не могут находиться в растворенном состоянии, слипаются друг с другом, образуя крошечные кристаллы-зародыши. Образованию зародышей способствуют примеси в растворе, например, пыль, мельчайшие неровности на стенках сосуда (химики иногда специально трут стеклянной палочкой по внутренним стенкам стакана, чтобы помочь кристаллизации вещества). Если раствор охлаждать медленно, зародышей образуется немного, и, обрастая постепенно со всех сторон, они превращаются в красивые кристаллики правильной формы. При быстром же охлаждении образуется много зародышей, причем частички из раствора будут «сыпаться» на поверхность растущих кристалликов, как горох из порванного мешка; конечно, правильных кристаллов при этом не получится, потому что находящиеся в растворе частицы могут просто не успеть «устроиться» на поверхности кристалла на положенное им место. Кроме того, множество быстро растущих кристалликов так же мешают друг другу, как несколько паркетчиков, работающих в одной комнате. Посторонние твердые примеси в растворе также могут играть роль центров кристаллизации, поэтому чем чище раствор, тем больше шансов, что центров кристаллизации будет немного. Охладив насыщенный при 90 °С раствор квасцов до комнатной температуры, мы получим в осадке уже 190 г, потому что при 20 °С в 100 г воды растворяется только 10 г квасцов. Получится ли при этом один большой кристалл правильной формы массой 190 г? К сожалению, нет: даже в очень чистом растворе вряд ли начнет расти один-единственный кристалл: масса кристалликов может образоваться на поверхности остывающего раствора, где температура немного ниже, чем в объеме, а также на стенках и дне сосуда. Метод выращивания кристаллов путем постепенного охлаждения насыщенного раствора неприменим к веществам, растворимость которых мало зависит от температуры. К таким веществам относятся, например, хлориды натрия и алюминия, ацетат кальция.
При каждой температуре в данном количестве растворителя (например, в воде) может раствориться не более определенного количества вещества. Например, в 100 г воды при 90 °С может раствориться 200 г алюмокалиевых квасцов. Такой раствор называется насыщенным. Будем теперь охлаждать раствор. С понижением температуры растворимость большинства веществ уменьшается. Так, при 80 °С в 100 г воды можно растворить уже не более 130 г квасцов. Куда же денутся остальные 70 г? Если охлаждение вести быстро, избыток вещества просто выпадет в осадок. Если этот осадок высушить и рассмотреть в сильную лупу, то можно увидеть множество мелких кристалликов. При охлаждении раствора частички вещества (молекулы, ионы), которые уже не могут находиться в растворенном состоянии, слипаются друг с другом, образуя крошечные кристаллы-зародыши. Образованию зародышей способствуют примеси в растворе, например, пыль, мельчайшие неровности на стенках сосуда (химики иногда специально трут стеклянной палочкой по внутренним стенкам стакана, чтобы помочь кристаллизации вещества). Если раствор охлаждать медленно, зародышей образуется немного, и, обрастая постепенно со всех сторон, они превращаются в красивые кристаллики правильной формы. При быстром же охлаждении образуется много зародышей, причем частички из раствора будут «сыпаться» на поверхность растущих кристалликов, как горох из порванного мешка; конечно, правильных кристаллов при этом не получится, потому что находящиеся в растворе частицы могут просто не успеть «устроиться» на поверхности кристалла на положенное им место. Кроме того, множество быстро растущих кристалликов так же мешают друг другу, как несколько паркетчиков, работающих в одной комнате. Посторонние твердые примеси в растворе также могут играть роль центров кристаллизации, поэтому чем чище раствор, тем больше шансов, что центров кристаллизации будет немного. Охладив насыщенный при 90 °С раствор квасцов до комнатной температуры, мы получим в осадке уже 190 г, потому что при 20 °С в 100 г воды растворяется только 10 г квасцов. Получится ли при этом один большой кристалл правильной формы массой 190 г? К сожалению, нет: даже в очень чистом растворе вряд ли начнет расти один-единственный кристалл: масса кристалликов может образоваться на поверхности остывающего раствора, где температура немного ниже, чем в объеме, а также на стенках и дне сосуда. Метод выращивания кристаллов путем постепенного охлаждения насыщенного раствора неприменим к веществам, растворимость которых мало зависит от температуры. К таким веществам относятся, например, хлориды натрия и алюминия, ацетат кальция.
Самый простой способ - испарение растворителя.
Установка представляла собой сосуд из органического стекла емкостью около 750 мл. В него налито примерно 600 мл насыщенного раствора медного купороса. По мере испарения в сосуд подливались новые порции раствора. Поэтому стенки не смачивались раствором и кристаллы-паразиты на них почти не появлялись. Первоначально из полукристаллической массы медного купороса мы отобрали семь кристалликов более или менее правильной формы. Каждый был опущен на тонкой (0,15 мм) лесе в сосуд с насыщенным раствором медного купороса. По мере роста удалялись неудачные кристаллы, обросшие паразитами и потерявшие типичную для монокристаллов медного купороса форму. Через две недели осталось только три лучших кристалла, а через месяц - всего один. Он был уже довольно велик, поэтому линейный рост его замедлился из-за большой поверхности кристаллизации. Вместо обычных в таких случаях перемешиваний раствора мы решили вращать сам кристалл. Для этого подвесили его на лесе, конец которой укрепили на оси электродвигателя. За 10-12 секунд работы двигателя леса закручивалась настолько, что после закрепления оси обеспечивала медленное вращение монокристалла в течение получаса. Пожалуй, проще было бы просто перемешивать раствор, вращающийся от микроэлектродвигателя мешалкой. В течение всего времени эксперимента сосуд был прикрыт целлофаном, чтобы в него не попадала пыль.
Несколько необычно мы получили второй кристалл. Во время более интенсивного испарения (при понижении относительной влажности и повышении температуры) возникало большое перенасыщение. Пока сам кристалл был мал, его рост не мог скомпенсировать испарение. Поэтому на неровностях лесы начинали расти кристаллы-паразиты. Один из них нам так понравился, что мы вырастили его отдельно. В этом случае не было затравки, внесенной в раствор извне, весь кристалл был выращен в нашем растворе. Полученный кристалл имел более правильную форму, так как он был свободен от дефектов затравки.
Для изготовления трехгранных призм спектрографов, позволяющих вести исследования в ультрафиолетовой части спектра, выращиваются крупные бочкообразные кристаллы поваренной соли. Способ выращивания таких кристаллов разработан С. Киропулосом.
Она состоит из вертикальной цилиндрической электропечи, в которую помещен большой тигель с расплавом чистой соли. В расплаве устанавливается постоянная температура на 50-60° выше температуры плавления соли. Сверху в расплав медленно, чтобы она успела прогреться, опускают затравку, вырезанную из кристалла той же соли. После соприкосновения затравки с расплавом и частичного оплавления ее держатель охлаждается струей воздуха, проходящей по трубке внутри его. Затравка и примыкающий к ней слой расплава охлаждаются, и кристалл начинает расти в виде сферы или шляпки перевернутого гриба. Когда ширина разросшейся сферы станет достаточно большой, специальный механизм начнет медленно поднимать затравку с нарастающим на нее бочкообразным кристаллом, не давая ему соприкоснуться со стенками. Выращенный кристалл быстро переносят в другую печь, нагретую вначале почти до температуры плавления соли, где кристалл медленно охлаждается до комнатной температуры. Кристалл весом 15-20 кг удается вырастить за 10-15 часов. Этим способом помимо поваренной соли выращивают кристаллы хлористого калия и других солей с температурой плавления до 1000°. Установки С. Киропулоса удобны тем, что в конце выращивания кристалл свободен от тигля, но это является и недостатком ее.
Кристаллы при высокой температуре обладают заметной пластичностью. В результате этого поднятый над расплавом под действием собственного веса он слегка провисает, деформируется, что нарушает однородность его кристаллографического строения.
Технология выращивания кристаллов в домашних условиях
Чтобы вырастить кристаллы в домашних условиях, нужно приготовить перенасыщенный раствор соли. В качестве исходных веществ мы выбрали те соли, которыми пользуется человек более или менее часто: медный и железный купорос (для обработки растений от вредителей) и поваренную соль (для употребления в пищу).
В чистую посуду наливаем горячую воду при температуре 50 °С, объем доводим до 500 мл. В стакан небольшими порциями засыпаем вещество, каждый раз перемешивая и добиваясь полного растворения, как только раствор «насытится», его нужно накрыть и оставить в помещении, где должна сохраняться постоянная температура. По мере остывания раствора до комнатной температуры возникает избыточная кристаллизация. В растворе вещества остается ровно столько, сколько соответствует растворимости при данной температуре, а лишнее выпадает на дно в виде маленьких кристалликов. Так мы получим маточный раствор.
Далее мы сливаем маточный раствор в другую чистую посуду, туда же помещаем кристаллики со дна, нагреваем посуду на водяной бане, добиваясь полного растворения, и даем охладиться. На этом этапе нашему раствору не желательны сквозняки и резкие перепады температуры. Через сутки осматриваем содержимое и замечаем, что на дне и стенках образовались небольшие плоские кристаллики-параллелограммы. Из них мы отбираем небольшой, но наиболее правильный кристалл. Его мы привязываем на тонкую леску и крепим к крышке банки.
Снова готовим насыщенный раствор на основе исходного маточного, добавляем еще немного (0,5чайной ложки) вещества, греем и перемешиваем. Раствор необходимо перелить в чистую и нагретую посуду и дать ему постоять 20-30 секунд, чтобы жидкость немного успокоилась. Если раствор теплый, дадим ему остыть до 30 °С, т. к. лишние градусы могут вызвать растворение самой затравки. Кристалл-затравку опускаем в центр раствора, при этом затравка должна «висеть», не касаясь дна и стенок сосуда. Теперь осталось только наблюдать за ростом. Наш кристалл-затравка играет в растворе роль центра кристаллизации. Наблюдение за ростом кристаллов
Эту технологи мы применили для выращивания трех кристаллов: медного, железного купороса и поваренной соли. Наблюдали за ростом каждый день. Изучив литературу, мы знали, что вырастить монокристалл очень сложно. Для этого нужно строго соблюдать все условия технологии, начиная со специальной посуды, чистоты раствора и заканчивая соблюдением строжайшего температурного режима. Но мы занимались экспериментальной работой в зимнее время, раствор очень быстро остывал, поэтому поддерживать температуру постоянной не удавалось. Также приходилось периодически подогревать содержимое и добавлять еще вещества в раствор. Все эти отклонения от технологии привели к тому, что кристаллы выросли сросшимися, т. е. у нас получились поликристаллы с ярко выраженными плоскими гранями отдельных кристаллов (см. рис.).
Не меняя положение затравки, мы периодически измеряли размеры некоторых граней и заметили следующее: грани изменяют свои размеры - растут, но форма их остается неизменной, углы между соответственными гранями тоже остаются постоянными. Но, возможно, эта закономерность характерна только данному кристаллу? Поэтому мы вырастили два разных кристалла медного купороса, сравнили формы граней и измерили их углы. Оказалось, что и для другого кристалла эта закономерность тоже справедлива. Это дает право говорить о том, что в различных кристаллах одного и того же вещества и форма граней, и их взаимные расстояния, и их число могут изменяться, но углы при этом остаются постоянными.
Исследование физических свойств кристаллов
Конечно, не все физические свойства можно исследовать в домашних условиях, но такие, как анизотропность и спайность, -можно. Причем получилось у нас это почти случайно. Когда мы продумывали свою работу, то задачу исследовать физические свойства перед собой не ставили, т. к. знали, что это будет сделать трудно. Нам помог случай. Выскользнув из рук, кристалл медного купороса упал на пол и раскололся на множество маленьких кристалликов. Тщательное изучение осколков показало, что они представляют собой одинаковой формы геометрические тела, отличающиеся только размерами. Отсюда напрашивается вывод, что один большой поликристалл при механическом воздействии может дробиться на части, ограниченные плоскими поверхностями, пересекающимися под острыми и тупыми углами (если прямоугольный параллелепипед растянуть по диагонали, то получим примерную форму таких осколков). Поперек этих поверхностей заставить разрушаться кристалл очень трудно. Способность кристалла раскалываться в определенных направлениях называется спайностью. Это свойство используется тогда, когда большой кристалл нужно раздробить (расчленить) на несколько небольших.
А затем мы исследовали самые крупные кристаллы на теплопроводность, т. е. как они проводят тепло.
Мы наносили каплю парафина на разные грани кристаллов и давали ей застыть. Затем дотрагивались до этих граней хорошо прогретой спицей и наблюдали за формой таявшей капельки парафина. В одних случаях форма была круглая, а в других - вытянутая, а это значит, что в первом случае тепло распространялось по всем направлениям одинаково, а во втором - тепло распространялось в одних направлениях медленнее, в других быстрее и форма проталинки была уже не круглой. Если подобный эксперимент провести с поликристаллом, то никакой разницы в форме проталинки не будет, а следовательно, поликристаллы одинаково проводят тепло по всем направлениям.
Исследовать другие физические свойства мы не смогли из-за ограниченности материально-технической базы нашего учебного заведения.
Еще одна задача стояла перед нами. Сравнить формы полученных кристаллов с формами их кристаллических решеток. Нам это удалось сделать только для кристаллов поваренной соли. В литературе мы нашли модель кристаллической решетки NaCl, согласно которой грани должны иметь форму квадратов, а кристаллы - кубов. Выращенный нами кристалл соответствует этим требованиям и относится к кубической сингонии - куб (гексаэдр).
Но нам не удалось найти формы решеток медного и железного купороса. Мы воспользовались предыдущим соответствием формы кристалла и его решетки и предположили следующее: основываясь на исследованиях фотографий выращенных кристаллов, можем утверждать, что форма монокристаллов медного купороса соответствует ромбоэдру (средние сингонии), а форма монокристаллов железного купороса соответствует ромбической призме (низшие сингонии).
Выводы
Все физические свойства, благодаря которым кристаллы так широко применяются, зависят от их строения - их пространственной решетки.
Наряду с твердотельными кристаллами в настоящее время широко применяются жидкие кристаллы, а в скором будущем мы будем пользоваться приборами, построенными на фотонных кристаллах.
К кристаллам относятся и ювелирные камни, из которых изготавливают украшения. Отношение человека к драгоценным камням за многие столетия претерпело изменения: от обожествления и применения в медицине до демонстрации своей состоятельности или доставления эстетического удовольствия от красоты и гармонии камня.
Мы отобрали наиболее приемлемый способ для выращивания кристаллов в домашних условиях и вырастили кристаллы медного и железного купороса, а также кристаллы поваренной соли. По мере роста кристаллов проводили наблюдения. Определили типы кристаллических решеток для медного и железного купороса.