Тема урока: «Решение задач на растворы и сплавы»
Цель урока: учащиеся будут применять приемы решения текстовых задач на растворы и сплавы.
Цель урока: Рассмотреть различные типы задач на растворы и приемы их решения.
образовательные:
- познакомиться с приемами решения задач в математике и химии;
- сформировать целостную картину о взаимосвязи предметов в школе;
Воспитательные задачи: совершенствовать интеллектуальные умения (анализ, прогнозирование, умения устанавливать причинно-следственные связи)
Задачи развития учащихся: продолжить формирование ценностного отношения к исследовательской деятельности как основному способу получения знаний в химии; создать условия для развития умений наблюдать и объяснять химические явления, умений анализировать результаты наблюдаемых опытов, грамотного химического языка, коммуникативных умений, самостоятельности в мышлении и учебной работе; формирование навыков самоконтроля и самооценки, навыков работы с реактивами.
Технологии:
Традиционные – проблемно-поисковый метод, выполнение эксперимента, работа с инструкционной картой.
Инновационные – ИКТ.
Тип урока:
Комбинированный урок
Краткое описание:
Интегрированный урок математика + химия на тему: «Решение задач на сплавы растворы»
Ход урока.
Организационный момент.
Учитель математики: Сегодня у нас необычный урок, это интегрированный урок математики и химии и вести его будут два учителя. На этом уроке мы посмотрим с вами на задачи с двух точек зрения – с химической и математической, и выясним: как математика помогает в решении химических задач и как химия решает некоторые математические задачи.
Учитель химии: Здравствуйте, ребята! Мы с вами увидим, как применить математические методы при решении задач по химии.
Тема урока: Решение задач на растворы и сплавы.
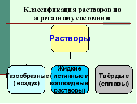
Учитель химии: Какие бывают растворы?
Ответ: Жидкие, твердые, газообразные по агрегатному состоянию. Насыщенные и ненасыщенные по растворимости веществ в воде. Истинные и коллоидные по размеру частиц.
Учитель химии: как выражают концентрацию раствора?
Какие существуют способы выражения концентрации растворов?
Ответ: массовая доля (w) и молярная концентрация раствора (См). Дать определения.
Ученик: w, mр.в., См, mр-ра, nр.в., Vр-ра
Учитель математики: А с математической точки зрения - разное процентное содержание вещества.
Итак, тема урока « Решение задач на сплавы и растворы».
Цель урока: Рассмотреть алгоритм решения задач на растворы, познакомить с приемами решения задач в математике и химии, расширить знания о значении этих растворов в быту, сформировать целостную картину о взаимосвязи предметов в школе.
Девиз: «Только из союза двух работающих вместе и при помощи друг друга рождаются великие вещи» Антуан де Сент- Экзюпери
Учитель математики: Для урока необходимо повторить понятие процента.
1 этап. Актуализация понятия процента.
Математическая разминка (проводит учитель математики).
Вспомним проценты: - Что называют процентом? (1/100 часть числа.)
- Выразите в виде десятичной дроби 17%, 40%, 6%
- Выразите в виде обыкновенной дроби 25%, 30%, 7%
- Установите соответствие 40% 1/4
25% 0,04
80% 0,4
4% 4/5
Как найти % от числа? (% записать в виде дроби, умножить число на эту дробь.)
- Найти 10% от 30 (10%=0,1 30*0,1=3)
- Вычислите 1) 20% от 70 2) 6% от 20
3) х% от 7
- Найти 30% от 2430 (729)
- Сколько % составит 12 от 60? (20%)
- Найдите число, 20% которого равны 42 (210)
- Какое число, увеличенное на 11% составит 222? (200)
- На сколько % число 180 больше числа 108? (40%)
- На сколько % число 120 меньше числа 150? (20%)
- В бронзе – сплаве меди с оловом, на долю олова приходится 20%. Сколько весит олово, пошедшее на создание Медного всадника, если масса памятника 5 тонн? (1 тонна)
- Найти массу 25% раствора, в котором растворено 80 г вещества. (320 г)
- Какова массовая доля раствора, при выпаривании 300 г которого получено 30 г соли? (10%)
- Рассчитать массовую долю раствора, полученного растворением 20 кг щелочи в 80 кг воды. (20%)
2 этап. Проверка домашнего задания. Бенефис одной задачи.
Цель: на данном этапе урока учащиеся демонстрируют оригинальные способы решения задач, полученных предварительно на дом.
1 группа.
Сплав алюминия и цинка содержит 82% алюминия. После добавления 18кг цинка содержание алюминия в сплаве понизилось до 70%. Вычислите, сколько алюминия и цинка в отдельности содержится в сплаве.
Ответ: 81,6кг. 36,9кг
2 группа.
Сплав состоит из меди и цинка. В первом куске меди содержится 60% и цинка 40%, а во втором это соотношение равно 7:3 Сколько следует взять от каждого куска, чтобы получить 1кг нового сплава, в котором медь и цинк находились бы в соотношении 11:5?
Ответ: 125г 875г
3группа.
Два слитка состоят из меди, цинка и олова. В первом слитке 40% олова, во втором 26% меди. Процентное содержание цинка в первом и во втором слитке одинаковое. Сплавив 150г первого и 250г второго, получили новый сплав, в котором оказалось 30% цинка. Сколько граммов олова содержится в новом сплаве.
Ответ: 170г
4 группа.
В одной тонне руды содержится определенное количество железа. После удаления из руды 400кг примесей, содержащих 12,5% железа, в оставшейся руде содержание железа повысилось на 20%. Какое количество железа осталось в руде?
Ответ: 375кг
3 этап урока. Методы решения задач на растворы и сплавы.
Учащиеся работаю в 4 группах.
Практическая работа: «Приготовление раствора заданной концентрации».
Первой группе учащихся было предложено задание: приготовить 250мл 3% раствора глюкозы из 5% раствора глюкозы.
Оборудование: калькулятор, пипетка на 10мл, мерный цилиндр, колба с дистиллированной водой, раствор глюкозы 5%.
Этапы практической работы:
1. Постановка вопроса, обусловливающего цель работы.
2. Инструктаж технический и организационный.
3. Выполнение работы (определение, наблюдение, постановка опыта).
4. Фиксация результатов (проводится одновременно с выполнением работы).
5. Выводы, отвечающие на поставленный вопрос.
Отчет учащихся:
Было получено задание: приготовить 250мл 3% раствора глюкозы из 5% раствора глюкозы. Плотность растворов глюкозы считаем равной 1г\мл.
Проведены расчеты по формуле массовая доля вещества – это отношение массы вещества к массе раствора. Найдена масса 250мл раствора по плотности. Найдена масса вещества в 250г 3% раствора. Рассчитана масса 5% раствора глюкозы – 150г.
С помощью мерного цилиндра отмерили 150мл раствора глюкозы (плотность равно 1г\мл). В колбу для приготовления растворов на 250мл через воронку прилили 150мл раствора глюкозы и довели объем до метки. Использовали дистиллированную воду.
Результат: получен 3% раствор.
Было получено задание: в пипетку на 10 мл набрать 40% раствор глюкозы. Приготовить раствор в колбе на 500 мл. Рассчитать концентрацию полученного раствора.
Проведен расчет. В 10мл раствора масса глюкозы составляет 4г. Масса раствора 500г (учитываем, что плотность раствора глюкозы 1г\мл. Концентрация глюкозы 0,8%.
Было получено задание: в пипетку на 10 мл набрать 40% раствор глюкозы. Приготовить раствор в колбе на 250 мл. Рассчитать концентрацию полученного раствора.
Проведен расчет. В 10мл раствора масса глюкозы составляет 4г. Масса раствора 250г (учитываем, что плотность раствора глюкозы 1г\мл. Концентрация глюкозы 1,6%.
Было получено задание: приготовить 15% раствор из 5% и 40%.
Используем конверт Пирсона для расчета частей растворов. Растворы смешиваем в соотношении 5:2. В пипетку наберем 10мл 40% раствора и отмерим 25мл 5% раствора. При смешивании получим 35мл 15% раствора.
Группа 2. Определение массовой доли редуцирующих веществ методом Лейна – Эйлона
Цель: установить концентрацию раствора глюкозы с помощью метода Лейна-Эйлона.
Фактором раствора Фелинга называют число, соответствующее объему в куб.см раствора глюкозы, затраченному на титрование 25см смеси растворов Фелинга.
Предварительное титрование
В плоскодонную колбу вместимостью на 100 см куб. пипеткой вносят 25 см куб. смеси растворов Фелинга, перемешивают на магнитной мешалке или вручную. Смесь доводят до кипения на электрической плитке, кипятят 2мин и из бюретки вносят стандартный раствор глюкозы. Снова нагревают колбу, раствор кипятят 2мин, затем добавляют 2-4 капли метиленовой сини, а из бюретки дотитровывают, по каплям до перехода окраски индикатора из синей в бесцветную. Отмечают объем, пошедший на титрование. Титрование проводят 3 раза, вычисляют среднее арифметическое. Это число является фактором раствора Фелинга.
Группа 3. Определение глюкозы с помощью глюкометра «GAMMA».
Вставьте тест полоску в приемник глюкометра лицевой стороной вверх и контактами вперед. Контакты должны полностью пройти, чтобы результат был точным. Прибор включается автоматически, на дисплее появляется символ капли крови. Каплю объемом 0,5 микролитра исследуемого раствора глюкозы нанесем на предметное стекло и поднесем к ней абсорбирующий участок на тест полоске. (Не трите тест полоску пальцами и не используйте загрязненные тест полоски). Жидкость должна полностью заполнить контрольное окошко перед тем как глюкометр начнет отсчет. Результаты измерений появляются на дисплее после того, как глюкометр закончит отсчет.
Диапазон измерений: 1,1-33,3 ммоль\литр
Группа 4. Разработка рецептуры коктейла.
Цель: разработать рецептуру коктейля.
Для приготовления коктейла мы использовании пломбир классический торговой марки «Золотой стандарт», жирность 15% и молоко жирность 6%.
Расчет: если смешать молоко и мороженое в соотношении 1:1, то получится коктейл жирностью 28%.
В блендере с чашей емкостью 2л смешиваем 1л мороженого и 1л 6% молока.
Готовый коктейл разливаем по стаканчикам на 200мл. Выходит 20 порций.
Задача №1. Какую массу молока 6%-й жирности и пломбира 50%-й жирности необходимо взять для приготовления 100г 28%-го новогоднего коктейля?
Решение:
%-е содержание
Масса раствора (г)
Масса вещества (г)
Молоко
Пло
бир
6%=0,06
50%=0,5
х
100-х
0,06х
0,5(100-х)
Коктейль
28%=0,28
100
0,28*100
0,06х + 0,5(100-х) = 0,28*100
0,06х + 50 – 0,5х = 28
-0,44х = -22
х = 50
50(г) – молока
100 – 50 = 50(г) – пломбира.
Ответ:50г молока,50г пломбира
Подведение итогов урока
Оценки за урок.
Домашнее задание.
Рефлексия. (Синквейн)
Спасибо за урок!