| 1. Организационный этап В
заимное приветствие учащихся и учителя, фиксация отсутствующих, проверка готовности к уроку.
2.Подготовка к основному этапу усвоения учебного материала.
Формулировка темы и задач урока.( см. приложение1)
Давайте определим задачи урока.
Вводное слово учителя. Химик: мы на прошлом уроке говорили о необходимости изучения серной кислоты, как важнейшего вещества, ежегодное производство которого в мире ≥160млн.тонн. Биолог: для химии кислота- важнейшее вещество. Но вы все слышали о кислотных дождях, о их влиянии на окружающую среду .Давайте же подробнее это рассмотрим. Биолог .Приступаем к закладке опыта. Приложение 2.
3. Совершенствование знаний по теме «Сера. Серная кислота».
Фронтальная беседа с классом. 1.назовите элементы V| группы А подгруппы ПСХЭ. 2.Какие важнейшие соединения серы вам известны. Напишите их в тетради, проверьте с доской. 3.Какие степени окисления характерны для атома серы. 4. Охарактеризуйте оксиды серы и их свойства. 5.Каковы физические свойства серной кислоты. 6.Какие общие свойства характерны для серной кислоты. 7.Какие индикаторы позволяют обнаружить кислоты. 8.Назовите продукты взаимодействия Н2SО4 с основными оксидами и основаниями. 9.Как называются соли серной кислоты. 10.С какими солями может реагировать серная кислота. 11.Как можно распознать серную кислоту. 12.С какими металлами реагирует серная кислота. 13.Какова особенность концентрированной серной кислоты. 14.Как действует конц. серная кислота на органические вещества.
Ребята, а теперь получите задания для своей группы. Группа1.Почему техническая серная кислота коричневого цвета? Зимой между рамами окон иногда помещают сосуд с концентрированной серной кислотой. С какой целью это делают? Почему нельзя заполнять сосуд кислотой до верху .
Группа2.Охарактеризуйте области применения серной кислоты. На каких свойствах основано применение серной кислоты.
Группа3.Концентрированная серная кислота при нагревании реагирует с ртутью и серебром подобно тому, как реагирует с медью. Составьте уравнения этих реакций, укажите окислитель и восстановитель. Группа4.Распознайте тремя способами растворы серной кислоты и хлорида натрия (пробирки№1 и 2). Напишите уравнения реаций.
Отчёт групп о выполнении своей работы.
Самостоятельная работа
Работа проводится по вариантам.(См.приложение4.)
Дети, имеющие хорошие уровень знаний, получают индивидуальные карточки. (См. приложения).
Итак: Какие же свойства характерны для серной кислоты.
2.Как действует концентрированная серная кислота на органические вещества? 3.Где мы встречаем органические вещества.
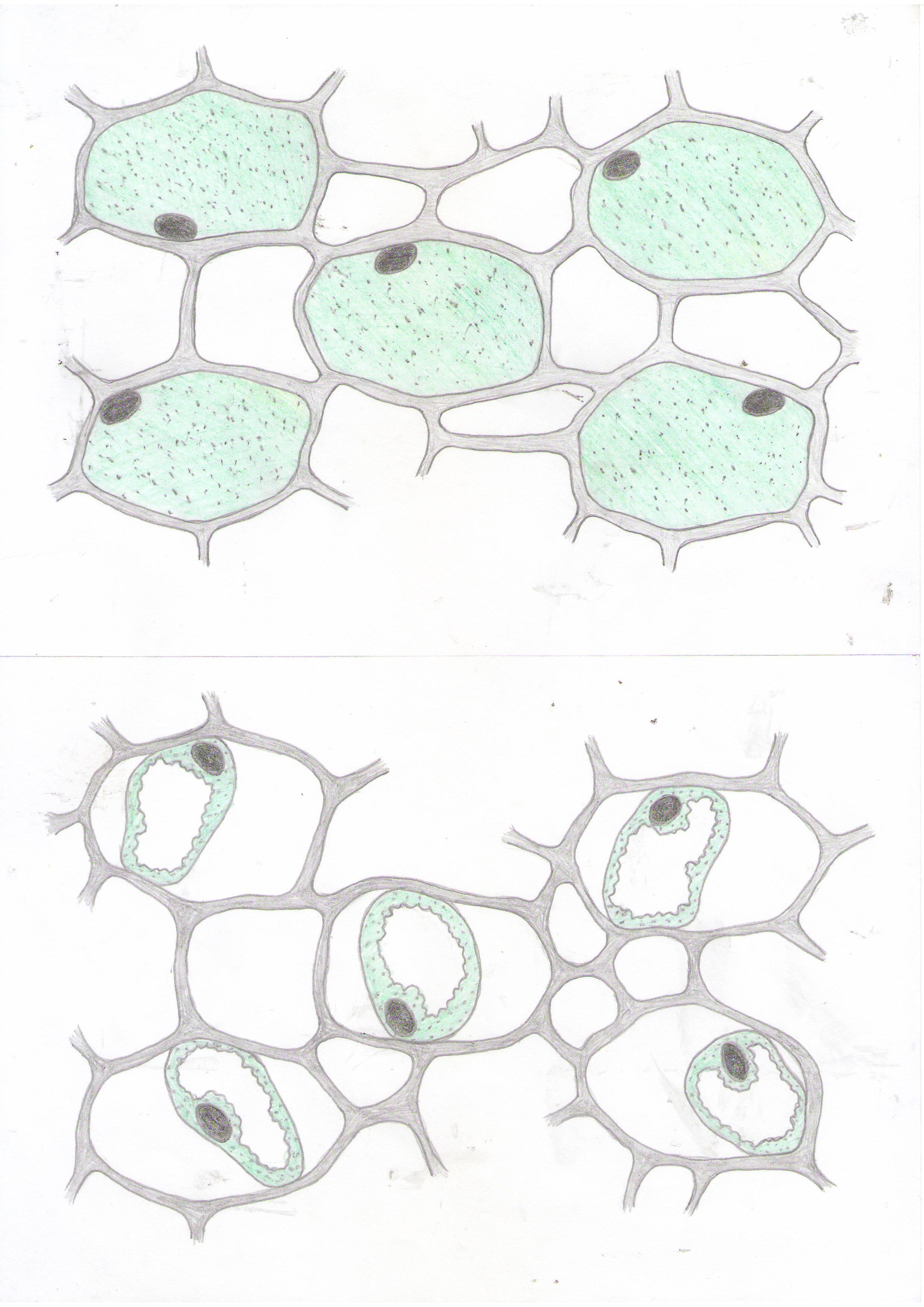
Биолог. Возвращаемся к нашему опыту. Как вы думаете, что мы можем ожидать в нашем опыте.
Чтобы подтвердить ваши предположения, приготовим микропрепараты.
Учитель биологии ведёт инструктаж.
Проведите плазмолиз 1М раствором сахарозы. 1-2мин.обождите. Задание Рассматривая микропрепарат при большом увеличении, посчитайте число оставшихся живых клеток.
Как распознать живую и мёртвую клетку.
Какой вывод можно сделать на основе увиденного?.
Сравните результаты подсчётов в своей группе. Везде ли одинаковое число мёртвых клеток.
Учитель формирует общий вывод. Больше живых клеток в тех листовых пластинках, где мало хлорофилла, у растений с толстой кутикулой.
Фронтальная прблемно – поисковая беседа 1.Где и когда мы наблюдаем действие кислоты на растения?
2.А откуда в воздухе серная кислота? Работа со схемой(см.приложение5)
3.Какие предприятия города выбрасывают кислотные оксиды.
4.Так ли безобиден летний дождь?.
5.А почему не все растения реагируют на кислотные дожди?. Àäðåñ îòïðàâèòåëÿ / получателя:
СТРАНА, Индекс, ã. Город, óë. Улица, äîì №, êâ. №
Кому Àäðåñ îòïðàâèòåëÿ / получателя:
СТРАНА, Индекс, ã. Город, óë. Улица, äîì №, êâ. №
Кому Àäðåñ îòïðàâèòåëÿ / получателя:
СТРАНА, Индекс, ã. Город, óë. Улица, äîì №, êâ. №
Кому Àäðåñ îòïðàâèòåëÿ / получателя:
СТРАНА, Индекс, ã. Город, óë. Улица, äîì №, êâ. №
Кому Àäðåñ îòïðàâèòåëÿ / получателя:
СТРАНА, Индекс, ã. Город, óë. Улица, äîì №, êâ. №
Кому
.Вывод Химик. Можно однозначную дать оценку серной кислоте, её свойствам? Кислоту применяют как кислоту, окислитель, обезвоживающее средство. В условиях антропогенного загрязнения, когда кислота входит в состав кислотных дождей – возможны повреждения и гибель растительных клеток.
Домашнее задание. Стр.93-94.№1.5.7.8.11.-1группа. 2группа.стр.93-94№4.10.13.16.17. 3группа стр.95.№26.
Итог урока
| Подготовка учащихся к работе, снятие напряжения, настрой на определённый ритм урока. Орг. момент – камертон урока.
Обеспечить мотивацию и принятие учащимися задачи урока. Подача темы через загадку снимет нервное напряжение, создаст более спокойную обстановку, настроит на взаимопонимание.
Происходит настрой на интеграцию химических и биологических знаний.
Дети, разбившись на 4 группы, закладывают опыт для изучения воздействия серной кислоты на растительную клетку. Учитель химии актуализирует правила обращения с серной кислотой.
Продолжительность воздействия на лист – 40мин.. В это время организуется совершенствование знаний по теме.
Проверка и корректировка знаний по теме.
Данная беседа организуется с целью проверки теоретических знаний по данной теме, проверки домашнего задания. Вопросы составлены таким образом, что при ответах на них можно и нужно пользоваться таблицами оформления кабинета, а потому работать могут и ученики слабо успевающие по химии.
Вопросы беседы выстроены в определённой логической последовательности.
Предполагается вспомнить и систематизировать знания, Развитие монологической речи.
В ходе беседы составляется схема обобщения. См. приложение3.
Для достижения максимального обучающего, развивающего и воспитывающего эффекта в группу объединяются дети с разным уровнем подготовки. Задания выполняют все вместе, если возникает затруднения, более сильно подготовленный объясняет материал всей группе. При отчёте учитель спрашивает любого члена группы. Т.о. планируется ликвидация пробелов знаний. Планируется выявить качество и уровень овладения учащимися знаниями и способами действий. Идёт отработка навыков и умений, что пригодится при самостоятельной работе.
Планируется актуализация знаний качественных реакций, отработка навыков обращения с реактивами, умения составлять уравнения реакций.
Расширение знаний по предмету .Слышат отчёт по 4 разным вопросам.
Проверка знаний свойств кислоты, отработка умений составления уравнений реакций. В то же время осуществляется дифференциация заданий по уровню сложности, объёму.
Учитель осуществляет переход от отработки свойств серной кислоты к выяснению влияния её на растительные клетки. Логическая взаимосвязь 2 этапов урока.
Ставится проблема, для решения которой ученики должны перенести знания из химии в биологию
Готовят препараты, происходит подготовка к исследовательской деятельности.
В группе каждый готовит один препарат, затем ими будут обмениваться.
Актуализация биологических навыков и знаний.
Отработка навыка обращения с микроскопом.
Актуализация биологических знаний.
Подводит под формулировку вывода.
Акцентируется внимание на каждом результате. Перед детьми ставится новая проблема.
Формулировка вывода побуждает к вопросу о приспособленности растений.
Активизация познавательной деятельности, расширение кругозора.
Постановка проблемы ведёт к поиску ответа.
Работа с краеведческим материалом заставляет задуматься о производстве в нашем городе.
Нацеливает внимание на вопрос охраны здоровья.
Интегрирование химических, биологически экологических знаний.
Происходит формирование мировоззрения.
Задание дифференцировано по уровню сложности и объёму знаний. Выполнение домашнего задания-этап творческого применения усвоенных знаний и способов действий, основа для решения новых учебных задач.
Констатация достижения поставленной задачи урока. Объективность выставления оценок, комментирование их. | Готовность и быстрое включение учащихся класса в деловой ритм урока.
Активный поиск ответа показывает их готовность к восприятию темы. После формулировки темы пытаются определить задачи урока.
В сознании детей возникает проблема: серная кислота – кислотные дожди – окружающие нас растения. Это усиливает мотивацию учения.
Работая с инструкционной карточкой, дети вспоминают правила обращения с режущим инструментом, правила техники безопасности при обращении с кислотами. Происходит развитие исследовательских навыков.
Учащиеся демонстрируют знания свойств серной кислоты, умения правильно излагать свои мысли .Проявляют интеграцию с курсом географии.
Пользуются при ответах справочными материалами, стендами, показывают знания ПСХЭ.
Отвечая на вопрос об общих свойствах кислот, вынуждены интегрировать знания ранее изученных тем.
У учащихся развивается логическое мышление, умение устанавливать причинно – следственные связи.
Записывая схему в тетрадь, учащиеся закрепляют знания о подгруппе кислорода, особенностях разбавленной и концентрированной кислот.
Учатся обобщать свои знания в виде схемы.
Происходит развитие монологической речи. В работу включена зрительная память, слуховая память, мышечная память.
В процессе групповой работы, тесного делового сотрудничества у учащихся формируются коммуникативные навыки, поведенческая культура.
Приобретают умения делового общения, учатся понимать и оценивать личность, дела товарищей, регулировать своё поведение в соответствии с интересами своей группы.
Устанавливают причинно- следственную связь между свойствами и применением.
Вспоминают свойства кислоты, расстановку коэффициентов методом электронного баланса, окислитель-восстановитель. Т.о. происходит внутрипредметная интеграция.
Вспоминают качественные реакции, отрабатывают навыки составления уравнений реакций, навыки работы с реактивами. .
Подводят итог своей работы. Происходит развитие монологической, химически грамотной речи.
Мобилизуют знания о свойствах серной кислоты, отрабатывают навык составления уравнений реакций в ионном, молекулярном виде, навык обращения со справочным материалом( таблица растворимости).. По индивидуальным карточкам –навык осуществления генетических цепочек, решение задач, окислительно- восстановительных реакций.
Ученики, выполнив письменную индивидуальную работу, проработав материал в группе и фронтально, обобщают химические свойства серной кислоты.
Вопросы позволяют осуществить логический переход от одной части урока к другой. Возникает необходимость интеграции биологических знаний.
Поставленный вопрос заставляет интегрировать материал химии-биологии. Ученики предполагают изменения свойств клеток, т.к. серная кислота обладает свойством обезвоживания. Дети предполагают причинно-следственную связь.
Вспоминают правила приготовления препарата, отрабатывают навык приготовления препарата.
Воспитывает ответственность за выполняемое дело.
Учащиеся ведут исследовательскую деятельность.
Выполняя задание, сравнивают живые и мёртвые клетки.
Вспоминают отличия мёртвой клетки от живой.
Анализируя увиденноё, проведя подсчёт, делают вывод о воздействии серной кислоты на растительную клетку.
Первый результат исследований вызвал интерес у детей. Вторая проблема этот интерес усиливает .Они активно анализируют, сравнивиют, приходят к выводу.
Больше живых клеток у растений, (герань, красула древовидная).
Записывают вывод в тетрадь. Возникает вопрос: Почему разное число мёртвых клеток?
Извлекают из долговременной памяти примеры внезапного пожелтения листвы на деревьях.
Анализируют, выдвигают гипотезы.
Вспоминают, сопоставляют, приводят примеры: мартеновский цех ВМЗ, теплоизол, автотранспорт.
Приходят к заключению о защите волос и кожи головы во время дождя.
Интегрируют знания из биологии, экологии и химии. Приходят к заключению об адаптации растений к действию абиотических факторов.
Учащиеся ещё раз анализируют весь материал урока. Связь химии с биологией и экологией обеспечивает понимание учащимися сущности наблюдаемых природных явлений, что крайне важно для формирования целостного миропонимания.
|




 онцентрированная Разбавленная
онцентрированная Разбавленная ислота + лакмус Красная
ислота + лакмус Красная ислота + метил.фт розовый
ислота + метил.фт розовый ислота +МеО Сульфат металла + вода
ислота +МеО Сульфат металла + вода ислота +Ме(ОН)2 Сульфат металла + вода
ислота +Ме(ОН)2 Сульфат металла + вода







 2
2


 nS
nS 

 ульфат натрия Сульфат цинка
ульфат натрия Сульфат цинка