Вариант 1.
Сумма коэффициентов в уравнении реакции между оксидом алюминия и серной кислотой равна
Верны ли следующие суждения о правилах безопасной работы в химической лаборатории?
вдохнуть.
Ответ:
В задании В4 на установление соответствия запишите в таблицу цифры выбранных вами ответов. Получившуюся последовательность цифр запишите в строку ответа. |
В4.
Установите соответствие между исходными веществами и продуктами реакции.
ИСХОДНЫЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
 А) Ca(OH)2 + CO2 1) CaCO3 + H2
А) Ca(OH)2 + CO2 1) CaCO3 + H2
 Б) CaCO3 + HCl 2) CaCO3 + H2O
Б) CaCO3 + HCl 2) CaCO3 + H2O
 В) Ca + H2O 3) CaCl2 + H2O + CO2
В) Ca + H2O 3) CaCl2 + H2O + CO2
4) CaO + H2
5) Ca(OH)2 + H2
Ответ: ___________
Часть 3
C1. Рассчитайте массу осадка, который выпадет при взаимодействии избытка карбоната калия с 17,4 г раствора Ca(OH)2 с массовой долей последнего 15%.
Стандартизированная контрольная работа
8 класс
На выполнение контрольной работы отводится 45 минут. Работа состоит из 3 частей и включает 16 заданий.
Часть 1 включает 10 заданий базового уровня (А1-А10). К каждому заданию дается 4 варианта ответа, из которых только один правильный. За выполнение каждого задания - 1 балл.
Часть 2 состоит из 4 заданий повышенного уровня (В1-В4), на которые надо дать краткий ответ в виде числа или последовательности цифр. За выполнение каждого задания - 2 балла.
Часть 3 содержит наиболее сложные объемные задания (С1-C2), которые требуют полного ответа. За выполнение задания ты можешь получить С1 – 4 балла.
Баллы, полученные за выполненные задания, суммируются. Максимально ты можешь набрать 22 балла.
Система оценивания работы:
0-7 баллов – «2» | 8-12 баллов – «3» |
13-18 баллов – «4» | 18-22 балла – «5» |
-
8 класс ВАРИАНТ-1
Часть 1
-
При выполнении заданий этой части под номером выполняемого вами задания поставьте знак «Х» в клеточку, номер которой соответствует номеру выбранного вами ответа. |
-
А1. Число атомов всех химических элементов в молекуле серной кислоты равно:
-
А2. Элемент второго периода главной подгруппы III группы ПСХЭ - это:
1) литий | 3) кальций |
2) бор | 4) магний |
А3. Число протонов, нейтронов и электронов в атоме фтора 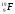
1) p+ – 9; n0 – 10; ē – 19 | 3) p+ – 9; n0 – 10; ē - 9 |
2) p+ – 10; n0 – 9; ē – 10 | 4) p+ – 9; n0 – 9; ē - 19 |
-
А4. Группа формул веществ с ковалентным типом связи:
1) H2S, P4, CO2 | 3) HCl, NaCl, H2O |
2) H2, Na, CuO | 4) CaO, SO2, CH4 |
-
А5. Верны ли следующие высказывания?
А. В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера усиливаются.
Б. В главной подгруппе неметаллические свойства атомов элементов с увеличением порядкового номера ослабевают.
1) верно только А | 3) верно только Б |
2) верны оба суждения | 4) оба суждения не верны |
-
А6. Запись 3О2 означает:
1) 2 молекулы кислорода | 3) 5 атомов кислорода |
2) 3 молекулы кислорода | 4) 6 атомов кислорода |
А7. Ряд формул, в котором все вещества – оксиды:
1) SO3, MgO, CuO | 3) ZnO, ZnCl2, H2O |
2) KOH, K2O, MgO | 4) H2SO4, Al2O3, HCl |
-
А8. Формула сульфата железа (III):
1) FeS | 3) Fe2 (SO4)3 |
2) FeSO4 | 4) Fe2(SO3)3 |
А9. Сумма всех коэффициентов в уравнении реакции, схема которой
Al + O2 Al2O3 равна:
-
А10. Верны ли следующие высказывания?
А. Оксид фосфора (V) - кислотный оксид.
Б. Соляная кислота - одноосновная кислота.
1) верно только А | 3) верно только Б |
2) верны оба суждения | 4) оба суждения не верны |
Часть 2
-
В задании В1 на установление соответствия запишите в таблицу цифры выбранных вами ответов, а затем полученную последовательность цифр перенесите в бланк ответов без пробелов и других символов. (Цифры в ответе могут повторяться). |
-
В1. Установите соответствие между формулой вещества и классом соединения:
Формула вещества: | Класс соединения: |
А) Н3РО4 | 1) соль |
Б) SO3 | 2) основный оксид |
В) Сu(OH)2 | 3) нерастворимое основание |
Г) CaCl2 | 4) кислотный оксид |
-
| 5) кислота |
-
| 6) растворимое основание |
А | Б | В | Г |
-
| -
| -
| -
|
Ответом к заданию В2-В3 является последовательность цифр, которые соответствуют номерам правильных ответов. Запишите выбранные цифры в бланк ответов в порядке возрастания без пробелов и других символов. |
В2. Уравнения реакции замещения:
1) BaO + H2O = Ba(OH)2 | 4) Ca(OH)2 + 2HCl = CaCl2+2H2O |
2) CuO + H2 = Cu + H2O | 5) 2NH3 = N2 + 3H2 |
3) 3KOH + H3PO4 = K3PO4 + 3H2O | 6) Mg + 2HCl = MgCl2 + H2 |
Ответ: _____________
В3. С раствором гидроксида натрия реагируют:
1) сульфат меди (II) | 4) азотная кислота |
2) оксид меди (II) | 5) магний |
3) гидроксид калия | 6) оксид углерода (IV) |
Ответ: _____________
Ответом к заданию В4 является число. Запишите это число в бланк ответов без указания единиц измерения. |
В4. Масса соли, содержащейся в 150 г 5 %-ного раствора соли, равна _____г. (Запиши число с точностью до десятых).
-
Часть 3
-
Запишите номер задания и полное решение |
C1. Составьте уравнения химических реакций согласно схеме:
Fe(OH)3 → Fe2O3 → Fe → FeSO4
Назовите все сложные вещества, укажите тип реакции.
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Стандартизированная контрольная работа
8 класс
На выполнение контрольной работы отводится 45 минут. Работа состоит из 3 частей и включает 16 заданий.
Часть 1 включает 10 заданий базового уровня (А1-А10). К каждому заданию дается 4 варианта ответа, из которых только один правильный. За выполнение каждого задания - 1 балл.
Часть 2 состоит из 4 заданий повышенного уровня (В1-В4), на которые надо дать краткий ответ в виде числа или последовательности цифр. За выполнение каждого задания - 2 балла.
Часть 3 содержит наиболее сложные объемные задания (С1-C2), которые требуют полного ответа. За выполнение задания ты можешь получить С1 – 4 балла, С2 – 3 балла.
Баллы, полученные за выполненные задания, суммируются. Максимально ты можешь набрать 22 балла.
Система оценивания работы:
0-7 баллов – «2» | 8-12 баллов – «3» |
13-18 баллов – «4» | 18-22 балла – «5» |
-
8 класс ВАРИАНТ-2
Часть 1
-
При выполнении заданий этой части под номером выполняемого вами задания поставьте знак «Х» в клеточку, номер которой соответствует номеру выбранного вами ответа. |
А1. Число атомов всех химических элементов в молекуле фосфорной кислоты равно:
-
А2. Элемент третьего периода главной подгруппы III группы ПСХЭ - это:
1) алюминий | 3) магний |
2) бериллий | 4) бор |
А3. Число протонов, нейтронов и электронов в атоме хлора 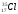
1) p+ – 18; n0 – 18; ē – 18 | 3) p+ – 17; n0 – 18; ē - 18 |
2) p+ – 17; n0 – 17; ē – 17 | 4) p+ – 17; n0 – 18; ē - 17 |
-
А4. Группа формул веществ с ионным типом химической связи:
1) Na2S, KCl, HF | 3) CO2, BaCl2, NaOH |
2) K2O, NaH, NaF | 4) Ca, O2, AlCl3 |
А5. Верны ли следующие высказывания?
А. В периоде металлические свойства атомов элементов с увеличением порядкового номера усиливаются.
Б. В периоде металлические свойства атомов элементов с увеличением порядкового номера ослабевают.
1) верно только А | 3) верно только Б |
2) верны оба суждения | 4) оба суждения не верны |
А6. Запись 4N означает:
1) 4 молекулы азота | 3) 4 атома азота |
2) 2 молекулы азота | 4) 4 атома натрия |
А7. Ряд формул, в котором все вещества – основания:
1) СuOH, CuCl2, NaOH | 3) Ca(OH)2, Mg(OH)2, MgOHCl |
2) K2O, HCl, Ca(OH)2 | 4) KOH, Ba(OH)2, Cu(OH)2 |
-
А8. Формула хлорида меди (II):
1) CuCl | 3) CuCl2 |
2) Cu(NO3)2 | 4) CuSO4 |
А9. Сумма вcех коэффициентов в уравнении реакции, схема которой Ca + HCl CaCl2 + H2, равна:
-
А10. Верны ли следующие высказывания?
А. Серная кислота – двухосновная.
Б. Оксид калия – основный оксид.
1) верно только А | 3) верно только Б |
2) верны оба суждения | 4) оба суждения не верны |
-
Часть 2
-
В задании В1 на установление соответствия запишите в таблицу цифры выбранных вами ответов, а затем полученную последовательность цифр перенесите в бланк ответов без пробелов и других символов. (Цифры в ответе могут повторяться). |
В1. Установите соответствие между формулой вещества и классом соединения:
-
-
-
Формула вещества: | -
-
-
Класс соединения: |
А) LiOH | 1) соль |
Б) SO2 | 2) основный оксид |
В) HNO3 | 3) нерастворимое основание |
Г) CaCO3 | 4) кислотный оксид |
-
| 5) кислота |
-
| 6) растворимое основание |
Ответом к заданию В2 является последовательность цифр, которые соответствуют номерам правильных ответов. Запишите выбранные цифры в бланк ответов в порядке возрастания без пробелов и других символов. |
В2. Уравнения реакции разложения:
1) CaO + SiO2 = CaSiO3 | 4) Fe2O3 + 2Al = Al2O3 + 2Fe |
2) FeS + 2HCl = FeCl2 + H2S | 5) NaСl + AgNO3 = NaNO3 + AgCl |
3) 2KNO3 = 2KNO2 + O2 | 6) 2Al(OH)3 = Al2O3 + 3H2O |
Ответ: _______
В3. В реакцию с раствором соляной кислоты вступают:
1) ртуть | 4) карбонат натрия |
2) гидроксид магния | 5) хлорид бария |
3) оксид натрия | 6) оксид серы (VI) |
Ответ: _______
Ответом к заданию В3 является число. Запишите это число в бланк ответов без указания единиц измерения. |
В4. В 450 г воды растворили 50 г соли. Массовая доля соли в полученном растворе равна_____%. (Запиши число с точностью до десятых).
-
Часть 3
-
Запишите номер задания и полное решение. |
-
C1. Составьте уравнения химических реакций согласно схеме
Na → NaOH → Cu(OH)2 → CuO.
Назовите все сложные вещества, укажите тип реакции.
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
-
Стандартизированная контрольная работа
9 класс
Контрольная работа по химии в IX классе проводится в форме, максимально приближенной к экзаменационной работе для проведения государственной итоговой аттестации выпускников IX классов общеобразовательных учреждений.
Система оценивания работы
-
| Тестирование |
Часть 1 | Каждое правильно выполненное задание части 1 оценивается 1 баллом. За выполнение задания с выбором ответа выставляется 1 балл при условии, если обведен только один номер верного ответа. Если обведены и не перечеркнуты два и более ответов, в том числе правильный, то ответ не засчитывается. |
Максимальное кол-во баллов за часть 1: | 19 баллов |
Часть 2 | Задание с кратким ответом считается выполненным верно, если правильно выбраны все варианты ответа. За полный правильный ответ – 2 балла, за неполный правильный ответ – 1 балл, за неверный ответ (или при его отсутствии) – 0 баллов. |
Максимальное кол-во баллов за часть 2: | 8 баллов |
Часть 3 | Задания части 3 оцениваются в зависимости от полноты и правильности ответа. Ответ правильный и полный – 3 балла. Правильно записаны 2 элемента ответа – 2 балла. Правильно записан один элемент – 1 балл. Все элементы ответа записаны неверно – 0 баллов. |
Максимальное кол-во баллов за часть 3: | 3 балла |
Общее кол-во баллов | 30 баллов | -
|
-
| Кол-во баллов | % выполнения работы | Оценка |
Тестирование -
| менее 10 баллов | менее 30 % | «2» |
10 - 17 баллов | 30 % - 52 % | «3» |
18 - 27 баллов | 53 % - 82 % | «4» |
28 - 30 баллов | 83 % - 100 % | «5» |
-
-
-
1
-
 А) SO2 + H2O 1) H2SO4
А) SO2 + H2O 1) H2SO4