Данная презентация полностью соответствует требованиям ФГОС и может использоваться учителями,работающими по любым учебным программам.Материал,представленный в презентации включает в себя: задания для повторения, обобщения и контроля знаний,задачи на вывод молекулярной формулы, что поможет ученику пополнить знания,полученные в классе.Задания,предложенные в презентации,можно рассматривать как первый шаг в подготовке учащихся к итоговой аттестации.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
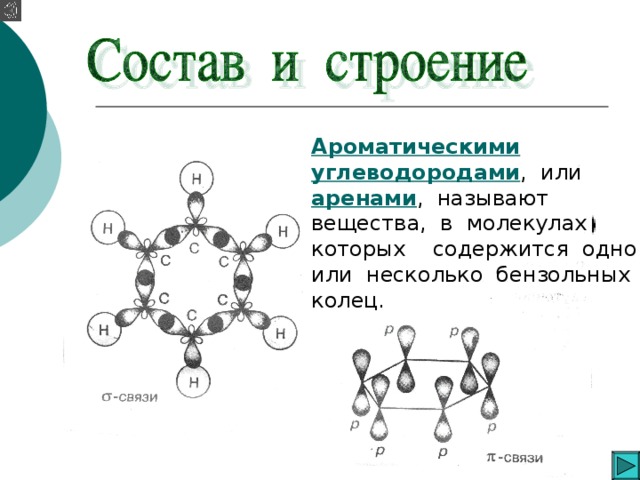
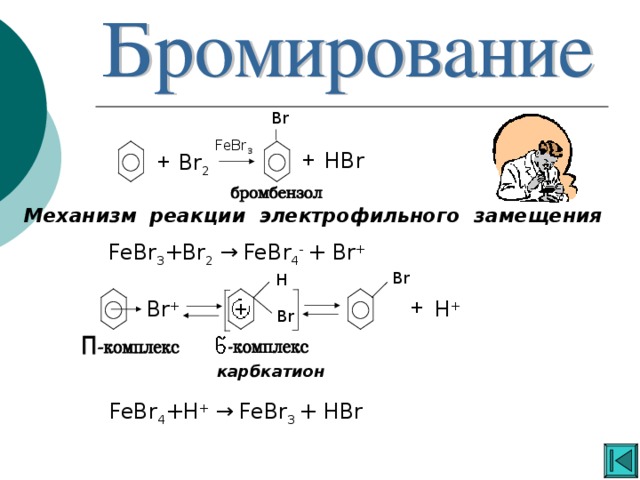
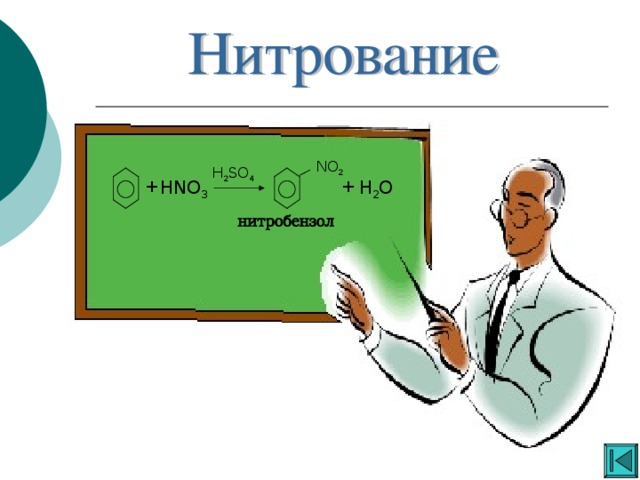
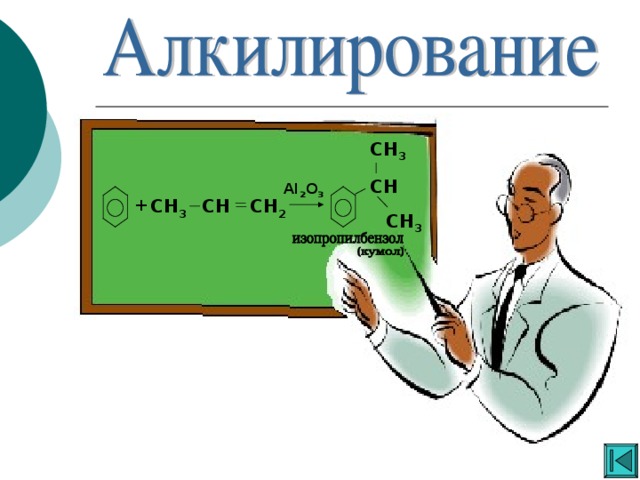
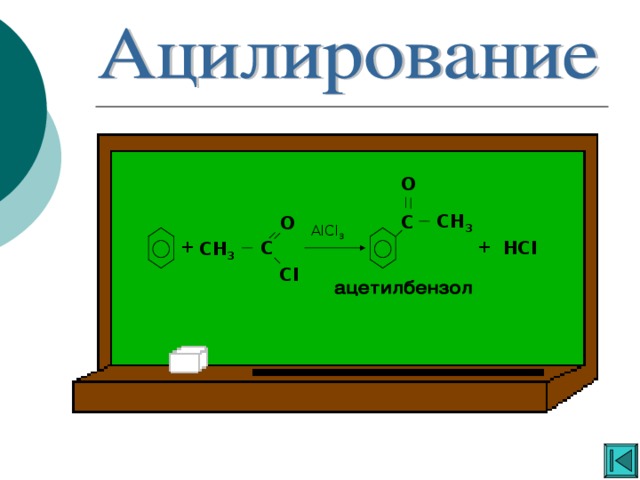
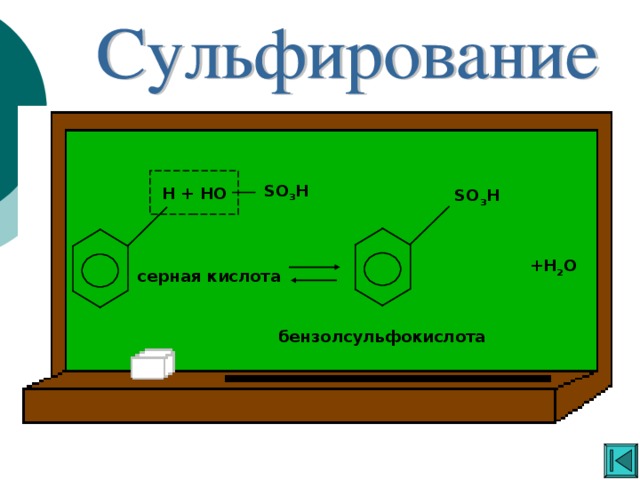
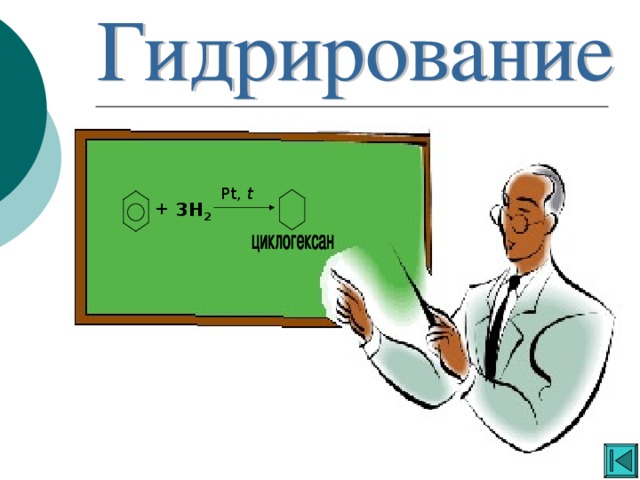
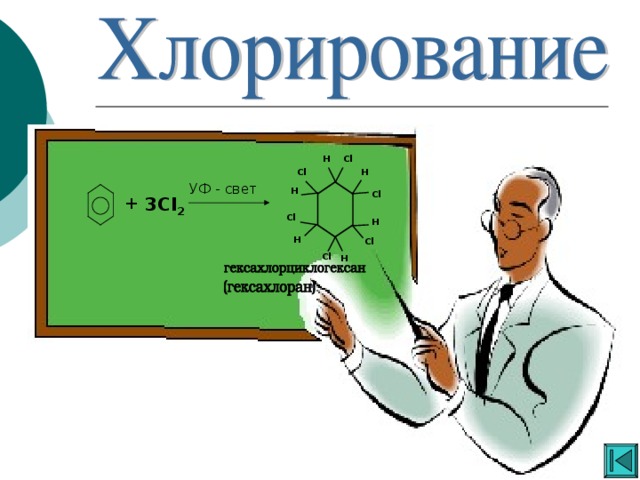
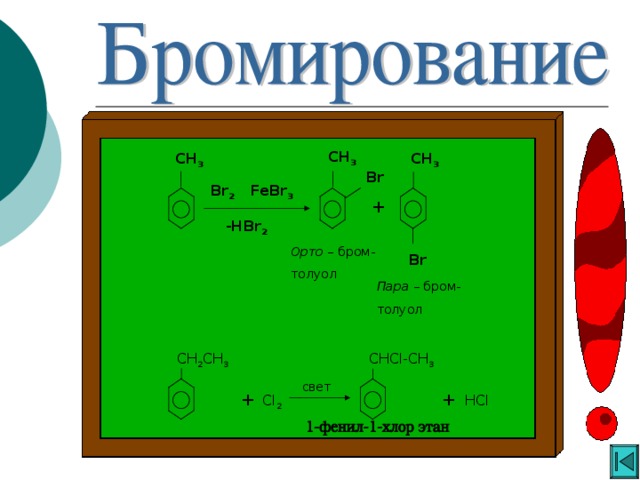
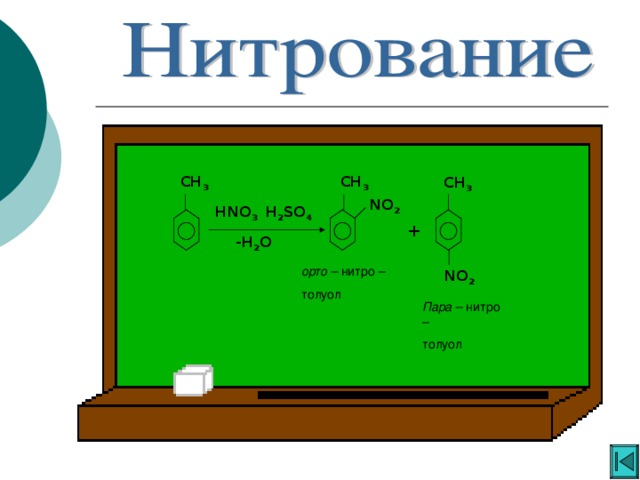
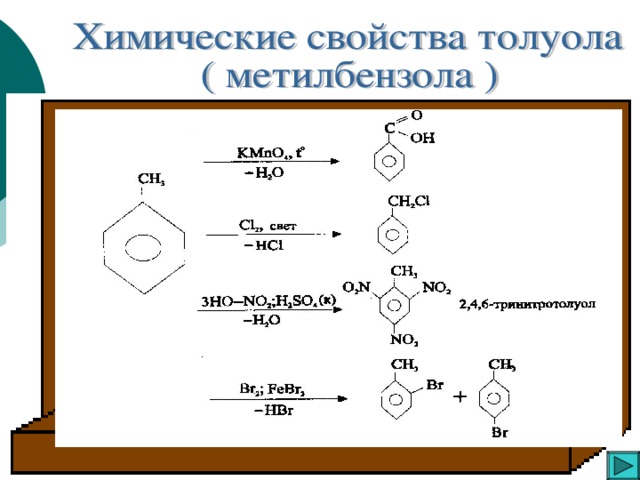
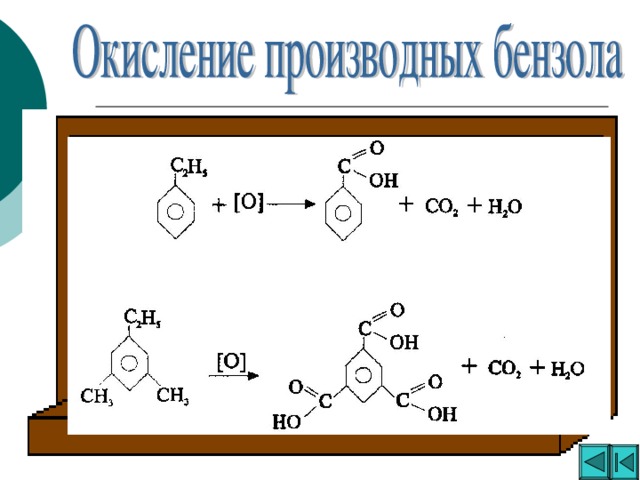
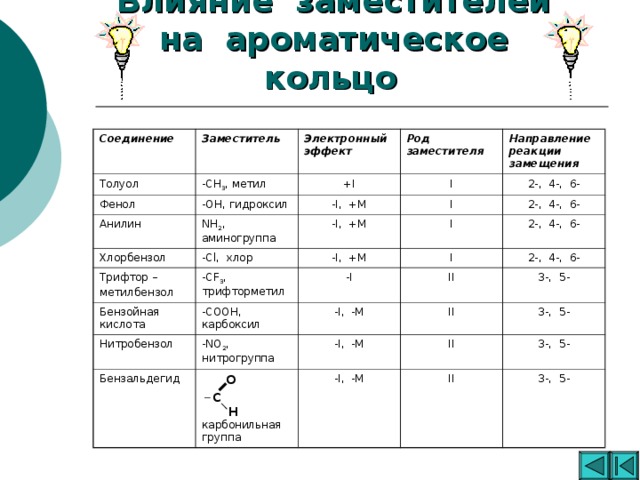
Ароматические углеводороды
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Ароматические углеводороды »
Полезное для учителя
Распродажа видеоуроков!
1520 руб.
2530 руб.
1660 руб.
2760 руб.
1700 руб.
2840 руб.
1660 руб.
2760 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства







![CH 3 COOH [O] CH 3 COOH терефталевая кислота](https://fsd.kopilkaurokov.ru/uploads/user_file_5620e44129d31/img_user_file_5620e44129d31_23.jpg)

















