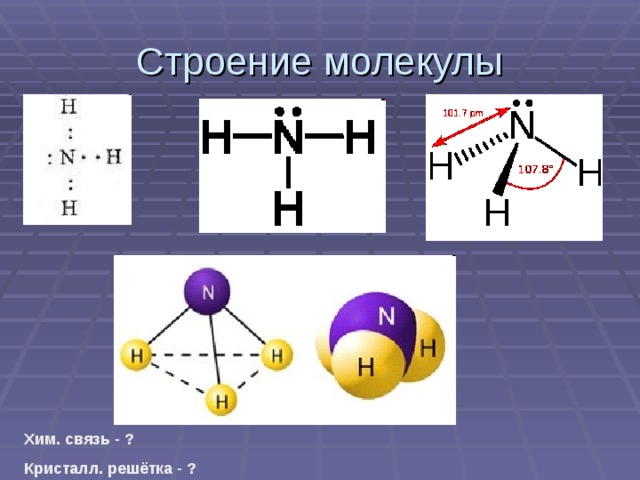
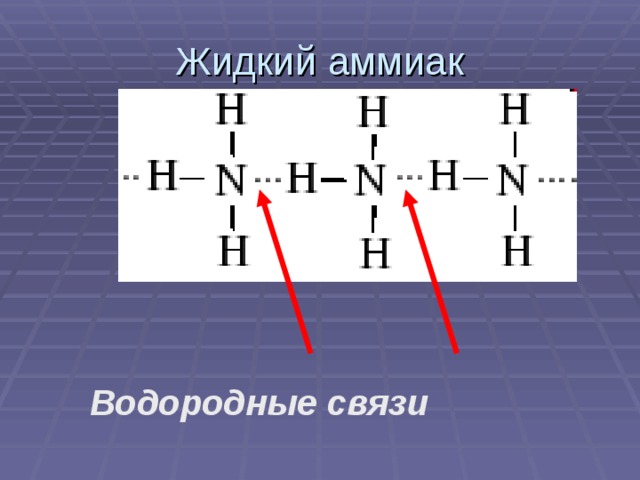
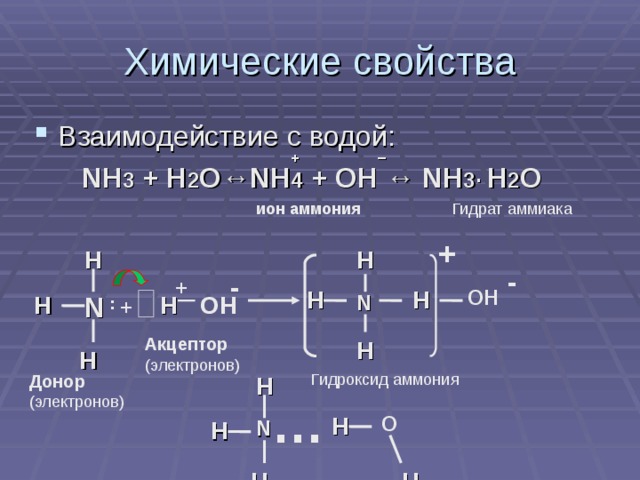
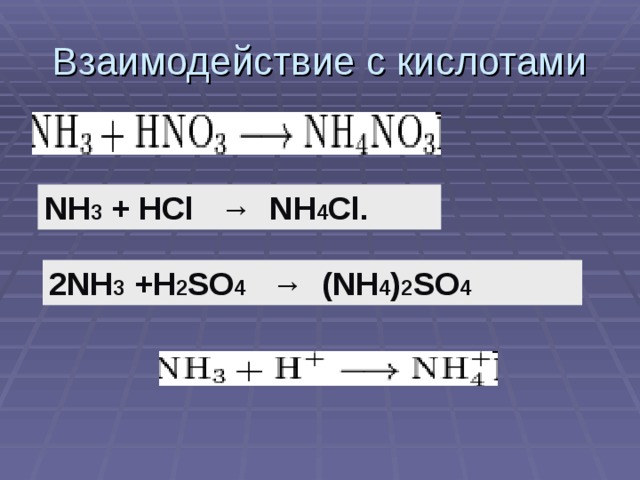
Взаимосвязь рельефа и природы родного края. Природопользование
Вихри враждебные
Влияние антропогенной деятельности на глобальное потепление климата
Влияние антропогенных факторов на состояние водных ресурсов села
Влияние водного туризма на изменение прибрежной зоны реки
Влияние газификации на экологию области
Влияние географических особенностей на национальные символы страны
Влияние географического положения на жизнь людей нашего района
Влияние изменения климата на живую природу
Влияние капризов погоды на здоровье людей
Влияние микроклимата на здоровье человека.
Влияние многолетней мерзлоты на окружающую среду
Влияние положения женщины в обществе на демографическую ситуацию в стране
Влияние хозяйственной деятельности человека на состояние почвы
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
Взаимосвязь рельефа и природы родного края. Природопользование
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Взаимосвязь рельефа и природы родного края. Природопользование»
Полезное для учителя
Распродажа видеоуроков!
1540 руб.
2560 руб.
1550 руб.
2580 руб.
1660 руб.
2770 руб.
1600 руб.
2660 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства