Общие правила:
правило № 1 – поднятая рука – готовность к ответу,
правило № 2 - умение слушать,
правило № 3 - умение вступать в обсуждение.

1-я загадка.
Она и дождь, и град и снег Туман и гололёд, Носитель благ,
предвестник бед И радуга и лёд. Что это за вещество?

Какова формула воды?

Н 2 О

2-я загадка.
Этот газ, необходимый растениям для фотосинтеза.
Этот газ, выделяемый нами при выдохе.
Что это за газ?

Назовите его формулу?

СО 2

3-я загадка.
Отрывок из стихотворения
А. Ахматовой.
...на рукомойнике моём Позеленела медь, Но так играет
луч на нём, Что весело глядеть...

Как вы считаете, что произошло с медью?
Почему она позеленела?

она окислилась

Загадка
С кислородом ходит парой,
То металл, то неметалл он,
Дружбу связями скрепит
Всем известный класс…

ОКСИД
Н 2 О
СuО
СО 2

Подготовила:
учитель химии,
Мынбаева
Жанар Тасбулатовна
ОКСИДЫ
г.Державинск – 2015 г.

Оксидами называются сложные вещества, состоящие из 2-х элементов, один из которых кислород с валентностью II.
ЭО

Приложение 1
«Узнай оксид»
1 команда: KNO 3 , H 2 O, KCL, N 2 O 5 , SO 3 , PH 3 , CaO, AgCL, NaOH, CaS, NaCl
2 команда: NH 3 , CO 2 , H 2 CO 3 , K 2 S, ZnO, Al 2 O 3 ,CH 4 , HNO 3 ,HgO, FeO, H 2 SO 4
3 команда: CS 2 , K 2 O, HCl, SO 2 , KOH, SiO 2 , Al(OH) 3 , BaO, HNO 3 , Na 2 O, KCl

Приложение 1
«Узнай оксид»
1 команда: H 2 O, N 2 O 5 , SO 3 , CaO,
2 команда: CO 2 , ZnO, Al 2 O 3 ,HgO, FeO
3 команда: K 2 O, SO 2 , SiO 2 , BaO, Na 2 O
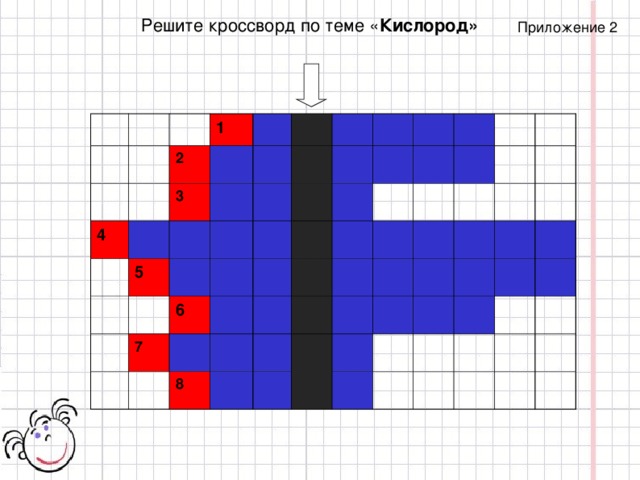
Решите кроссворд по теме « Кислород»
Приложение 2
1
2
4
3
5
6
7
8
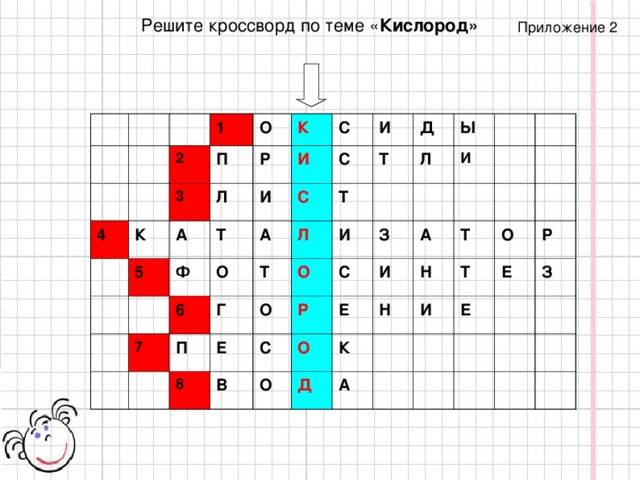
Решите кроссворд по теме « Кислород»
Приложение 2
1
2
4
П
К
3
О
К
5
А
Р
Л
Т
И
Ф
С
И
6
И
7
О
А
С
С
Г
Л
Т
Т
П
Т
Д
8
О
О
Л
Е
И
Ы
З
В
Р
И
С
С
Е
А
О
И
О
Н
Д
Т
Н
К
А
О
И
Т
Е
Р
Е
З

Оксиды – oxides – оксидтер
Лист – leaf (Sheet) – жапырақ (парақ)
Фотосинтез – photosynthesis - фотосинтез
Катализатор – catalyst - катализатор
Горение – burning - жану
Песок – sand - құм
Вода – water - су

ЭО
Название оксида = оксид + название элемента в Р.п.
Н 2 О – Оксид водорода
СО 2 – Оксид углерода (IV)
СuО – Оксид меди(II)
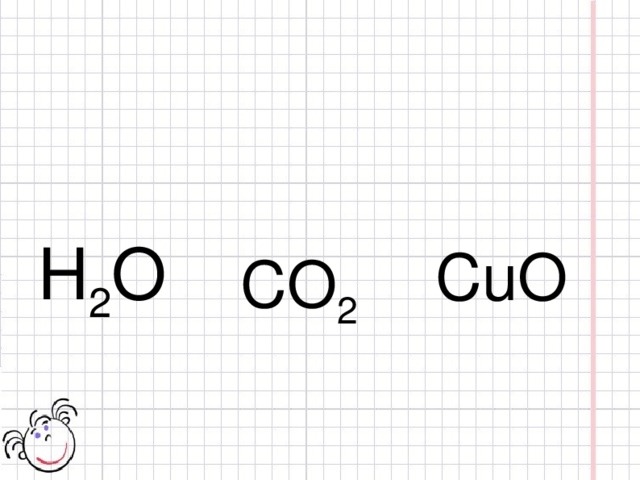
Н 2 О
СuО
СО 2
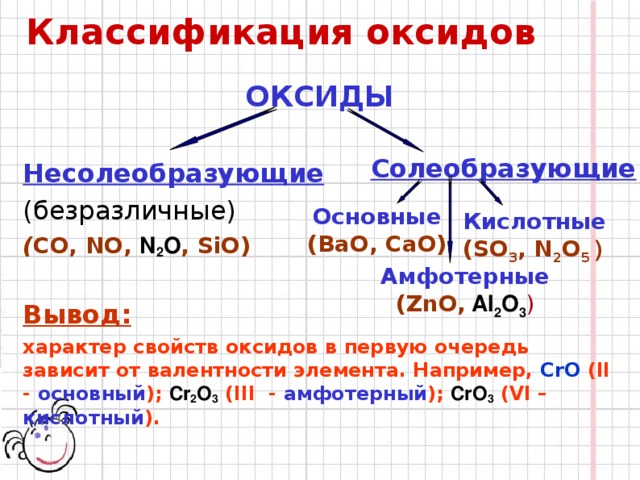
Классификация оксидов
ОКСИДЫ
Несолеобразующие
(безразличные)
( СО, NO, N 2 O , SiO)
Вывод:
характер свойств оксидов в первую очередь зависит от валентности элемента. Например, CrO (II - основный ); Cr 2 O 3 (III - амфотерный ); CrO 3 (VI – кислотный ).
Солеобразующие
Основные
(ВаО, СаО)
Кислотные
(SO 3 , N 2 O 5 )
Амфотерные
(ZnO, Al 2 O 3 )

«Найди свой домик»
У вас на столах кружочки с номерами валентности. Из каждой команды участвуют 3 учащихся. Ученик показывает тот кружочек, которому соответствует валентность элемента в прочитанном оксиде.

Приложение 3
1 команда: H 2 O, N 2 O 5 , SO 3 , CaO, CO
2 команда: CO 2 , ZnO, Al 2 O 3 ,HgO, FeO
3 команда: K 2 O, SO 2 , SiO 2 , BaO, Na 2 O

Неметаллы, знай, мой друг,
Строго все себя ведут:
Коль в оксиды он подался -
Так "кислотным" и назвался!
Металл хотел запутать нас,
Но я найду опору:
Если валентность меньше трех -
Оксид зову "основным".
Ну, а уж если повезло,
Валентность пять и выше –
Я буду помнить, всем назло,
Оксид "кислотным" кличут.

Приложение 4
Найдите формулы всех оксидов, которые можно составить из следующих записей. Проклассифицируйте их.
Са, S, О, О 2 , Аl 2 , Mg, О 3 , Fe.
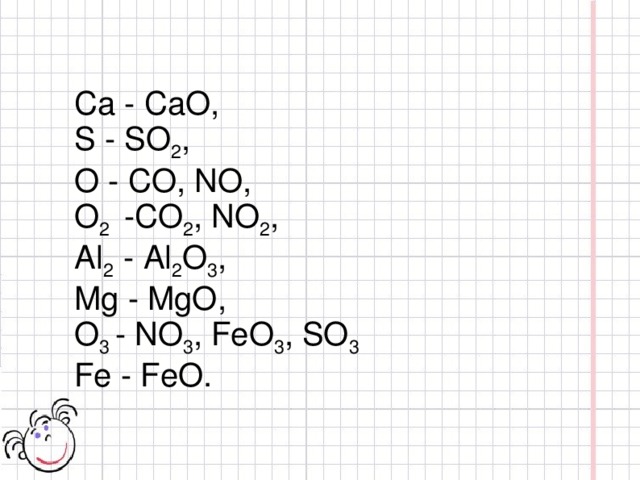
Са - СаО,
S - SO 2 ,
О - СО, NO,
О 2 -СО 2 , NO 2 ,
Аl 2 - Al 2 O 3 ,
Mg - MgO,
О 3 - NO 3 , FеО 3 , SО 3
Fe - FеО.

Взаимопроверка.
Основные: СаО, Аl 2 О 3 , MgO, Fe 2 O 3 , FeO.
Кислотные: SO 2, СО, СО 2, NО, NO 2, SО 3, NО 3 .

Приложение 5
Поиграйте в «крестики – нолики».
Покажите выигрышный путь,
который составляют формулы оксидов.
HCl
O 2
NaOH
SO 2
Al 2 O 3
FeO
Li 2 S
H 2 CO 3
NaBr

1). Оксиды – это:
а) вещества, в состав которых входит водород
б) вещества, в состав которых входит кислород
в) вещества, в состав которых входят металлы
2). Как называется оксид СО 2 :
а) оксид углерода (II)
б) угарный газ
в) оксид углерода(IV)
3). К оксидам относят вещество:
а) СаО; б) СаН 2 ; в) СаСl 2

Закончите предложения
1. Меня удивило…. 2 . Я задумался… 3 . У меня возник вопрос…

Домашнее задание
Написать небольшой рассказ
в тетради на тему
«Оксиды в повседневной жизни человека».

Синквейн - это творческая работа, которая имеет короткую форму стихотворения, состоящего из пяти нерифмованных строк .
Синквейн – это не простое стихотворение, а стихотворение, написанное по следующим правилам:
1 строка – одно существительное , выражающее главную тему cинквейна.
2 строка – два прилагательных , выражающих главную мысль.
3 строка – три глагола , описывающие действия в рамках темы.
4 строка – фраза , несущая определенный смысл.
5 строка – слово-резюме в форме существительного, характеризующее суть предмета или объекта .

Пример синквейна
Оксид меди -
- Чёрный, твёрдый
- Не растворяется, не испаряется, не используется в пищу
- Сложное химическое соединение
- Медь оксидовна !

Темы синквейнов
- Углекислый газ
- Угарный газ
- Сернистый газ
- Оксид железа (II)
- Оксид железа (III)
- Песок
- Гашёная известь
- Оксид алюминия
- Оксид серы (VI)
- Вода

Приложение 6
Физические свойства оксидов
Широка натура у оксидов,
Камнем вниз(…), а то рекой течет (…),
А захочет – газ различных видов (…),
И веществ создаст круговорот (…).
Может черным быть (…), и белым (…),
Может с запахом (…) и без (…),
Не оставит вас без дела:
«Изучайте – мир чудес!»

Физические свойства оксидов
Широка натура у оксидов,
Камнем вниз ( CuO, CaO ), а то рекой течет ( H 2 O ),
А захочет – газ различных видов ( CO 2 , SO 2 ),
И веществ создаст круговорот ( CO 2 , H 2 O, SO 3 ) .
Может черным быть ( CuO ), и белым ( CaO ),
Может с запахом ( SO 2 ) и без ( CO 2 ),
Не оставит вас без дела:
«Изучайте – мир чудес!»


Спасибо за внимание!
Успехов в работе и отличного настроения !