Туысындаймын адамның.
Мыңдаған жылдар бұрын
Алғашқы адам үңгірін
Жарқыратып тұрғанмын
Алау отпен жаққанмын.
Ханымдар мен мырзаның
Әшекейлеп бергенмін
Үстіне киген киімін.
Жұмсақ болып кейде мен
Дәптерге де жазамын,
Табиғатым осындай
Элементпін мен қандай?

Көміртек және оның қосылыстары

Көміртек
Қолданылуы
Аяқ киім майы
адсорбент
типография
болат
С
Ауыл шаруашылығы
Әшекей бұйымдар
отын
медицина
резеңке

Сабақтың мақсаты:
- Менделеев кестесіне сүйене отырып, көміртек атомының құрылысын зерттеу;
- Көміртектің аллотропиялық түрөзгерісін зерттеу;
- Көміртектің химиялық қасиетін және қолданылуын үйрену;
- Көміртектің (ІІ) және (IV) оксидінің құрылысын, қасиеттерін, алынуын және қолданылуын үйрену;
- Көмір қышқылының құрылысын, қасиетін және қолданылуын үйрену

№ 1 оқу модулі
Көміртектің периодтық жүйедегі орнына сүйене отырып, мына сұрақтарға жауап беріңдер:
Көміртектің химиялық таңбасы қандай?
Атомдық нөмірі мен ядро заряды?
Атомдық массасы?
Атомдық ядросында қанша протон бар?
Атомдық ядросында қанша нейтрон бар?
Көміртек атомында қанша электрон бар?
Валенттік электроны қанша?
Ең төмен тотығу дәрежесі нешеге тең?
Ең жоғары тотығу дәрежесі нешеге тең?
Әрбір дұрыс жауапқа 1 ұпай.
Жауабы
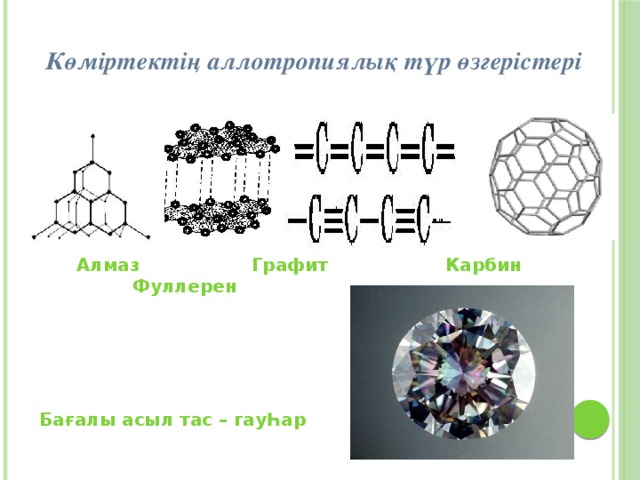
№ 1 оқу модулі Жауабы
1) С
2) 6, +6
3) Ar(C) = 12
4) 6
5) 12 – 6 = 6
6) 6,
7) 4,
8) -4
9) +4
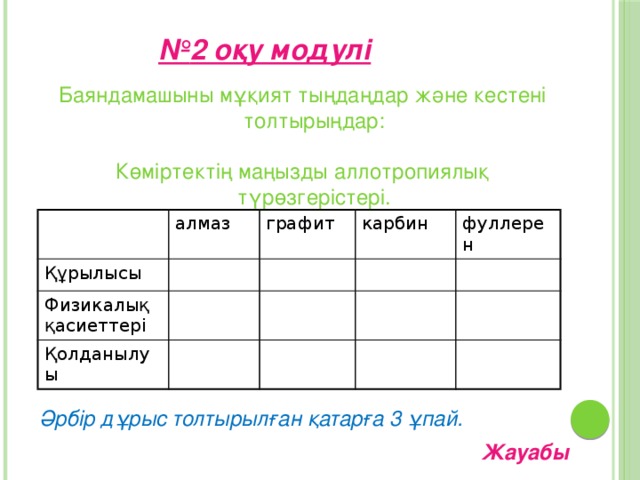
Көміртектің аллотропиялық түр өзгерістері
Алмаз Графит Карбин Фуллерен
Бағалы асыл тас – гауҺар

№ 2 оқу модулі
Баяндамашыны мұқият тыңдаңдар және кестені толтырыңдар:
Көміртектің маңызды аллотропиялық түрөзгерістері.
Құрылысы
алмаз
Физикалық қасиеттері
графит
Қолданылуы
карбин
фуллерен
Әрбір дұрыс толтырылған қатарға 3 ұпай.
Жауабы

Алмаз
- Түссіз
- Мөлдір
- Электр тогын өткізбейді
- Мықты
- Қатты
Алмаз кубтық сингонияда кристалданады.
Алмаз кристалындағы көміртек атомдары бір-бірінен бірдей қашықтықта тетраэдр түзе орналасқан.
Графит
- Қара сұр түсті
- Мөлдір емес
- Электр тогын өткізеді
- Жұмсақ
- Аздап жылтыры бар
- Қағазға оңай жұғады
- Майлы
Графитте атомдар бір жазықтықта орналасқан, ал әртүрлі параллель жазықтықтарда орналасқан атомдардың өзара байланысы өте әлсіз. Графиттің қабаттары бірінің үстінде
бірі оңай жылжиды. Сондықтан одан қарындаш
өзектерін жасайды.

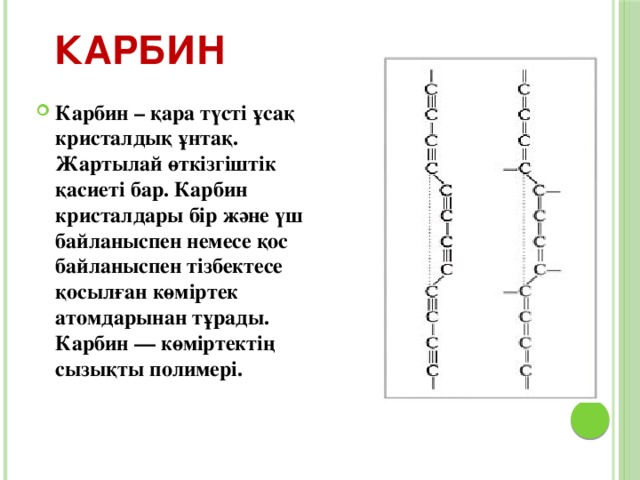
Карбин
- Карбин – қара түсті ұсақ кристалдық ұнтақ. Жартылай өткізгіштік қасиеті бар. Карбин кристалдары бір және үш байланыспен немесе қос байланыспен тізбектесе қосылған көміртек атомдарынан тұрады. Карбин — көміртектің сызықты полимері.

Фуллерен
- Фуллере́ндер — көміртек атомдарының белгілі бір сандарынан C 60 , C 70 , тұратын тұйықталған құрылымдар. C 60 фуллеренінің түрі футбол добына ұқсайды, C 70 сопақ қауынға ұқсайды.
- Жартылай өткізгіштер, дәрілер, жасанды алмаздар алуда қолданылады.

№ 2 оқу модулі (Жауабы)
Құрылысы
алмаз
Физикалық қасиеттері
графит
Кубтық атомдық тор, коваленттік полюссіз байланыс
Қабатталған құрылысы бар. Ішкі қабаттары коваленттік полюссіз байланысқан, әрбір қабаттары –молекулаішілік қарым-қатынаста
карбин
Қолданылуы
Қатты
Электр тоғын жақсы өткізеді, тугоплавкий, майлағыш қасиеті бар
Шынжыр іспетті байланысқан
фуллерен
Бұрғылайтын, тесетін құралдар…
C60, C70, молекулалары шар және сопақ қауын сияқты тор түзеді
Электродтар, отқа төзімді ыдыстар, ракета қозғалтқыштары…
Химиялық берік, қатты
Жоғары қатты құралдар

Көміртек
Тотықтырғыш қасиеті – көміртек атомы 4 электрон қосып алған кезде -4 тотығу дәрежесін көрсетеді.
Тотықсыздандырғыш қасиеті – көміртек атомы 4 (2) электрон берген кезде, оның тотығу дәрежесі +4 (+2) тең болады.
Көміртек

Тотықтырғыш қасиеті
1.Қыздырған кезде көміртек оттекпен әрекеттесіп, көміртек (IV)оксидін (көмірқышқыл газын) түзеді:
С + O 2 = CO 2
Оттек толық жетіспеген жағдайда көміртек (II) оксиді (иіс газы) түзіледі:
2С + О 2 = 2СО
2. Көміртек сутекпен тек катализатор қатысында және жоғары температурады әрекеттеседі.
С + 2H 2 = CH 4
3. Көміртек қыздыру нәтижесінде күкірт және фтормен, ал азотпен электр тогының әсерімен әрекеттеседі:
С + 2S = CS 2
С + 2F 2 = CF 4
2С + N 2 = (CN) 2
Тотықсыздандырғыш қасиеті
1. Су буларын қыздырылған көмір арқылы өткізгенде сутек газын ығыстырып шығарады :
Н 2 O + С = СО + Н 2
2. Көміртекті көміртек (IV) оксидімен бірге қыздырғанда иіс газы түзіледі:
С + СО 2 = 2СО
3. Көміртек көптеген оксидтерді бос металдарға дейін тотықсыздандыра алады:
2Fe 2 O 3 + 3С = 4Fe + 3CO 2
4. Көміртек металмен немесе оның оксидтерімен әрекеттескенде карбидтер түзеді:
CaO + 3C = CaC 2 + СО
4Al + 3C = Al 4 C 3
№ 3 оқу модулі
Көміртек
Реакция теңдеулерін аяқтап, теңестіріңдер
- C + O 2 =
- C + O 2 =
- C + H 2 =
- C + Ca =
- C + Al =
- C + CuO =
- C + FeO =
- C + H 2 O =
Коэффициенттері дұрыс қойылып, аяқталған реакция теңдеуіне 1 ұпайдан
Жауабы

№ 3 оқу модулі (Жауабы)
Көміртек
Реакция теңдеулерін аяқтап, теңестіріңдер
- 2C + O 2 = 2СО
- C + O 2 = СО 2
- C + 2H 2 = СН 4
- 2C + Ca = СаС 2
- 3C + 4Al = Аl 4 С 3
- C + CuO =Сu + CO.
- C + FeO = Fe + CO,
- C + H 2 O = CO + H 2 ,

№ 4 оқу модулі
Кестені толтырыңдар
Салыстыру белгілері
Көміртек II оксиді
Көміртек IV оксиді
2. Алынуы
3. Физикалық қасиеттері
4. Химиялық қасиеттері
5. Қолданылуы
Әрбір ұяшықтың жауабы дұрыс болса 5 ұпаймен бағаланады.
Жауабы
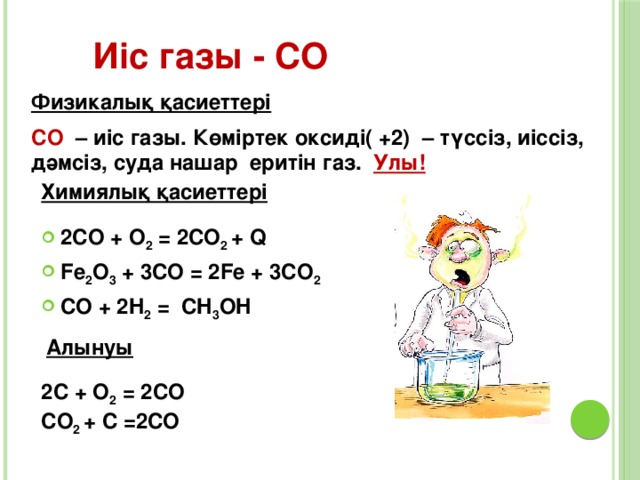
Иіс газы - СО
Физикалық қасиеттері
СО – иіс газы. Көміртек оксиді( +2) – түссіз, иіссіз, дәмсіз, суда нашар еритін газ. Улы!
Химиялық қасиеттері
- 2CO + O 2 = 2CO 2 + Q
- Fe 2 O 3 + 3CO = 2Fe + 3CO 2
- CO + 2H 2 = CH 3 OH
Алынуы
2C + O 2 = 2CO
CO 2 + C =2CO
Көмірқышқыл газы – СО 2
Физикалық қасиеттері
СО 2 – көміртек оксиді (+4) , көмірқышқыл газы – иіссіз, түссіз газ, дәмі сәл қышқылдау, ауадан 1,5 есе ауыр. Суда ериді.
CaCO 3 + 2HCl = CaCI 2 + CO 2 + H 2 O
CaCO 3 = CaO + CO 2
Химиялық қасиеттері
- CO 2 + H 2 O = H 2 CO 3
- Na 2 O + CO 2 = Na 2 CO 3
- Ca(OH) 2 + CO 2 = CaCO 3 + H 2 O
Тапсырмаға оралу

№ 4 оқу модулі ( жауабы)
1.Формуласы
Көміртек II оксиді
Көміртек IV оксиді
СО
2. Алынуы
СО 2
2С + О 2 = 2СО
3.Физикалық қасиеттері
4. Химиялық қасиеттері
СО 2 + С = 2СО
CaCO 3 + 2HCl = CaCI 2 + CO 2 + H 2 O.
Түссіз, иіссіз, дәмсіз, суда нашар еритін газ. Улы!
2CO + O 2 = 2CO 2 + Q.
Иіссіз, түссіз газ, дәмі сәл қышқылдау, ауадан 1,5 есе ауыр. Суда ериді.
CaCO 3 = CaO + CO 2 .
CO + 2H 2 = CH 3 OH.
CO 2 + H 2 O = H 2 CO 3
5. Қолданылуы.
Металл оксидтерінен таза металл алу үшін қолданылады.
Fe 2 O 3 + 3CO = 2Fe + 3CO 2
Na 2 O + CO 2 = Na 2 CO 3
Құрғақ мұз, өрт сөндіруге,
Ca(OH) 2 + CO 2 = CaCO 3 + H 2 O
Тамақ өнеркәсібінде.
Көмір қышқылының тұздарын алуда қолданылады.

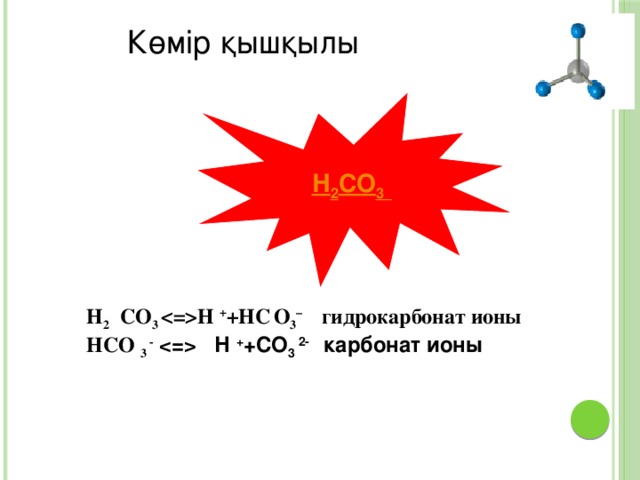
Көмір қышқылы
H 2 CO 3
Көмір қышқылы — екінегізді тұрақсыз қосылыс,
бос күйінде алуға болмайды. Сілтілермен әрекеттесіп орта және қышқыл тұздар түзе әрекеттеседі.
Көмірқышқыл газы суда ерігенде аз мөлшерде
түзіледі.

Көмір қышқылы
Н 2 СО 3 Н + +НС О 3 – гидрокарбонат ионы
НСО 3 - Н + +СО 3 2- карбонат ионы

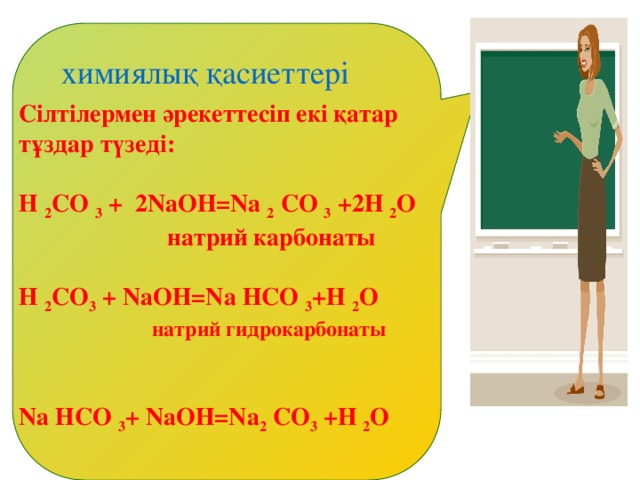
химиялық қасиеттері
Сілтілермен әрекеттесіп екі қатар тұздар түзеді:
Н 2 СО 3 + 2NаОН=Nа 2 СО 3 +2Н 2 О
натрий карбонаты
Н 2 СО 3 + NаОН=Nа НСО 3 +Н 2 О
натрий гидрокарбонаты
Nа НСО 3 + NаОН=Nа 2 СО 3 +Н 2 О

Көмір қышқылының тұздары
Қыздырғанда ыдырайды:
СаСО 3 =СаО+СО 2 ↑
2NаНСО 3 =Nа 2 СО 3 +СО 2 ↑+Н 2 О
Гидролизге ұшырайды:
Nа 2 СО 3 +НОН=NаОН+NаНСО 3
Сапалық реакциясы:
Nа 2 СО 3 +2НСl=2NaCl+СО 2 ↑+Н 2 О
СО 2 ↑+Са ( ОН ) 2 = Са СО 3 ↓+Н 2 О
ақ тұнба

Қолданылуы
Көмір қышқылы көмірқышқыл газының судағы ерітіндісінде кездеседі. (газдалған су).
Көмір қышқылын таза күйінде газдалған сусын
ішу арқылы қолданамыз.
Газдалған сусынның қақпағын ашқан кезде быжылдаған
газ бөлінеді. Дәл сол жерде көмір қышқылы
көмірқышқыл газы мен суға айналады.

№ 5 оқу модулі
Айналымды жүзеге асырыңдар
С→СО→СО 2 →Na 2 CO 3 → NaHCO 3 →CO 2
Әрбір дұрыс реакция теңдеуіне 1 ұпай.
Жауабы

№ 5 оқу модулі (Жауабы)
1. 2С + О 2 = 2СО
2. 2CO + O 2 = 2CO 2
3. Na 2 O + CO 2 = Na 2 CO 3
4. Na 2 CO 3 + CO 2 + H 2 O = 2NaHCO 3
5. 2NaHCO 3 = Na 2 CO 3 + CO 2 + H 2 O

Табиғаттағы айналымы

Сабақты қорытындылау.
- Сабақтың мақсатын оқыңдар.
- Сіз сабақтың мақсатына жеттіңіз бе? Қандай дәрежеде?
- Сабақтағы өз жұмысыңызды бағалаңыз.
– 39 – 41 ұпай
– 36–38 ұпай
– 30–35 ұпай
30 ұпайдан төмен болса қанағаттандырылмайды.
- Жинаған ұпай санына қарай үй тапсырмасын алыңыз және күнделікке жазып қойыңыз.

Үйге тапсырма.
- – §22,23 105бет № 12, 110бет №9
- □ – §22,23 105бет №11, 110бет №8
- – §22,23 105бет №10, 110бет №7
- “ 2” – §22,23 110бет №10

Сабағымыз аяқталды
Сау болыңыздар!
 – §
– §