Тип урока: обобщение и систематизация знаний.
Вид: урок -путешествие.
Цели урока:
1.Повторение систематизаций знаний о классификации неорганических веществ и их свойствах.
2.Развитие навыков составления генетических рядов элементов, написание соответствующих реакций.
3.Совершенствование техники проведения химического эксперимента
Методы обучения:
- фронтальная беседа
- самостоятельная работа
- эксперимент
Оборудование: мультимедийная презентация, микролаборатории с веществами, таблица «Генетическая связь неорганических веществ»
Ход урока.
1. Организационный момент.
- Обобщение материала.
Слайд 1. Тема: Основные классы неорганических веществ.
Учитель: Сегодня обобщающий урок по теме: «Основные классы неорганических веществ». Задача нашего урока – систематизировать изученный материал – основные классы неорганических соединений путем логического мышления, обобщения, классификации, генетической связи. Поэтому мы сегодня совершим с вами увлекательное путешествие в страну знаний. Это будет непростая прогулка. В дороге нас ждут испытания, преодолеть, которые можно применив знания, полученные на уроках химии. И насколько ваши ответы будут быстрыми и логически правильными, настолько наше путешествие будет интересным. Итак, в путь за знаниями.
Слайд 2. Наши цели:
1.Закрепить и углубить знания об основных классах неорганических веществ;
2.Повторить характеристику оксидов, кислот, оснований, солей;
3.Развить умения составлять уравнения реакции;
4.Совершенствовать умения экспериментально подтверждать химические свойства различных веществ.
Для выполнения целей мы совершим путешествие по загадочным местам
Слайд 3. Этапы маршрута
u Собери рюкзак
u Восхождение
u Водопад веществ
u Река Превращений
u В пещере колдунов
u Путь домой
u Путевые заметки
Слайд 4. Собери рюкзак.
План характеристики вещества:
u Определение
u Классификация
u Примеры
А. Оксиды – это…
В. Кислоты – это…
С. Основания – это…
Д. Соли – это…
На данном этапе необходимо вспомнить определения, классификации всех изученных классов неорганических соединений:
Оксиды- сложные вещества, состоящие из двух элементов, один из которых кислород. Оксиды делятся на: основные и кислотные, солеобразующие и несолеобразующие
Основания – электролиты, которые при диссоциации образуют катионы металла и анионы гидроксогрупп ОН-. Классифицируются на растворимые и нерастворимые,сильные и слабые, однокислотные и многокислотные.
Кислоты – электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Делятся на: одноосновные и многоосновные, растворимые и нерастворимые, кислородные и бескислородные, летучие и нелетучие, сильные и слабые, стабильные и нестабильные.
Соли – электролиты, которые при диссоциации образуют катионы металла (или аммония) и анионы кислотных остатков. Делятся на: средние, кислые и основные.
Слайд 5. Индикаторы – указатели.
Существуют такие вещества, с помощью которых можно определить щёлочь, кислоту и воду в пробирке. У вас имеются пробирки с прозрачными растворами: кислота, щёлочь и вода. С помощью индикатора определите их.
(их можно определить с помощью метилоранжа или лакмуса)
Слайд 6. Этап II-Восхождение.
SO3 – c H2O, Na2O, NaOH
HCl – c Zn, Na2O, NaOH
KOH – c SO3, HCl, CO2
Слайд 7. Этап III – Водопад веществ.
Распределите вещества по классам и назовите их
Al2O3, Mg(NO3)2, H2SO4,CO2, Ca(OH)2, Na2O, H2CO3, Mg, K2O, NaCl, KNO3, H2SiO3, MgO, Na2SO4,N2O5, NaOH, Ca, ZnCl2, CaCO3, Cl2O7, HCL, AL(OH)3, C, ZnSO4, AL2(SO4)3, H2SO3, Mg(OH)2, SiO2
Простые вещества: металлы- Mg, Ca; неметаллы - C
Сложные вещества:
Оксиды - Al2O3, CO2, Na2O, , K2O, MgO, N2O5 ,Cl2O7, SiO2
Основания - Ca(OH)2, NaOH, AL(OH), , Mg(OH)2
Кислоты - H2SO4, H2CO3, H2SiO3, HCL, , H2SO3
Соли - Mg(NO3)2, NaCl, KNO3, Na2SO4, ZnCl2, CaCO3, ZnSO4, AL2(SO4)3
Слайд 8. Этап IV. Река превращений
Осуществите ряд превращений:
Cu → CuO → CuSO4 → Cu(OH)2
Назовите полученные вещества.
Cu + O2 = CuO CuO + H2SO4= CuSO4 + H2O CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Слайд 9. Этап V. В пещере колдунов
Допишите уравнения реакций:
Экспериментально осуществите эти превращения.
MgO + 2HCl = MgCl2 + H2O
Zn + H2SO4 = ZnSO4 + H2
NaOH + HCl = NaCl + H2O
Слайд 10. Этап VI. Путь домой
Al2O3, Mg(NO3)2, H2SO4,CO2, Ca(OH)2, Na2O, H2CO3, Mg, K2O, NaCl, KNO3, H2SiO3, MgO, Na2SO4, N2O5, NaOH, Ca, ZnCl2, CaCO3, Cl2O7, HCL, AL(OH)3, C,ZnSO4, AL2(SO4)3, H2SO3, Mg(OH)2, SiO2
Составьте генетическую связь между классами неорганических соединений:
Слайд 11. Проверьте себя
Mg → MgO → Mg(OH)2 → Mg(NO3)2 - Генетический ряд металла
C → CO2 → H2CO3 → CaCO3 - Генетический ряд неметалла
Слайд 12. Этап VII. Путевые заметки
u Дополните записи урока – оформите дневник путешественника
Слайд 13. Домашнее задание:
Царь зовёт к себе Стрельца,
Удалого молодца,
И даёт ему поручение
Государственного значения.
Чтоб я стал опять богат,
Нужен бария сульфат.
Ночь даю тебе подумать –
Утром буду ждать доклад!
Не смогёшь - кого винить?
Должен я тебя казнить.
Запиши себе названье,
Чтоб со страху не забыть.
1). Помогите Стрельцу получить возможными способами сульфат бария.
2). §42, с. 169-171
3. Заключение по уроку. Выставление отметок
Просмотр содержимого документа
«Основные классы неорганических веществ»
Основные классы неорганических веществ.
Тип урока: обобщение и систематизация знаний.
Вид: урок -путешествие.
Цели урока:
1.Повторение систематизаций знаний о классификации неорганических веществ и их свойствах.
2.Развитие навыков составления генетических рядов элементов, написание соответствующих реакций.
3.Совершенствование техники проведения химического эксперимента
Методы обучения:
фронтальная беседа
самостоятельная работа
эксперимент
Оборудование: мультимедийная презентация, микролаборатории с веществами, таблица «Генетическая связь неорганических веществ»
Ход урока.
Организационный момент.
Обобщение материала.
Слайд 1. Тема: Основные классы неорганических веществ.
Учитель: Сегодня обобщающий урок по теме: «Основные классы неорганических веществ». Задача нашего урока – систематизировать изученный материал – основные классы неорганических соединений путем логического мышления, обобщения, классификации, генетической связи. Поэтому мы сегодня совершим с вами увлекательное путешествие в страну знаний. Это будет непростая прогулка. В дороге нас ждут испытания, преодолеть, которые можно применив знания, полученные на уроках химии. И насколько ваши ответы будут быстрыми и логически правильными, настолько наше путешествие будет интересным. Итак, в путь за знаниями.
Слайд 2. Наши цели:
Закрепить и углубить знания об основных классах неорганических веществ;
Повторить характеристику оксидов, кислот, оснований, солей;
Развить умения составлять уравнения реакции;
Совершенствовать умения экспериментально подтверждать химические свойства различных веществ.
Для выполнения целей мы совершим путешествие по загадочным местам
Слайд 3. Этапы маршрута
Собери рюкзак
Восхождение
Водопад веществ
Река Превращений
В пещере колдунов
Путь домой
Путевые заметки
Слайд 4. Собери рюкзак.
План характеристики вещества:
Определение
Классификация
Примеры
А. Оксиды – это…
В. Кислоты – это…
С. Основания – это…
Д. Соли – это…
На данном этапе необходимо вспомнить определения, классификации всех изученных классов неорганических соединений:
Оксиды- сложные вещества, состоящие из двух элементов, один из которых кислород. Оксиды делятся на: основные и кислотные, солеобразующие и несолеобразующие
Основания – электролиты, которые при диссоциации образуют катионы металла и анионы гидроксогрупп ОН-. Классифицируются на растворимые и нерастворимые,сильные и слабые, однокислотные и многокислотные.
Кислоты – электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Делятся на: одноосновные и многоосновные, растворимые и нерастворимые, кислородные и бескислородные, летучие и нелетучие, сильные и слабые, стабильные и нестабильные.
Соли – электролиты, которые при диссоциации образуют катионы металла (или аммония) и анионы кислотных остатков. Делятся на: средние, кислые и основные.
Слайд 5. Индикаторы – указатели.
Существуют такие вещества, с помощью которых можно определить щёлочь, кислоту и воду в пробирке. У вас имеются пробирки с прозрачными растворами: кислота, щёлочь и вода. С помощью индикатора определите их.
(их можно определить с помощью метилоранжа или лакмуса)
Слайд 6. Этап II-Восхождение.

SO3 – c H2O, Na2O, NaOH
HCl – c Zn, Na2O, NaOH
KOH – c SO3, HCl, CO2
Слайд 7. Этап III – Водопад веществ.
Распределите вещества по классам и назовите их
Al2O3, Mg(NO3)2, H2SO4,CO2, Ca(OH)2, Na2O, H2CO3, Mg, K2O, NaCl, KNO3, H2SiO3, MgO, Na2SO4,N2O5, NaOH, Ca, ZnCl2, CaCO3, Cl2O7, HCL, AL(OH)3, C, ZnSO4, AL2(SO4)3, H2SO3, Mg(OH)2, SiO2
Простые вещества: металлы- Mg, Ca; неметаллы - C
Сложные вещества:
Оксиды - Al2O3, CO2, Na2O, , K2O, MgO, N2O5 ,Cl2O7, SiO2
Основания - Ca(OH)2, NaOH, AL(OH), , Mg(OH)2
Кислоты - H2SO4, H2CO3, H2SiO3, HCL, , H2SO3
Соли - Mg(NO3)2, NaCl, KNO3, Na2SO4, ZnCl2, CaCO3, ZnSO4, AL2(SO4)3
Слайд 8. Этап IV. Река превращений
Осуществите ряд превращений:
Cu → CuO → CuSO4 → Cu(OH)2
Назовите полученные вещества.
Cu + O2 = CuO CuO + H2SO4= CuSO4 + H2O CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
Слайд 9. Этап V. В пещере колдунов
Допишите уравнения реакций:
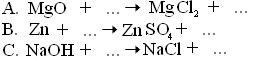
Экспериментально осуществите эти превращения.
MgO + 2HCl = MgCl2 + H2O
Zn + H2SO4 = ZnSO4 + H2
NaOH + HCl = NaCl + H2O
Слайд 10. Этап VI. Путь домой
Al2O3, Mg(NO3)2, H2SO4,CO2, Ca(OH)2, Na2O, H2CO3, Mg, K2O, NaCl, KNO3, H2SiO3, MgO, Na2SO4, N2O5, NaOH, Ca, ZnCl2, CaCO3, Cl2O7, HCL, AL(OH)3, C,ZnSO4, AL2(SO4)3, H2SO3, Mg(OH)2, SiO2
Составьте генетическую связь между классами неорганических соединений:
Слайд 11. Проверьте себя
Mg → MgO → Mg(OH)2 → Mg(NO3)2 - Генетический ряд металла
C → CO2 → H2CO3 → CaCO3 - Генетический ряд неметалла
Слайд 12. Этап VII. Путевые заметки
Слайд 13. Домашнее задание:
Царь зовёт к себе Стрельца,
Удалого молодца,
И даёт ему поручение
Государственного значения.
Чтоб я стал опять богат,
Нужен бария сульфат.
Ночь даю тебе подумать –
Утром буду ждать доклад!
Не смогёшь - кого винить?
Должен я тебя казнить.
Запиши себе названье,
Чтоб со страху не забыть.
1). Помогите Стрельцу получить возможными способами сульфат бария.
2). §42, с. 169-171
3. Заключение по уроку. Выставление отметок.
Просмотр содержимого презентации
«Презентация1»


Наши цели:
- Закрепить и углубить знания об основных классах неорганических веществ;
- Повторить характеристику оксидов, кислот, оснований, солей;
- Развить умения составлять уравнения реакции;
- Совершенствовать умения экспериментально подтверждать химические свойства различных веществ.
Для выполнения целей мы совершим путешествие по загадочным местам

Этапы маршрута
- Собери рюкзак
- Восхождение
- Водопад веществ
- Река Превращений
- В пещере колдунов
- Путь домой
- Путевые заметки

Этап I . Собери рюкзак
План характеристики вещества:
- Определение
- Классификация
- Примеры
А. Оксиды – это…
В. Кислоты – это…
С. Основания – это…
Д. Соли – это…

Индикаторы – «Указатели».
Индикатор
Цвет индикатора
В чистой воде (нейтральная среда)
Лакмус
В растворах кислот
(кислая среда)
Метилоранж
В растворах щелочей
(щелочная среда)
Фенолфталеин

Этап II . Восхождение

Этап III . Водопад веществ
Распределите вещества по классам и назовите их
Al 2 O 3 , Mg(NO 3 ) 2 , H 2 SO 4 ,CO 2 ,
Ca(OH) 2 , Na 2 O, H 2 CO 3 , Mg, K 2 O,
NaCl, KNO 3 , H 2 SiO 3 , MgO, Na 2 SO 4 ,N 2 O 5 , NaOH, Ca
ZnCl 2 ,
CaCO 3 , Cl 2 O 7 , HCL, AL(OH) 3 , C,
ZnSO 4 , AL 2 (SO4) 3 , H 2 SO 3 ,
Mg(OH) 2 , SiO 2

Этап IV . Река превращений
Осуществите ряд превращений:
Cu → CuO → CuSO 4 → Cu(OH) 2
Назовите полученные вещества.

Этап V . В пещере колдунов
Допишите уравнения реакций:
Экспериментально осуществите эти превращения.

Этап VI . Путь домой
Al 2 O 3 , Mg(NO 3 ) 2 , H 2 SO 4 ,CO 2 ,
Ca(OH) 2 , Na 2 O, H 2 CO 3 , Mg, K 2 O,
NaCl, KNO 3 , H 2 SiO 3 , MgO, Na 2 SO 4 , N 2 O 5 , NaOH, Ca, ZnCl 2 ,
CaCO 3 , Cl 2 O 7 , HCL, AL(OH) 3 , C,
ZnSO 4 , AL 2 (SO 4 ) 3 , H 2 SO 3 ,
Mg(OH) 2 , SiO 2
Составьте
генетическую связь
между классами
неорганических соединений.

Проверьте себя
Mg → MgO → Mg(OH) 2 → Mg(NO 3 ) 2
Генетический ряд металла
C → CO 2 → H 2 CO 3 → CaCO 3
Генетический ряд неметалла

Этап VII . Путевые заметки
- Дополните записи урока – оформите дневник путешественника

Домашнее задание:
Царь зовёт к себе Стрельца, Удалого молодца, И даёт ему поручение Государственного значения. Чтоб я стал опять богат, Нужен бария сульфат. Ночь даю тебе подумать – Утром буду ждать доклад! Не смогёшь - кого винить? Должен я тебя казнить. Запиши себе названье, Чтоб со страху не забыть .
1. Помогите Стрельцу получить возможными способами сульфат бария.
2. § 42, с. 169-171