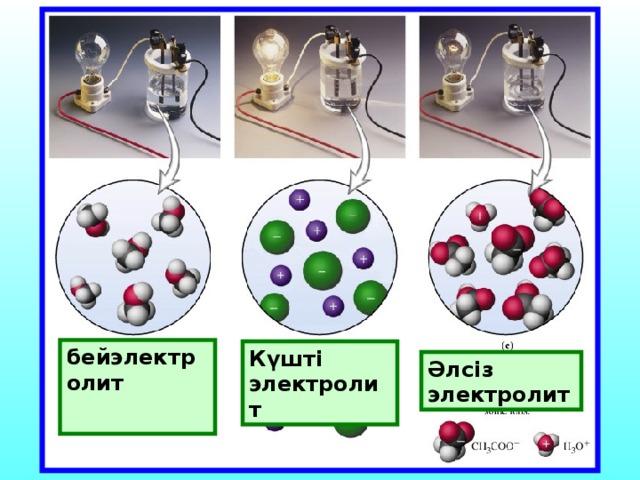
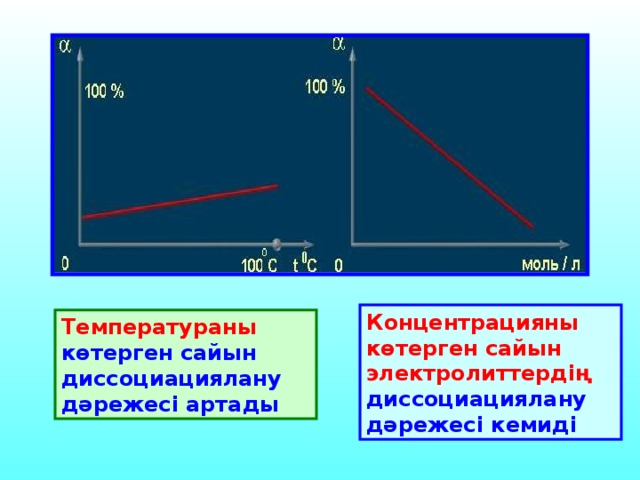
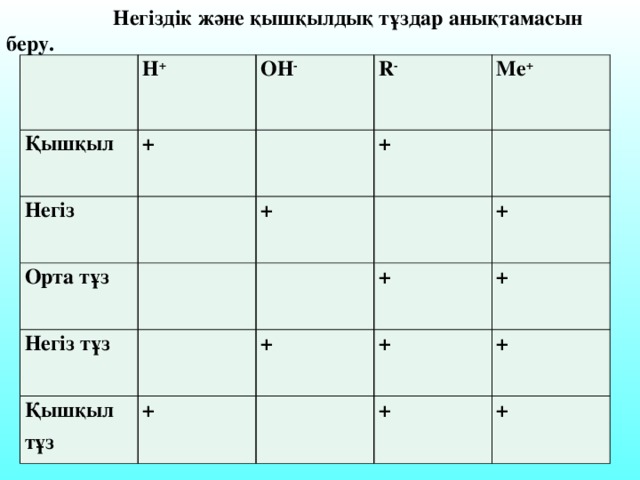
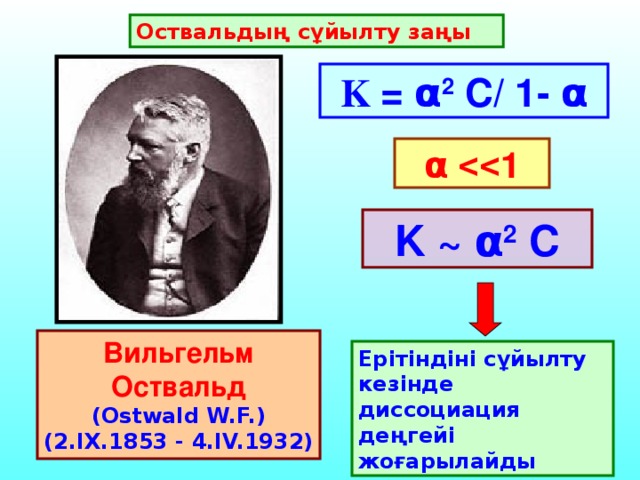
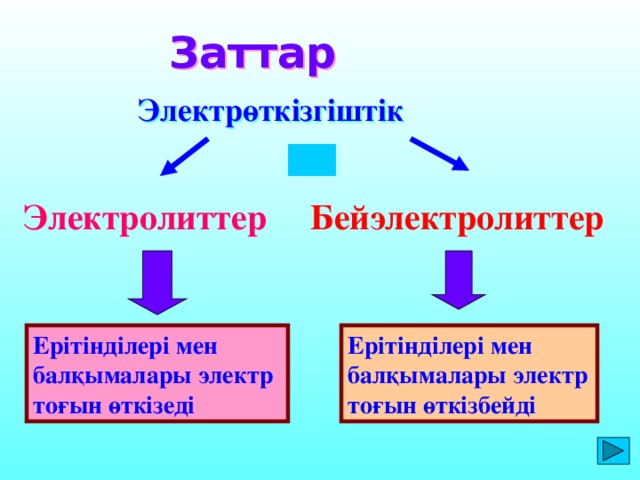
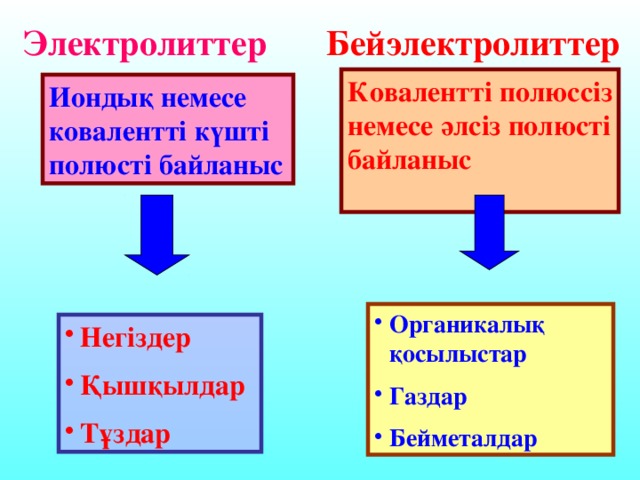
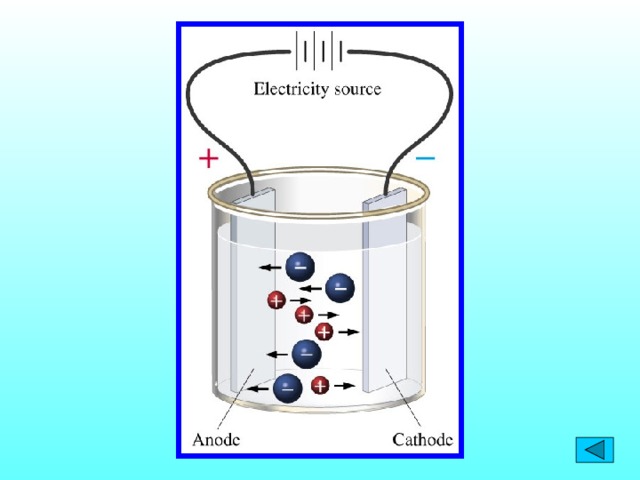
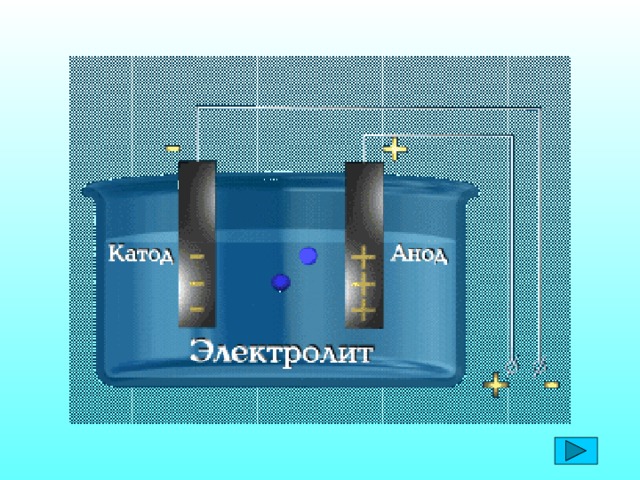
C. Аррениус теориясын толы?тыр?ан ?алымдар - И.А. Каблуков, В.А. Кистяковский, Д.И. Менделеев. Диссоциацияланатын заттар электролиттер, ал диссоциация?а ?шырамайтын заттар бейэлектролиттер. Т?здар, ?ыш?ылдар, негіздер ерігенде ж?не бал?ы?анда иондар?а ыдырайды. ерітінділер мен бал?ымаларды? ток ?ткізгіштігі осы иондарды? концентрациясына т?уілді болады, оларды? о? зарядтал?аны катод?а тартылатынды?тан катиондар деп, ал анод?а тартылатындары аниондар деп аталады.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
Презентация "Электролиттік диссоциация теориясы"
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«презентация "Электролиттік диссоциация теориясы" »
Полезное для учителя
Распродажа видеоуроков!
1660 руб.
2760 руб.
1880 руб.
3140 руб.
1880 руб.
3140 руб.
1660 руб.
2760 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства











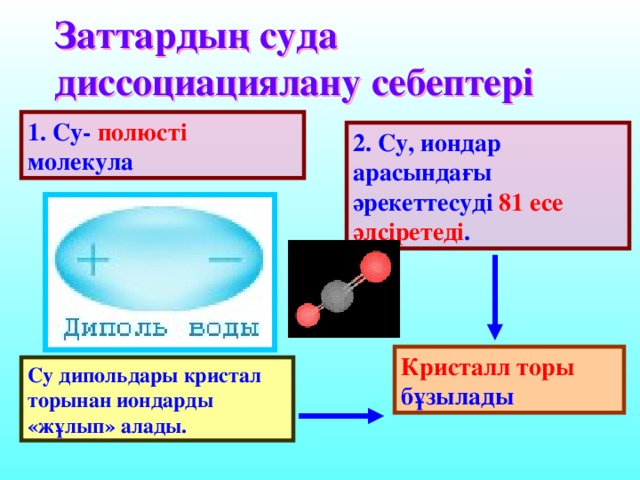

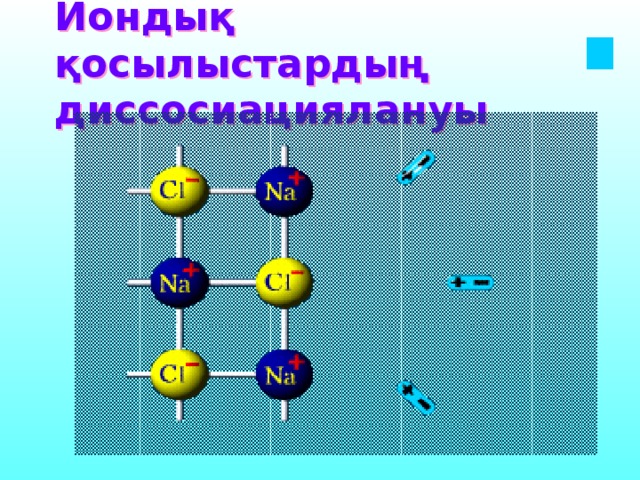
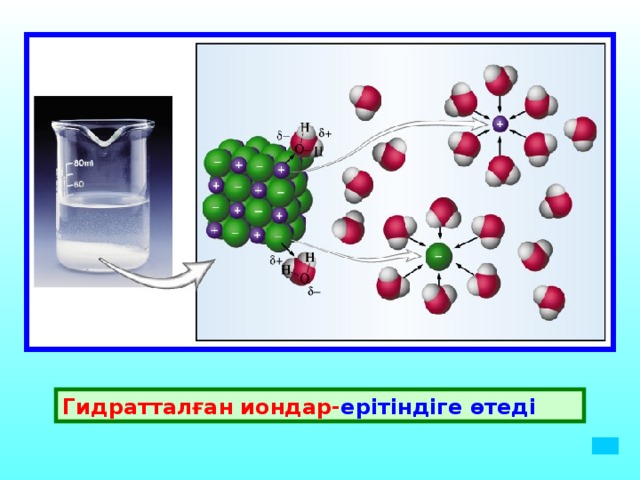



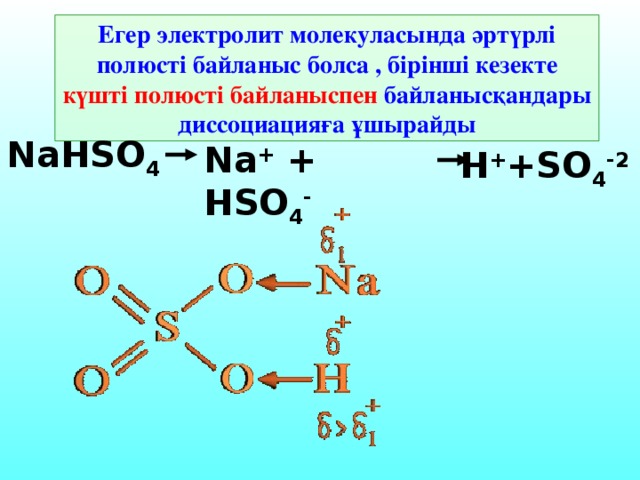

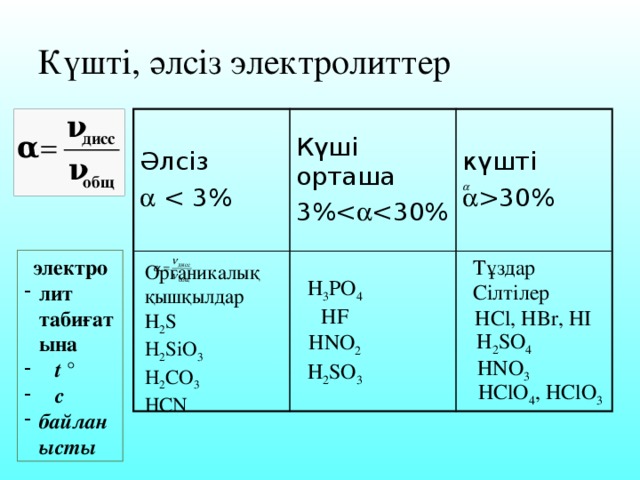 30% электро Тұздар лит табиғатына t ° с байланысты Органикалық қышқылдар Н 2 S H 2 SiO 3 H 2 CO 3 HCN H 3 PO 4 HF HNO 2 H 2 SO 3 Сілтілер HCl, HBr, HI H 2 SO 4 HNO 3 HClO 4 , HClO 3" width="640"
30% электро Тұздар лит табиғатына t ° с байланысты Органикалық қышқылдар Н 2 S H 2 SiO 3 H 2 CO 3 HCN H 3 PO 4 HF HNO 2 H 2 SO 3 Сілтілер HCl, HBr, HI H 2 SO 4 HNO 3 HClO 4 , HClO 3" width="640"