oОбщая характеристика ХАЛЬКОГЕНОВ
КИСЛОРОД
oХАЛЬКОГЕНЫ
oЭто элементы 6 группы
главной подгруппы ПСХЭ
Д.И.Менделеева.
oO – Кислород
oS – Сера
oSe – Селен
oTe – Теллур
oPo – Полоний
oВсе элементы являются НЕМЕТАЛЛАМИ.
oХАЛЬКОГЕНЫ
oХалькогены – «рождающие руды».
oМногие соединения этих элементов – оксиды и сульфиды – являются РУДАМИ.
oFe2O3 – красный железняк
oFe2O3 * H2O – бурый железняк
oFe3O4 – магнитный железняк
oCaO – негашеная известь.
oFeS – пирит.
oZnS – цинковая обманка,
oCuS – медный блеск,
oPbS – свинцовый блеск.
oЭЛЕКТРОННОЕ СТРОЕНИЕ
o+8 О 2е 6е
o+16 S 2е 8е 6е
o+34 Se 2е 8е 18е 6е
o+52 Te 2е 8е 18е 18e 6е
o+84 Po 2е 8е 18е 18e 32e 6е
o
oЧто общего в атомном строении всех элементов 6 группы ПСХЭ?
oОдинаковое строение внешнего электронного слоя, у всех элементов на внешнем энергетическом уровне по 6 е.
oДо завершения у них не хватает по 2е, поэтому эти электроны принимают от МЕТАЛЛОВ и от менее ЭО НЕМЕТАЛЛОВ.
o
oВ пределах группы окислительные (неметаллические) свойства с верху
уменьшаются вниз
oВосстановительные (металлические) свойства увеличиваются с верху
вниз
oО – самый сильный окислитель.
oSe,Te,Po – самые сильные восстановители – проявляют металлические свойства – металлический блеск.
oРо – радиоактивный металл.
o
oСТЕПЕНЬ ОКИСЛЕНИЯ
oКИСЛОРОД – самый сильный окислитель.
oВсегда окислитель – с.о. -2 – оксиды, -1 – пероксиды.
oТолько с ФТОРОМ – восстановитель, так как он более ЭО – с.о. +2
oСТЕПЕНЬ ОКИСЛЕНИЯ
oСЕРА – менее окислитель.
oМожет быть ВОССТАНОВИТЕЛЕМ – с металлами и неметаллами с большей ЭО – с.о. +4, +6.
oМожет быть ОКИСЛИТЕЛЕМ – с неметаллами с меньшей ЭО – с.о. -1, -2.
oКИСЛОРОД
oКислород – газ, без цвета, без запаха.
oБывает в жидком состоянии – светло-голубой.
oБывает в твердом состоянии – светло-голубой.
ot плав = -218, 7 градусов.
ot кип = -183 градуса.
o
oПОЛУЧЕНИЕ КИСЛОРОДА
oВ промышленности: из жидкого воздуха.
oВ лаборатории:
o- разложением перманганата калия при нагревании:
o 2KMnO4= K2MnO4 + MnO2 + O2
oразложением перокисда водорода в присутствии катализатора – оксида марганца – MnО2;
oВЫПОЛНИТЕ ЗАДАНИЕ
№3 на стр 129.
o- разложением перокисда водорода в присутствии катализатора – оксида марганца – MnО2:
o2H2O2 = 2H2O + O2
o2O-1 +2e O20 - окислитель
oO-1 -1e O-2 - восстановитель
o
oВЫПОЛНИТЕ ЗАДАНИЕ
№4 на стр 129.
o2HgO = 2 Hg + O2 - нагревание.
o
oHg+2 -2е Hg0 - восстановитель
o2O-2 +4е O02 -окислитель
o
o1. Химическое свойство
oС МЕТАЛЛАМИ – оксиды.
o- основной оксид
o2Ca + O2 = 2CaO
oCa0 -2e Ca+2 - восстановитель
oO20 +4e 2O-2 -окислитель
o
o- амфотерный оксид
o4Al + 3O2 = 2Al2O3
oAl0 -3e Al+3 – восстановитель
oO20 +4e 2O-2 -окислитель
o
o
o
o- ПЕРОКСИД
o2Na + O2 = Na2O2
oNa0 -1e Na+1 – восстановитель
oO20 +4e 2O-2 -окислитель
o2. Химическое свойство
oС НЕМЕТАЛЛАМИ – кислотные оксиды.
o4P + 5O2 = 2P2O5
oР0 -5e P+5 – восстановитель
oO20 +4e 2O-2 -окислитель
o
oS + O2 = SO2
oS0 -4e S+4 – восстановитель
oO20 +4e 2O-2 -окислитель
o
o3. Химическое свойство
oПри взаимодействии с фтором кислород – восстановитель.
oВЫПОЛНИТЕ ЗАДАНИЕ
№8 на стр 129.
o
o2F2 + 2H2O = 4HF + O2
oF20 +2e 2F-1 – окислитель
o2O-2 -4e O20 - восстановитель
o
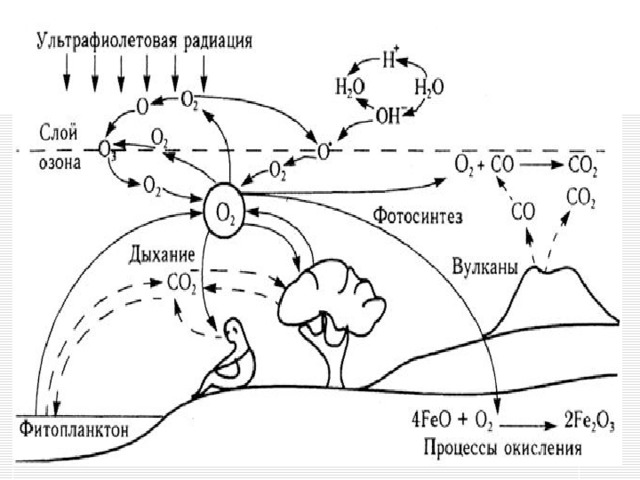
oЗНАЧЕНИЕ КИСЛОРОДА
oДля дыхания
oДля реакций горения
oПродукт фотосинтеза
oПрименяется в медицине
oПрименяется в промышленности – для ускорения производства.
o
o
oДОМАШНЕЕ ЗАДАНИЕ
oПрочитать параграф.
oВыполнить задания № 1,2,5 страница 129.
o