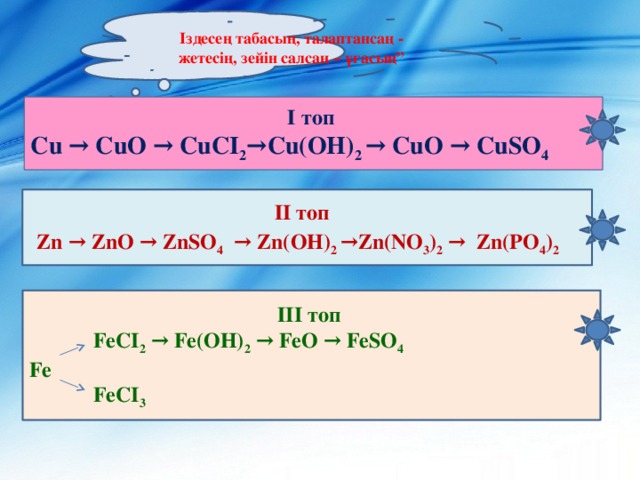
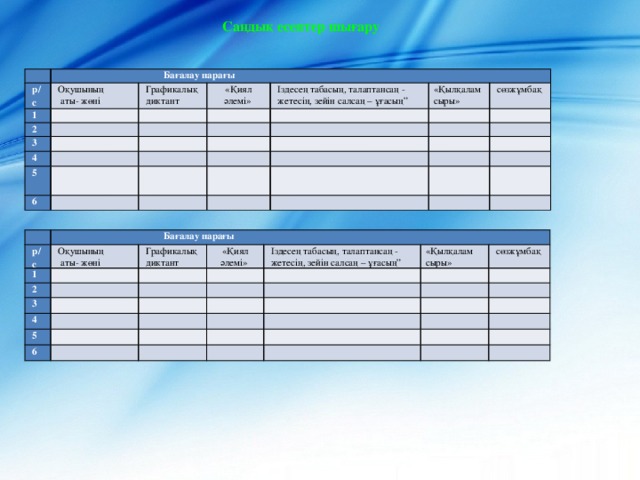
Саба?ты? ма?саты: О?ушыларды? металдарды? жалпы ?асиеттері тарауы бойынша ал?ан білімдерін ж?йелеу ж?не ?орытындылау. Санды? есептер шы?ару да?дысын ?алыптастыру.
К?тілетін н?тиже: О?ушылар сын т?р?ысынан ойланып, бір-бірімен диалог?а т?сіп, тапсырмаларды топпен орындайды. Формативті ж?не критериалды ба?алау ар?ылы білімдерін ?орытындылайды.
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
Химиялы? те?деу бойынша , бір зат арты? болатын есептеулер.
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Химиялы? те?деу бойынша , бір зат арты? болатын есептеулер. »
Полезное для учителя
Распродажа видеоуроков!
1700 руб.
2840 руб.
1700 руб.
2840 руб.
1660 руб.
2760 руб.
1690 руб.
2820 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства








 ν (H 2 SO 4 ) V m = 22,4 л/моль V (Н 2 ) = ν · V m = 1 моль · 22,4 л/моль 13 г Zn ----- х л Н 2 65 г Zn ---- 22,4 л Н 2" width="640"
ν (H 2 SO 4 ) V m = 22,4 л/моль V (Н 2 ) = ν · V m = 1 моль · 22,4 л/моль 13 г Zn ----- х л Н 2 65 г Zn ---- 22,4 л Н 2" width="640"