1. Суды? кермектілігі дегеніміз не?
2. Суды? кермектілігіні? неше т?рі бар?
3. Уа?ытша кермектілік дегеніміз не?
4. Т?ра?ты кермектілік дегеніміз не?
5. Кермектілікті жою жолдары ?андай?
Просмотр содержимого документа
«Алюминий ж?не оны? ?осылыстары (презентация)»

1 . Судың кермектілігі дегеніміз не?
2. Судың кермектілігінің неше түрі бар?
3 . Уақытша кермектілік дегеніміз не?
4 . Тұрақты кермектілік дегеніміз не?
5. Кермектілікті жою жолдары қандай?

Алюминий және оның қосылыстары, алюминийдің маңызы. Табиғи қосылыстары және олардың Қазақстандағы
кен орындары
Табиғатта кездесуі
Физикалық қасиеті
Атом құрылысы
Алюминий
және оның қосылыстары
Химиялық қасиеттері
Периодтық жүйедегі орны
Қолданылуы
Алынуы
Қосылыстары
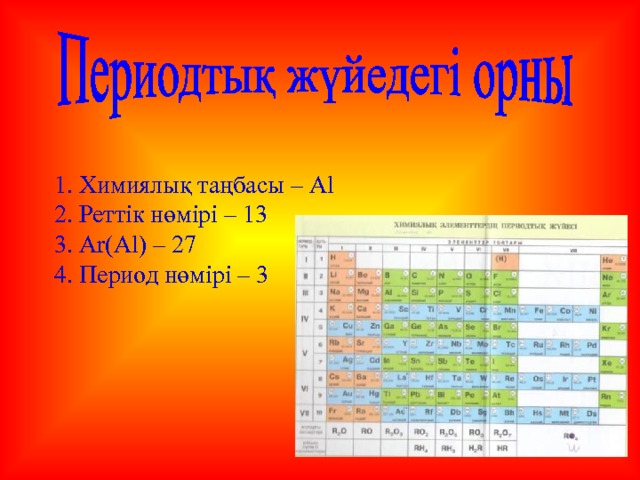
1. Химиялық таңбасы – Al
2. Реттік нөмірі – 13
3. Ar(Al) – 27
4. Период нөмірі – 3

1.Ядро заряды – 13
2 .Протон саны – 13
3 .Нейтрон саны – 14
4. Электрон саны – 13
5.Тотығу дәрежесі – 0, +3
6.Валенттілігі – III
7. Электрондық формуласы – 1s 2 2s 2 2p 6 3s 2 3p 1

Табиғатта таралуы:
Ақ саз - Al 2 O 3 · 2SiO 2 · 2H 2 O ;
Ортоклаз, далалық шпат – K 2 O · Al 2 O 3 · 6 SiO 2 ;
C люда – K 2 O · 3Al 2 O 3 · 6 SiO 2 · 2H 2 O;
Нефелин – Na 2 O · K 2 O · Al 2 O 3 ;
Корунд - (Al 2 O 3 ) Боксит - (Al 2 O 3 · 2H 2 O)

Түсі- күмістей ақ,
Тығыздығы: p=2.7 г/см3
Электр тогы мен жылуды жақсы өткізеді, оңай созылады, жаншылады.

Химиялық қасиеттері:
А) жай заттармен әрекеттесуі;
- 4Al+3O 2 →2Al 2 O 3
- 2Al+3Cl 2 →2AlCl 3
- Al+P→AlP Al фосфиді
- 4Al+3C→Al 4 C 3 Al карбиді
Ә) күрделі заттармен:
1) 2 Al+6HOH→2Al(OH) 3 ↓ +3H 2 ↑
2) 2Al+6HCl=2AlCl 3 +3H 2 ↑
3) 2Al+3CuSO 4 = Al 2 (SO 4 ) 3 +3Cu
4) 2Al+2NaOH+2H 2 O=2NaAlO 2 +3H 2 ↑
натрий алюминаты
5) 2Al+Fe 2 O 3 =Al 2 O 3 +2Fe
алюмотермия реакциясы

Алюминий қосылыстары
Al 2 O 3 – ақ түсті, қатты зат. Суда ерімейді.
Құрылымдық формуласы: О = Al – O – Al = O
Al(OH) 3 – іркілдек, ұйыған айран тәрізді ақ түсті зат.
Құрылымдық формуласы :
H – O
H – O Al
H – O
Al(OH) 2 Cl Al(OH)Cl 2
O – H O – H
Al O – H Al Cl
Cl Cl


1 . Мына айналуларды жүзеге асыруға болатын реакция теңдеулерін жаз.
Al 2 (SO 4 ) 3 → A lCl 3 → Al(OH) 3
2. Массасы 5,4 г алюминийді еріту үшін қанша 10%- дық тұз қышқылының массасы қажет?

Алюминий қосылыстарының атаулары
Химиялық формуласы
Алюминий оксиді
Алюминий сульфаты
Алюминий гидроксиді
Алюминий хлориді
Алюминий нитраты
Алюминий бромиді

§3 5 -36. Алюминий және оның қосылыстары, алюминийдің маңызы. Табиғи қосылыстары және олардың Қазақстандағы
кен орындары