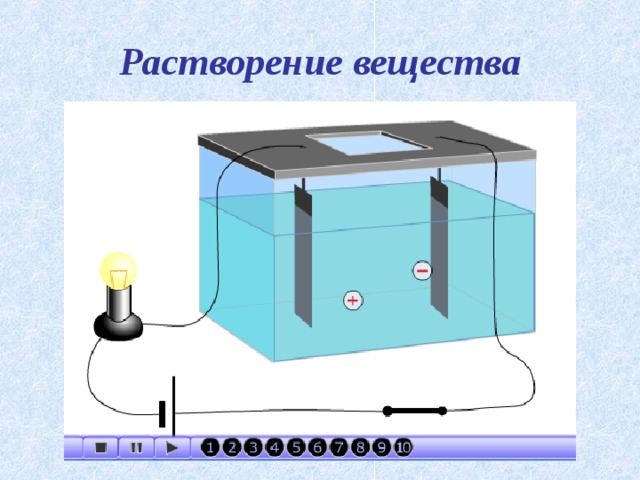
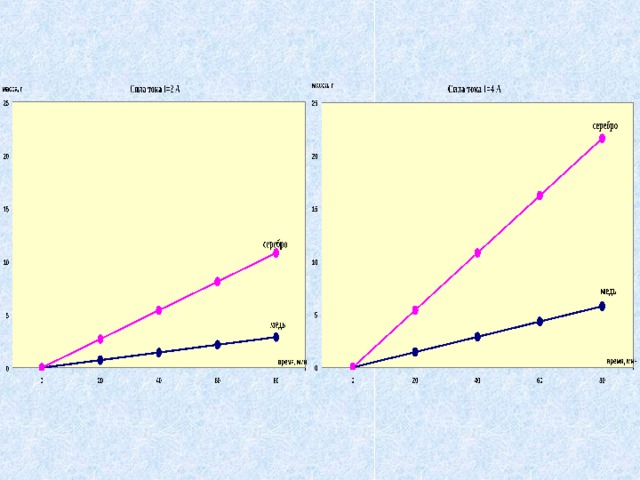
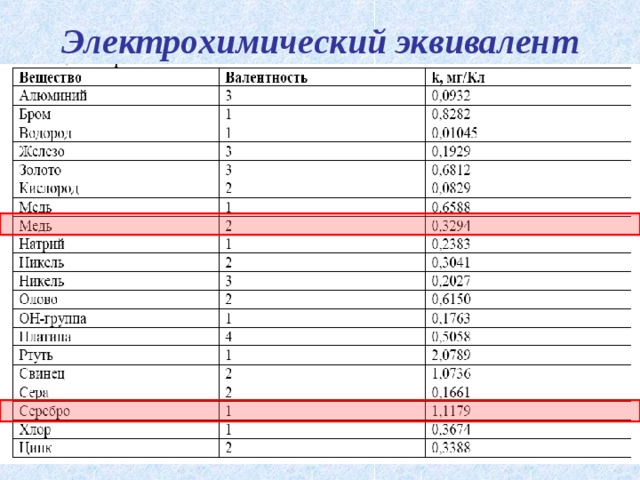
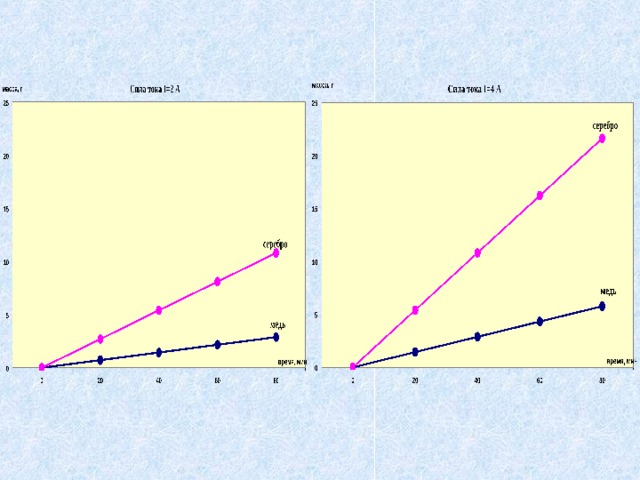
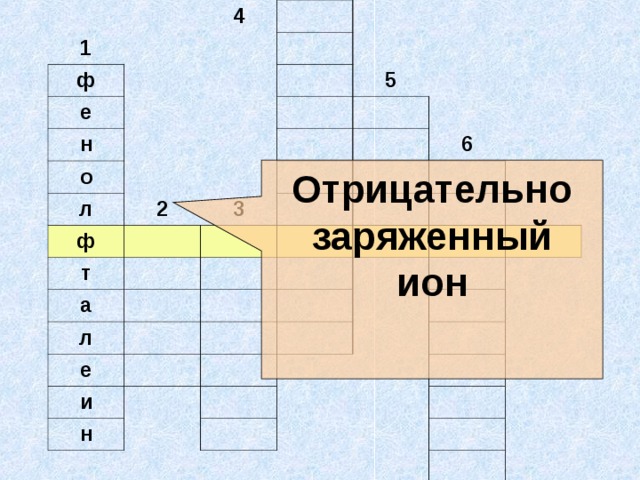
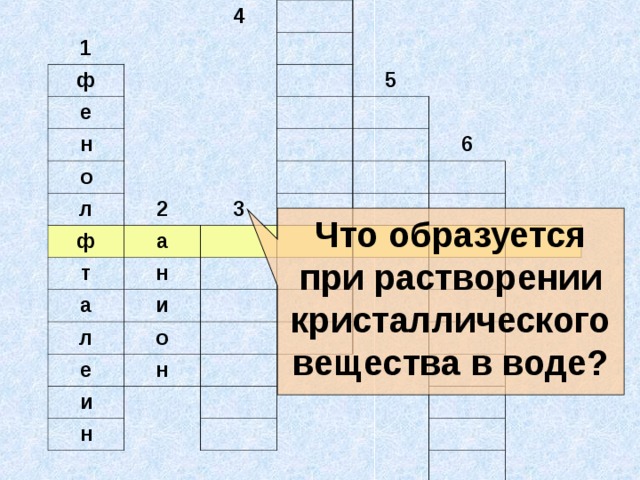
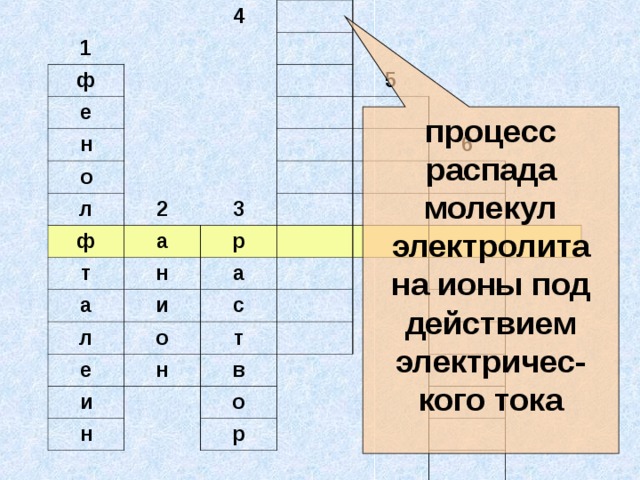
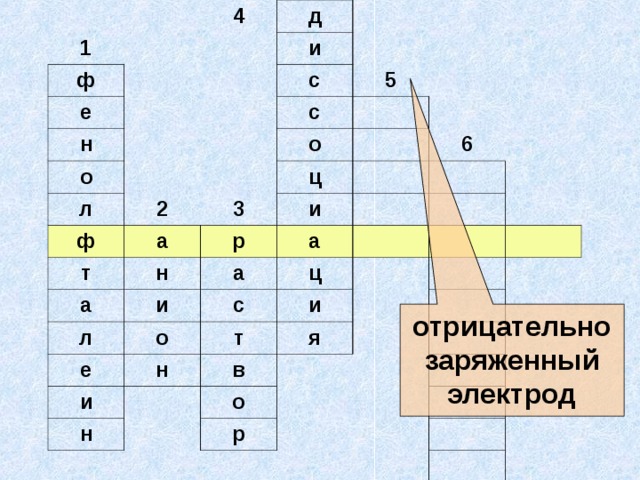
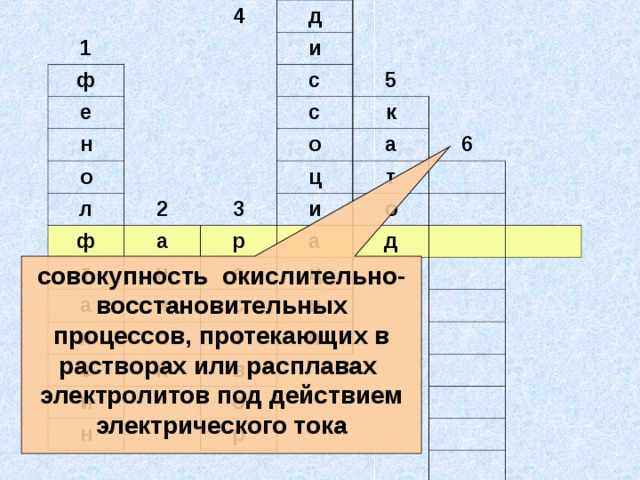
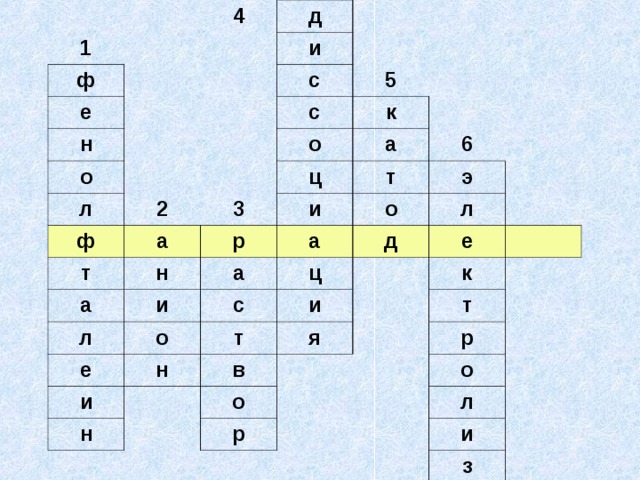
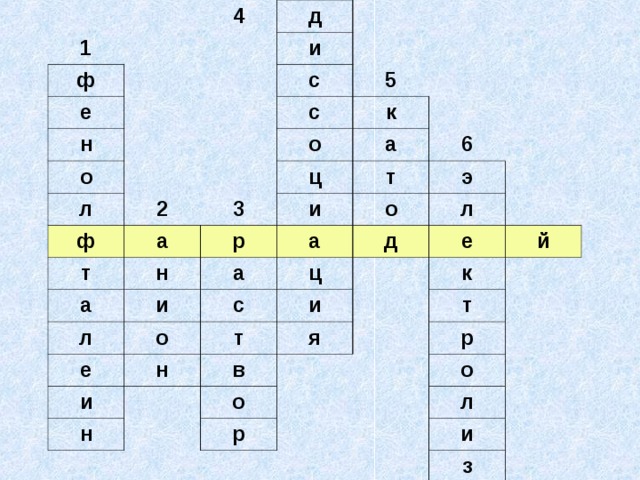
Презентация к интегрированному уроку химии и физики для 11 класса по теме «Электрический ток в жидкостях. Закон электролиза»
Создайте Ваш сайт учителя Видеоуроки Олимпиады Вебинары для учителей
Презентация к интегрированному уроку химии и физики для 11 класса по теме «Электрический ток в жидкостях. Закон электролиза»
Вы уже знаете о суперспособностях современного учителя?
Тратить минимум сил на подготовку и проведение уроков.
Быстро и объективно проверять знания учащихся.
Сделать изучение нового материала максимально понятным.
Избавить себя от подбора заданий и их проверки после уроков.
Наладить дисциплину на своих уроках.
Получить возможность работать творчески.
Просмотр содержимого документа
«Презентация к интегрированному уроку химии и физики для 11 класса по теме «Электрический ток в жидкостях. Закон электролиза»»
Полезное для учителя
Распродажа видеоуроков!
1510 руб.
2510 руб.
1610 руб.
2690 руб.
1670 руб.
2780 руб.
1520 руб.
2530 руб.
ПОЛУЧИТЕ СВИДЕТЕЛЬСТВО МГНОВЕННО
* Свидетельство о публикации выдается БЕСПЛАТНО, СРАЗУ же после добавления Вами Вашей работы на сайт
Удобный поиск материалов для учителей
Проверка свидетельства