ФИЗИКА – 8 «Б» класс
Тема: Электрический ток в металлах и электролитах.
Закон электролиза. Применение электролиза.
•Цели и задачи урока:
•Воспитание гармонически развитой личности, формирование положительной самооценки, путем развития интереса к предмету и вовлечения каждого учащегося в учебную деятельность. Перевести учащихся из объекта в субъект воспитания и обучения.
•Развитие логического мышления, всех видов памяти, умение выделять главное, самостоятельно получать знания, используя учебную литературу и учебное оборудование, развитие умения объяснять физические явления на основе полученных знаний, применять полученные знания на практике.
•Изучение новой главы «Электрический ток в различных средах». Объяснить учащимся, что есть электрический ток в металлах и электролитах. Ввести учащимся понятие электролиза. Рассмотреть применение электролиза.
Оборудование: 1) доска, мел, пояснительные рисунки;
• 2) слайды, раздаточный материал
Ход урока:
1.Организационный момент: цели урока, присутствующие.
2.Актуализация знаний.
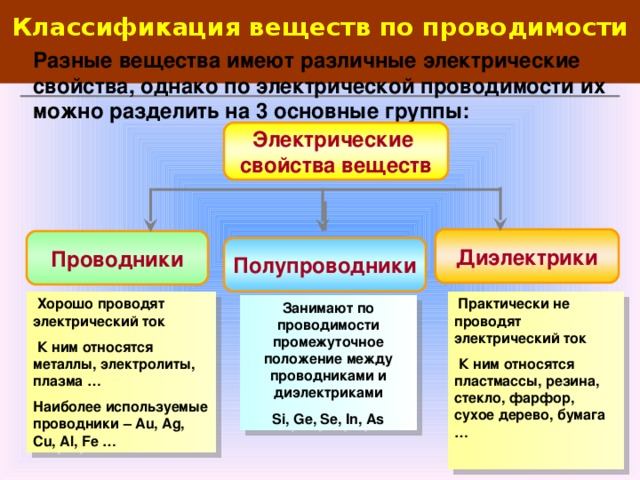
Разные вещества имеют различные электрические свойства, однако по электрической проводимости их можно разделить на 3 основные группы: проводники, полупроводники и диэлектрики.
3.Изучение нового материала:
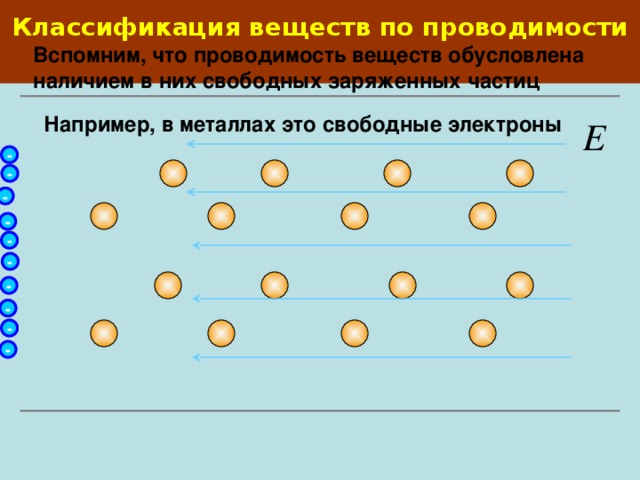
- Электрический ток в металлах представляет собой упорядоченное движение свободных электронов.
- Скорость движения электронов в металле под действием электрического поля не велика. Скорость же распространения самого электрического поля внутри проводника огромна, она приблизительно равна скорости света, т.е. 300 000км/с.
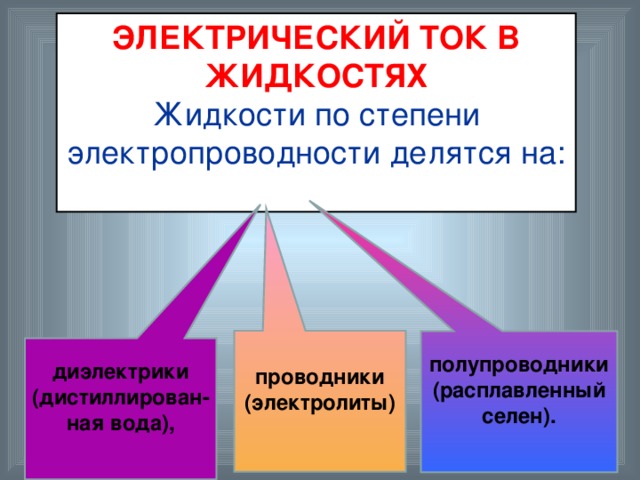
ЭЛЕКТРИЧЕСКИЙ ТОК В ЖИДКОСТЯХ
Жидкости по степени электропроводности делятся на:
*диэлектрики (дистиллирован-ная вода),
*проводники (электролиты)
*полупроводники (расплавленный селен).
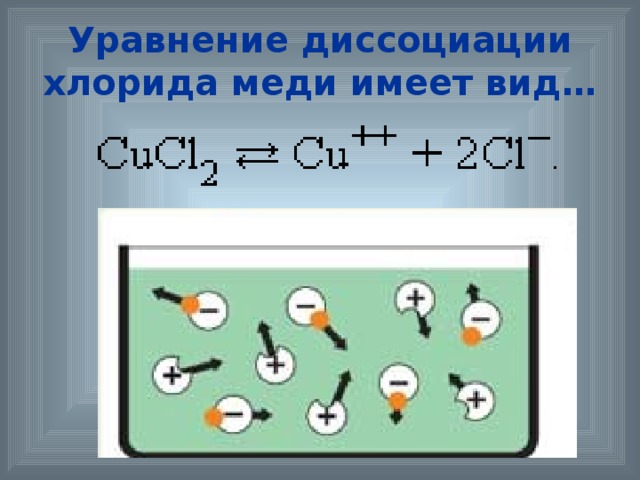
Электролиты – это …
водные растворы солей, кислот и щелочей, а также расплавы солей и металлов. Электролиты являются хорошими проводниками электрического тока.
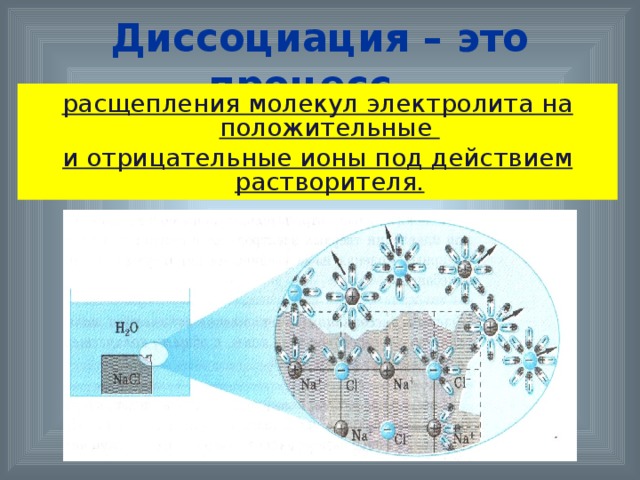
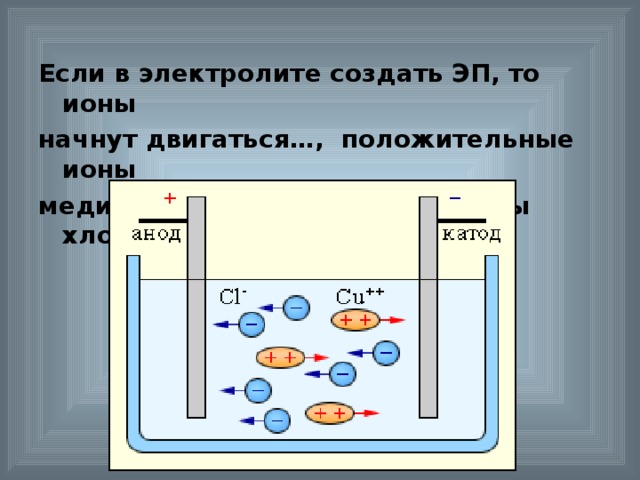
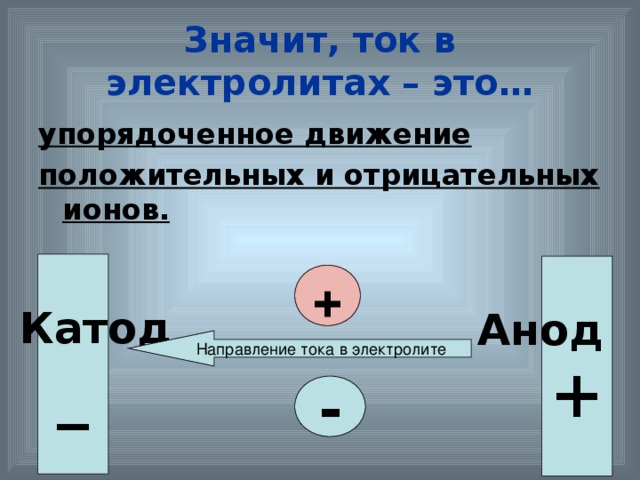
Носителями заряда в электролитах являются - положительные и отрицательные ионы.
Электролиз – это явление- выделения на электродах веществ, входящих в состав электролита, при протекании через него электрического тока.
Закон Фарадея для электролиза формулируется так…
Масса m вещества, выделившегося на электроде, прямо пропорциональна заряду q, прошедшему через электролит:
m = kq = kIt.
Величину k называют электрохимическим эквивалентом, измеряют в
и находят для разных веществ в таблице.
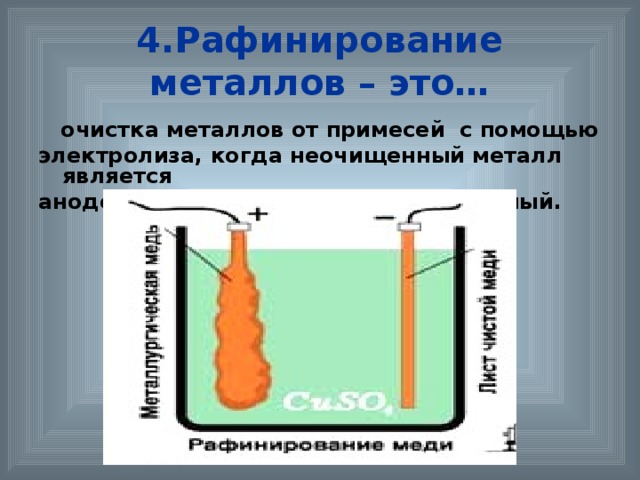
4. Применение электролиза прочитать и посмотреть на слайдах.
5. Итог урока:
• 1) домашнее задание: §45-47, упр 23 (5)
•2) выставление оценок